Tack alla läsare och forskare som har bidragit med texter på Nutritionsfakta under året. Vi önskar er alla en riktigt fin ledighet. Tack för i år!
Arkiv
Global Burden of Disease – jämför världens största sjukdomar och hälsorisker
Du som är intresserad av folkhälsonutrition har säkert stött på formuleringar i stil med: ”Ohälsosamma matvanor orsakar fler dödsfall än tobak i Sverige.” Men hur väl stämmer det? Betyder det att en korv är lika skadlig som en cigarett? Kan man verkligen jämföra sådana riskfaktorer?
Bakom dessa siffror ligger en omfattande och ambitiös studie med syftet att kartlägga och rangordna data om hälsa och dess bestämningsfaktorer världen över. Resultaten är fascinerande och pekar ut ohälsosamma matvanor som en mycket viktig faktor. Samtidigt är studien komplicerad, och metoderna inte alltid lätta att överblicka. Här förklaras några av de begrepp du kan möta om du vill tolka resultaten från studien.
>>text: Emma Patterson, docent i folkhälsovetenskap, nutritionist, Avdelningen för risk- och nyttovärdering, Livsmedelsverket, Uppsala och adjungerad lektor i folkhälsonutrition, Institutionen för global folkhälsa, Karolinska Institutet, Stockholm
En ambitiös studie
Om man har läst en artikel om hur viktig matvanorna är för hälsan har man med stor sannolikhet stött på statistik från Global Burden of Disease-studien (GBD), liknande den ovan. Studien är ett omfattande och ambitiöst försök att sammanställa data om ohälsa och ohälsans bestämningsfaktorer världen över.
Studien kartlägger de vanligaste dödsorsakerna och sjukdomarna, land för land. Den identifierar också de viktigaste bestämningsfaktorerna, eller riskfaktorerna, som är kopplade till dessa utfall samt hur vanligt förekommande de är. Studiens kärna är avancerade modeller som uppskattar hur stor del av den totala ohälsan som orsakas av varje sjukdom eller riskfaktor.
Prioriteringar och jämförelser
Syftet med studien är att med hjälp av data kunna identifiera och rangordna hälsoproblem och riskfaktorer på ett jämförbart sätt. Målet är att kunna prioritera mellan mycket olika typer av sjukdomar och riskfaktorer så att åtgärder kan riktas mot rätt problem. Man kan till exempel undersöka om relaterade insatser, såsom lagstiftning eller forskningsmedel, står i proportion till hälsoproblem. Eftersom en standardiserad metodik används är tanken att man ska kunna jämföra mycket olika riskfaktorer. Ytterligare jämförelser är möjligt mellan länder och regioner, över tid, mellan kön och så vidare.
Vilka står bakom?
Det var Världshälsoorganisationen (WHO) som drog igång den första GBD-studien redan 1992 på uppdrag av World Bank (1). Den version som idag benämns GBD-studien utförs av Institute for Health Metrics Evaluation (IHME) i Seattle, USA, som grundades 2007 med finansiering bland annat från Bill & Melinda Gates Foundation. Eftersom WHO och IHME har väldigt olika uppdrag, förutsättningar och skyldigheter har visionen om att enas kring en enda GBD-studie visat sig svårt att förverkliga. WHO tar också fram egna hälsoestimat numera, även om visst samarbete förekommer (1, 2).
Sjukdomsbörda som begrepp
En av de unika aspekterna med studier som denna, som undersöker total ohälsa (sjukdomsbörda), är att den inte bara inkluderar dödsfall (mortalitet), utan även tidigt dödsfall, samt sjuklighet (morbiditet). Antalet dödsfall är relativt enkelt att räkna på och nästan alla länder har bra statistik över dödsfall i befolkningen. Men ska ett dödsfall vid 89 års ålder likställas med ett dödsfall vid 63? Hur väger man ohälsa till följd av olika kroniska sjukdomar eller funktionsnedsättningar mot varandra?
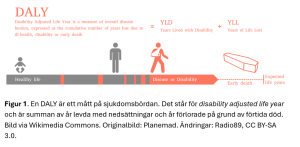
Om man lever med en sjukdom, ett tillstånd eller en funktionsnedsättning har man inte full hälsa – man kanske är blind, orkar inte gå så långt på grund av hjärtsvikt eller man kanske får återkommande migrän. WHO utvecklade till den första GBD-studien konceptet DALYs – disability adjusted life years, vilket innebär förlorade friska levnadsår på grund av ohälsa eller förtida död (figur 1) och detta är det huvudsakliga måttet som används för att uppskatta den totala sjukdomsbördan. Ett förenklat exempel på hur DALYs beräknas: Om en person förväntas leva till 90 år, men får svår hjärtsvikt vid 70 års ålder – något som har bedömts försämra hälsan med 18 %, och dör vid 85 års ålder, motsvarar det (15 × 0,18) + 5 = 7,7 DALYs. Olika hälsoutfall tilldelas olika vikter utifrån en subjektiv bedömning.
Vilka faktorer ingår – och vilka gör det inte?
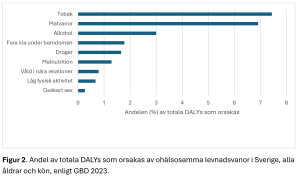
I GBD-studien ingår nästan 90 riskfaktorer, uppdelade i metabola, beteenderelaterade och miljörelaterade faktorer. Bland de beteenderelaterade finns bland annat matvanor, tobak, högt intag av alkohol, låg fysisk aktivitet, drogmissbruk (figur 2). För att en faktor ska ingå ska det finnas god evidens för en koppling till de hälsoutfall som ingår i modellen. Viktigt att notera här är att övervikt och obesitas betraktas som en metabol riskfaktor och inte som ett utfall i sig i modellen.
Femton kostfaktorer
Det finns i nuläget 15 kostfaktorer, och det är en blandning av livsmedel och näringsämnen (figur 3). Kostfaktorerna är: lågt intag av fullkorn, högt intag av chark, högt intag av rött kött, lågt intag av frukt, lågt intag av grönsaker, högt intag av natrium (salt), lågt intag av fleromättat fett, lågt intag av fibrer, lågt intag av baljväxter, lågt intag av nötter och frön, högt intag av sötade drycker, lågt intag av omega 3-fett, lågt intag av mjölk, lågt intag av kalcium och högt intag av transfett. För varje faktor har man identifierat en optimal intagsnivå som teoretiskt innebär lägst risk för ohälsa, samt hur mycket risken ökar (relativa risker) vid intag som ligger över eller under denna nivå. Naturligtvis krävs även här god evidens för ett samband mellan en riskfaktor och ett hälsoutfall. Ett sätt att kvantitativt utvärdera sambandens styrka och form har utvecklats (3) och evidensläget omvärderas då och då (4). Se även stycket ”Uppdateringar sker”.
Hur ska resultaten tolkas?
Ett viktigt koncept att förstå är att rangordningen av hur ”viktig” en riskfaktor är inte enbart är kopplat till hur starkt eller säkert sambandet med utfallet är. Rangordningen är en kombination av hur mycket riskfaktorn ökar risken för ohälsa samt hur vanligt förekommande den är i befolkningen. En mycket vanlig faktor som ökar risken lite kan därför hamna högre än en farligare faktor som är relativt ovanlig. Till exempel ökar ett lågt intag av baljväxter inte risken för sjukdom lika mycket som ett lågt intag av nötter och frön, men eftersom ett intag av baljväxter under den optimala nivån är vanligare i befolkningen orsakar det enligt beräkningarna mer ohälsa totalt sett.
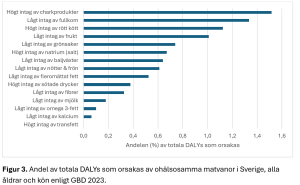
Är riskfaktorerna oberoende av varandra?
När man läser diagrammet på nivån som visas i figur 3 ska det läsas som om matvanorna vore oberoende av varandra. Låt oss ta exemplet med riskfaktorn ”lågt intag av grönsaker”, som enligt figur 3 orsakar 0,75 % av alla DALYs. Lägst risk anses enligt GBD-studien vara vid ett genomsnittligt intag mellan spannet 306–372 gram per dag (5). Ett lägre intag anses i GBD-studien öka risken för bland annat typ-2 diabetes. Ett lågt intag av fibrer ger likadana effekter, och en del av grönsakers skyddande effekt förklaras av fibrer. Det framgår dock inte i stapeldiagrammet som visar andelen av den totala sjukdomsbördan som förklaras av enskilda matvanor. Man bör därför inte själv lägga ihop dessa riskfaktorer. När GBD-studien summerar till nivån som presenteras i figur 2, det som heter ”ohälsosamma matvanor”, då tas vissa överlapp – så kallade medieringseffekter – till exempel mellan grönsaker och fibrer eller mellan mjölk och kalcium, om hand.
Begränsningar
En modell som denna är naturligtvis mycket komplex och svårt att överblicka. Den kräver mycket data av bra kvalitet, som måste harmoniseras. Modellen bygger på flera antaganden, och när data saknas måste modellen kompensera för detta på något sätt. Alla beslut som tagits är inte alltid lätt att följa. Mycket data finns tillgängligt via GBD:s webbplats, vissa data måste man fråga efter. Det är svårt att undvika känslan av en ”svart låda” när man inte kan följa processen i detalj, även om metodbeskrivningar publiceras i omfattande bilagor (5) och en del rådata finns tillgänglig i GBD:s katalog.
Som ett exempel baseras data om matvanornas utgångsläge, det vill säga information om vad befolkningen konsumerar, på ett antal olika källor. I Sverige är det inte enbart baserat på vår senaste nationella matvaneundersökning, utan även på regionala kohortstudier, jordbruksstatistik och viss försäljningsstatistik. Det är förstås klokt att ta tillvara på all tillgänglig data av bra kvalitet, men tyvärr är det svårt att veta exakt vilka data som ingår eller hur de har kombinerats för att komma fram till intagsnivåerna (samt exakt vad det är för nivåer). Att GBD inte är så transparenta i sina metoder är en av de vanligast förekommande kritiken mot studien (1).
Problemet blir än mer påtagligt för länder där data är bristfällig, av osäker kvalitet eller saknas helt. GBD avser att omfatta 204 länder, och för att uppnå detta måste mycket data lånas in och modelleras (2). För Sveriges del är problemet antagligen begränsat när det gäller hälsoutfall tack vare våra registerdata, medan utmaningar med att mäta riskfaktorer är något man bör vara medveten om.
Uppdateringar sker
Modellen uppdateras löpande och nya versioner släpps med några års mellanrum. En ny version, GBD 2023, släpptes den 12 oktober 2025 (6). Det är positivt att modellen utvecklas – dataluckor fylls när nya data finns tillgängliga och antaganden skruvas på när kunskapsläget förändras. Men ibland sker stora förändringar, vilket är viktigt att vara uppmärksam på. I den senaste versionen GBD 2023 förändrades till exempel hur fullkorn uppskattas, och i GBD 2021 bedömdes ett lågt intag av nötter och frön inte längre vara en riskfaktor för typ-2 diabetes. Detta innebär att om man vill jämföra hur viktig en riskfaktor är över tid eller mellan länder måste man använda samma version av GBD-modellen. När en ny version kommer ersätter den tidigare versioner.
Vilka använder resultaten?
Modellen och dess resultat används bland annat av forskare, studenter, lärare, policyutvecklare och planerare. GBD Compare är verktyget där alla resultat kan utforskas interaktivt (7) och där man kan skapa diagram som de som visas i figurerna ovan. Bilderna kan vara mycket användbara i utbildningssyfte – förutsatt att man förstår hur de ska tolkas. På Livsmedelsverket använder vi till exempel en bild på en webbsida riktad till allmänheten om matvanor och sjukdom (8), och en på en sida riktad till dem som jobbar inom hälso- och sjukvården om hur bra matvanor räddar liv (9).
Författaren uppger inga jävsförhållanden.
Referenser
1. Mathers CD. History of global burden of disease assessment at the World Health Organization. Arch Public Health. 2020. 78:77. http://dx.doi.org/10.1186/s13690-020-00458-3
2. Tichenor M, Sridhar D. Metric partnerships: global burden of disease estimates within the World Bank, the World Health Organisation and the Institute for Health Metrics and Evaluation. Wellcome Open Res. 2019. 4:35. http://dx.doi.org/10.12688/wellcomeopenres.15011.2
3. Zheng P, Afshin A, Biryukov S. et al.The Burden of Proof studies: assessing the evidence of risk. 2022. 28, 2038–2044. https://doi.org/10.1038/s41591-022-01973-2
4. Haile D, Harding KL, McLaughlin SA, et al. Health effects associated with consumption of processed meat, sugar-sweetened beverages and trans fatty acids: a Burden of Proof study. Nat Med. 2025 31(7):2244–54. http://dx.doi.org/10.1038/s41591-025-03775-8
5. Brauer M, Roth GA, Aravkin AY, et al. Global burden and strength of evidence for 88 risk factors in 204 countries and 811 subnational locations, 1990–2021: a systematic analysis for the Global Burden of Disease Study 2021. Lancet. 2024. 403(10440):2162–203. https://doi.org/10.1016/S0140-6736(24)00933-4
6. Institute for Health Metrics and Evaluation (IHME) [webbsida]. https://www.healthdata.org
7. Institute for Health Metrics and Evaluation (IHME). GBD Compare Data Visualization. Seattle, WA: IHME, University of Washington. 2024. http://vizhub.healthdata.org/gbd-compare.
8. Matvanor och sjukdom [webbsida]. 2025. https://www.livsmedelsverket.se/matvanor-halsa–miljo/sjukdomar-allergier-och-halsa/matvanor-sjukdom
9. Livsmedelsverket. Bra matvanor räddar liv [webbsida]. 2025. https://www.livsmedelsverket.se/matvanor-halsa–miljo/samtal-om-mat-i-halso–och-sjukvarden/bra-matvanor-raddar-liv
Krononutrition och måltidsmönster i Sverige
Inte bara vad vi äter, utan även när vi äter kan ha betydelse för vår hälsa. Detta studeras inom forskningsfältet krononutrition, där tidpunkter för ätande och dess effekter på livsmedels- och näringsintag och hälsa, såsom risken för hjärt-kärlsjukdom, studeras. I en ny studie har svenskarnas måltidsmönster analyserats för att undersöka hur de skiljer sig mellan olika grupper i befolkningen samt vilka samband som finns med näringsintaget.
>>text: Jenny Schultz, doktorand vid Institutionen för kostvetenskap, Uppsala universitet, Uppsala
Måltidsmönster handlar om hur måltiderna fördelas över dygnet, där antal måltider, nattlig fasta, regelbundenhet, tidpunkt för dagens första och sista måltid och att inte äta frukost är exempel på faktorer som studeras. Tidigare fanns det i Sverige rekommendationer om att äta tre huvudmåltider och ett till två mellanmål (1). Dessa rekommendationer baserades dock främst på praktisk erfarenhet snarare än vetenskaplig evidens och har därför tagits bort. Både i Norden och i USA har sambandet mellan måltidsmönster och hälsa kartlagts i arbetet med officiella kostråd, men evidensen saknades för kunna ge råd om måltidsmönster (2, 3). Idag finns därför inga råd i Sverige om måltidsmönster för den generella befolkningen. Måltidsmönster varierar mellan individer, men också mellan länder och kulturer, där måltidernas storlek och tidsmässiga fördelning över dygnet varierar stort (4–7).
Kroppens förmåga att hantera mat varierar vid olika tider på dygnet, eftersom biologiska processer följer de cirkadiska rytmerna (8, 9). Cirkadiska rytmer är kroppens inre biologiska klocksystem, som styr återkommande processer med en cykel på cirka 24 timmar. Dessa rytmer spelar en central roll i regleringen av olika fysiologiska funktioner, såsom kroppstemperatur, blodtryck, aptit, matsmältning och ämnesomsättning. Det är troligen fördelaktigt för den metabola hälsan att äta synkroniserat med de cirkadiska rytmerna. Exempelvis har kroppen sämre glukostolerans på kvällen jämfört med på morgonen (10). Det finns även samband mellan skiftarbete och en högre risk för metabola syndromet, sannolikt på grund av att dessa personer bland annat äter osynkroniserat med kroppens rytmer (11, 12). Vid metabola syndromet samverkar obesitas, förhöjda blodfetter, högt blodtryck och insulinresistens, vilka tillsammans ökar risken för hjärt-kärlsjukdomar, typ 2-diabetes och andra hälsoproblem.
Forskningen har också funnit samband mellan tidsmässiga måltidsmönster och hälsa, men resultaten är inte entydiga. Det finns mycket begränsat med interventionsstudier inom området, vilka är nödvändiga för att kunna dra slutsatser om rekommendationer för befolkningen. Att äta frukost har i både observations- och interventionsstudier visat sig vara viktigt och skyddande för den kardiometabola hälsan, som i sin tur påverkar risken för hjärt-kärlsjukdom och typ 2-diabetes (13). Att äta sent på dygnet verkar däremot vara negativt för hälsan (13). En stor fransk studie visade att intag av dagens första måltid efter klockan 9 eller den sista efter klockan 21 var kopplat till en ökad risk för hjärt-kärlsjukdom (14). Undersökningar om antalet måltider per dag och effekter på hälsan har visat blandade resultat i relation till obesitas, men när det gäller metabol hälsa såsom risk för hjärt-kärlsjukdom eller typ 2-diabetes verkar fler måltider (>4 per dag) vara mer fördelaktigt än få måltider (<3 per dag) (13).
Måltidsmönster i Sverige
I en nyligen publicerad artikel undersöktes tidsmässiga måltidsmönster hos ungdomar och vuxna i Sverige, baserat på data från Livsmedelsverkets nationella matvaneundersökningar Riksmaten vuxna 2010-11 och Riksmaten ungdom 2016-17 (15).
I studien rapporterade deltagarna sitt matintag via webben under tre till fyra dagar. Deltagarna svarade även på enkäter om sina matvanor och bakgrundsfaktorer. Ungdomarnas längd och vikt mättes, och viss bakgrundsinformation om de vuxna hämtades från register. Studien visar att svenskar i genomsnitt äter 4 till 5 måltider per dag. Ungdomar åt i snitt 4,2 måltider per dag, och vuxna 4,6 måltider per dag. Kvinnor åt generellt fler måltider än män, både bland ungdomar och vuxna, och antal måltider ökade med åldern hos vuxna. Ungdomar med föräldrar som har en längre utbildning åt också fler måltider (4,2 måltider) jämfört med ungdomar vars föräldrar har en kortare utbildning (3,7 måltider).
Endast 9 procent av de vuxna åt inte frukost varje dag, medan andelen bland ungdomar var 17 procent. Det var betydligt vanligare att skippa frukost bland ungdomar som hade föräldrar med en kortare utbildning (34 %).
Måltidsmönster i förhållande till näringsintag
Det fanns ett samband mellan antal måltider (måltidsfrekvens) och intag av energi och näringsämnen. Generellt observerades att ju fler måltider, desto högre var energiintaget, vilket innebär att personer som äter få måltider inte verkar kompensera genom att äta större måltider – och tvärtom. Fler måltider var också kopplat till ett högre intag av näringsämnen som fullkorn, fibrer, vitamin D, järn och folat – men även fritt socker och mättat fett. Dessutom undersöktes näringsintaget i förhållande till genomsnittsbehovet (Average Requirement, AR) eller det rekommenderade intaget (Recommended Intake, RI) i de nordiska näringsrekommendationerna, NNR 2023, för att undersöka hur väl individer med olika rapporterade måltidsfrekvenser uppfyllde näringsbehovet. Resultatet visade att de som rapporterade färre än tre måltider per dag hade svårt att nå upp till behovet av ett antal viktiga näringsämnen, såsom folat, järn, vitamin D och fibrer.
När det gäller betydelsen av att äta frukost visade studien att personer som inte åt frukost hade ett lägre energiintag och åt färre måltider. Det tyder på att man inte verkar ta igen den missade energin från frukosten senare under dagen. Personer som inte åt frukost hade även ett lägre intag av exempelvis fullkorn, fibrer, vitamin D, järn och folat – även när man justerade för ett lägre energiintag. Dessutom hade de ett högre intag av fritt socker, vilket tyder på att personer som inte äter frukost har en sämre kostkvalitet.
Sammantaget visade studien att det finns skillnader i måltidsmönster inom befolkningen, både bland vuxna och ungdomar. Det finns även tydliga samband mellan måltidsfrekvens och näringsintag – det verkar vara fördelaktigt att äta fler måltider per dag och att äta frukost. Samtidigt behövs mer forskning inom området för att kunna dra säkrare slutsatser om hur måltidsmönster påverkar hälsan och för att kunna ge rekommendationer till befolkningen.
Författaren uppger inga jävsförhållanden.
Referenser
1. Livsmedelsverket. Svenska näringsrekommendationer 2005. Rekommendationer om näring och fysisk aktivitet. Fjärde upplagan. Uppsala Livsmedelsverket; 2005.
2. Svendsen M, Bertéus Forslund H. Meal patterns, including intermittent fasting – a scoping review for Nordic Nutrition Recommendations 2023. fnr (Internet). 2024 (cited 2024 Mar 12);68. Available from: https://foodandnutritionresearch.net/index.php/fnr/article/view/10505
3. Palacios C, Andres A, Odoms-Young A, Stanford FC, Anderson CAM, Fisher JO, et al. Frequency of Meals and/or Snacking and Consuming a Dietary Pattern Aligned with the Dietary Guidelines for Americans: A Systematic Review (Internet). Alexandria (VA): USDA Nutrition Evidence Systematic Review; 2024 (cited 2025 Feb 20). Available from: http://www.ncbi.nlm.nih.gov/books/NBK610625/
4. Huseinovic E, Winkvist A, Slimani N, Park MK, Freisling H, Boeing H, et al. Meal patterns across ten European countries – results from the European Prospective Investigation into Cancer and Nutrition (EPIC) calibration study. Public Health Nutr. 20160519th ed. 2016;19:2769–80.
5. Park MK, Freisling H, Huseinovic E, Winkvist A, Huybrechts I, Crispim SP, et al. Comparison of meal patterns across five European countries using standardized 24-h recall (GloboDiet) data from the EFCOVAL project. Eur J Nutr. 20170308th ed. 2018;57:1045–57.
6. Fjellström C. Mealtime and meal patterns from a cultural perspective. Scandinavian Journal of Nutrition. 2004;48:161–4.
7. Kant AK, Graubard BI. 40-year trends in meal and snack eating behaviors of American adults. J Acad Nutr Diet. 2015;115:50–63.
8. Flanagan A, Bechtold DA, Pot GK, Johnston JD. Chrono-nutrition: From molecular and neuronal mechanisms to human epidemiology and timed feeding patterns. J Neurochem. 20201210th ed. 2021;157:53–72.
9. West AC, Bechtold DA. The cost of circadian desynchrony: Evidence, insights and open questions. Bioessays. 20150522nd ed. 2015;37:777–88.
10. Morris CJ, Yang JN, Garcia JI, Myers S, Bozzi I, Wang W, et al. Endogenous circadian system and circadian misalignment impact glucose tolerance via separate mechanisms in humans. Proceedings of the National Academy of Sciences. 2015;112:E2225–34.
11. Sooriyaarachchi P, Jayawardena R, Pavey T, King NA. Shift work and the risk for metabolic syndrome among healthcare workers: A systematic review and meta-analysis. Obes Rev. 2022;23:e13489.
12. Schettini MAS, Passos RF do N, Koike BDV. Shift Work and Metabolic Syndrome Updates: A Systematic Review. Sleep Sci. 2023;16:237–47.
13. St-Onge MP, Ard J, Baskin ML, Chiuve SE, Johnson HM, Kris-Etherton P, et al. Meal Timing and Frequency: Implications for Cardiovascular Disease Prevention: A Scientific Statement From the American Heart Association. Circulation. 20170130th ed. 2017;135:e96–121.
14. Palomar-Cros A, Andreeva VA, Fezeu LK, Julia C, Bellicha A, Kesse-Guyot E, et al. Dietary circadian rhythms and cardiovascular disease risk in the prospective NutriNet-Santé cohort. Nature Communications. 2023;14:7899.
15. Schultz J, Moraeus L, Lindroos AK, Lemming EW. Temporal meal patterns in the Swedish population and associations with sociodemographic variables and nutrient intakes: a cross-sectional study. British Journal of Nutrition. 2025;1–30.
Mycket fiber och lite gluten – ett skydd mot celiaki?
De senaste årens forskning har breddat synen på tidig prevention av celiaki, från att enbart fokusera på amning och när gluten ska introduceras, till att omfatta hela kosten. Celiaki kallas även för glutenintolerans, och gluten är ett växtprotein som finns i olika sädesslag (vete, råg och korn). Varför bara en del barn med genetiska förutsättningar utvecklar celiaki, och varför de flesta insjuknar före tio års ålder, är fortfarande oklart. Forskning från den stora prospektiva studien TEDDY visar att ett lägre intag av fiber och ett högre intag av gluten samt ett västerländskt kostmönster under de första levnadsåren verkar bidra till att den kroniska sjukdomen utvecklas. Fynden har lagt grunden till två pågående kostinterventionsstudier i Skåne, som ska fastslå om det finns ett orsakssamband.
>>text: Elin Hård af Segerstad, med dr, dietist specialiserad i pediatrik, Enheten för celiaki och diabetes, Kliniska vetenskaper Malmö, Lunds universitet, Malmö
Tidigare kostråd som syftade till att minska risken för celiaki hos barn rekommenderade att gluten skulle introduceras till bebisar under skydd av amning, mellan 4–6 månaders ålder, och i långsamt ökande mängder. Men under de senaste 20 åren har stora, prospektiva studier visat att varken amning, tidpunkten för glutenintroduktion under det första levnadsåret eller små mängder gluten vid introduktion påverkar barnets risk att utveckla sjukdomen (1). Dessa longitudinella studier, där barn med genetisk risk har följts under uppväxten, visar att celiaki – ett kroniskt autoimmunt tillstånd där immunsystemet reagerar mot gluten och skadar tunntarmens slemhinna – i de flesta fall utvecklas under barnets första fyra till fem levnadsår (2).
Den genetiska bakgrunden, främst HLA-typerna DQ2 och DQ8, förklarar ungefär hälften av orsaken till sjukdomen, medan faktorer i barnets levnadsmiljö bidrar med resterande 50 procent. I Sverige har dock cirka 40 procent av befolkningen någon av dessa HLA-typer, samtidigt som knappt tre procent utvecklar celiaki (3). Flera av de miljöfaktorer som tros bidra till utvecklingen av celiaki är svåra att påverka, som vanliga virusinfektioner. Sedan 80- och 90-talet då incidensen av celiaki i Sverige varierande stort i samband med förändringar i allmänna kostråd till spädbarn, har det istället funnits en hypotes om att kunna minska risken för sjukdom genom barnets mat.
TEDDY-studien
De senaste årens forskning har breddat synen på tidig celiakiprevention, från att enbart handla om tidpunkten för glutenintroduktion och amning till att omfatta flera delar av barnets kost under de första levnadsåren (2). I TEDDY-studien (The Environmental Determinants of Diabetes in the Young) har cirka 8700 barn med genetisk HLA-risk i USA, Sverige, Finland och Tyskland följts från födseln upp till 15 års ålder under två decennier (4). Under studiens gång har omfattande information samlats in om barnen, inklusive deras mat, levnadsvanor, och infektioner, vilket har möjliggjort stora framsteg i vår förståelse om hur olika miljö- och genetiska faktorer bidrar till celiakiutveckling. Något som är unikt med TEDDY-studien är att barnen regelbundet screenas för celiakiautoantikroppar, vilket gör det möjligt att fastställa när i tiden utvecklingen av celiaki påbörjats och därmed undersöka olika faktorer hos barnet innan celiaki är fullt utvecklat. Det är också möjligt att ta hänsyn till andra viktiga kända faktorer som påverkar risken för celiaki, såsom kvinnligt kön och om det finns någon i familjen som har celiaki. I TEDDY-studien har knappt 20 procent av alla barn utvecklat ett förstadium till celiaki, celiakiautoimmunitet, och knappt 8 procent har fått en celiakidiagnos.
Mer fiber verkar kunna minska risken för celiaki
I en studie från TEDDY, nyligen publicerad i tidskriften Gastroenterology, analyserade vi barnens fiberintag från sex månaders ålder till fem års ålder hos cirka 6 500 barn (5). Information om barnens kost samlades in genom upprepade 3-dagars matdagböcker vid totalt elva tillfällen. Med hjälp av en harmoniserad gemensam näringsdatabas kunde barnens totala fiberintag över tid undersökas. Barnen följdes upp tills de var minst 13 år gamla.
Barnens intag av fiber ökade under det första levnadsåret, med ett högre intag i Finland och lägre i USA, till knappt 10 gram/1000 kcal/dag från ett års ålder. WHO:s rekommendation för fiber är 15 gram/dag vid två års ålder (6). Resultaten från studien visade att ett högre intag av kostfiber fram till 3 års ålder var kopplat till en lägre risk för att senare utveckla celiaki. När vi tog hänsyn till mängden gluten barnet åt var det framför allt under det första levnadsåret som riskminskningen sågs. Barn som åt cirka 3 gram mer fiber per dag än genomsnittet under det första året hade ungefär 40 procent lägre risk att utveckla celiaki.
Vi undersökte även om det hade någon betydelse från vilken livsmedelsgrupp fibern kom, utifrån att olika typer av fiber har skilda mekanismer i tarmen. Men vi kunde visa en riskminskande effekt oavsett om fiber kom från frukt, grönsaker, spannmål eller andra källor. Mängden fiber som barnet åt senare under barndomen verkade däremot inte påverka risken för sjukdomen. Det i sig är intressant och samstämmer med tidigare forskning som visar att just fiber tidigt i livet påverkar barnet, men också att det kanske är under de första levnadsåren som det finns möjlighet att aktivt påverka barnets risk för att utveckla sjukdomen. Det är en period då barnets immunförsvar utvecklas och barnet stöter på många patogener. Celiaki är ett tillstånd där tunntarmens skyddande barriär påverkas, och det finns indikationer på att tarmflorans sammansättning kan ha betydelse för sjukdomens uppkomst (2). Särskilt tidigt i livet bidrar fiber till att tarmfloran utvecklas, tarmen mognar och det är ett stort samspel mellan tarm och immunförsvar (7).
Tillsammans med fynd om att vissa vanliga virusinfektioner, särskilt upprepade infektioner i tarmen under barndomen, ökar risken för celiaki, stärktes vår hypotes om att fiber kan utgöra en skyddande faktor (8).
Tidigare fynd från TEDDY om kostens roll i utvecklingen av celiaki
Det första stora steget mot en ny förståelse om hur kosten kan bidra till celiakiutveckling kom 2019 då TEDDY-studien visade att barn som åt mer gluten upp till 5 års ålder hade en högre risk att utveckla celiaki (9). För varje grams ökning av gluten per dag (medelintag 3,7 gram/dag) ökade risken för att senare utveckla celiaki med 50 procent. Kort därefter publicerades ytterligare studier från andra kohorter som bekräftade fynden (2).
En uppföljningsstudie på de svenska barnen i TEDDY visade dessutom att det även verkade ha betydelse från vilken typ av mat som gluten kom (10). Barn som vid ett års ålder åt mer bröd, välling och barngröt hade en högre risk för celiaki, oberoende av deras totala glutenintag. Fyndet tyder på att det inte bara är den totala mängden gluten, utan även källan till gluten, som kan ha betydelse. Dock hade andra delar av barnens kost i liten utsträckning undersökts. I TEDDY-studien undersökte vi därför vidare om kostmönster i stort kan påverka celiakirisk (11). Genom att undersöka vilka kostmönster som barnen hade såg vi att ett typiskt västerländskt kostmönster, oberoende av mängden gluten, också ökade risken för celiaki. Samtidigt fanns andra kostmönster hos barnen som istället verkade vara skyddande, vilket var i linje med tidigare forskning från en mindre nederländsk kohortstudie (12).
Detta gav ytterligare stöd för att även andra delar av kosten kan bidra till sjukdomsutvecklingen – och att vissa livsmedel istället kunde vara skyddande. En gemensam nämnare för de skyddande kostmönstren var att de var rika på grönsaker, frukt och spannmål, men innehöll mindre av fiberfattiga livsmedel som juice och vete. Att i nästa steg undersöka om fiber kunde vara en gemensam nämnare låg därför nära till hands.
Kostens roll i utvecklingen av celiaki
Hittills har forskning från TEDDY och andra stora kohortstudier bidragit till en hypotes om att flera delar av kosten tidigt i livet kan påverka barns risk för att utveckla celiaki, samtidigt som kosten i sig sannolikt inte är den utlösande faktorn (2). Istället skulle kosten kunna bidra med olika förutsättningar för tarmens förmåga att hålla patogener och gluten ute samt påverka hur immunförsvaret svarar när tarmslemhinnan utsätts för gluten.
Sammantaget visar forskningen också på flera möjliga strategier för hur kostråd på gruppnivå skulle kunna minska förekomsten av celiaki. Samtidigt är forskningen baserad på observationer, vilket inte kan bekräfta orsakssamband och än så länge är evidensen inte tillräckligt stark för att ändra kostråd, vare sig för den generella befolkningen eller för riskgruppen (13). För att med säkerhet kunna fastslå att kosten verkligen kan påverka risken för celiaki hos barn krävs randomiserade interventionsstudier.
Pågående kostinterventioner
Just nu driver vår forskargrupp två stora kostinterventioner i Skåne: ”Prevention av Celiaki i Skåne” (PreCiSe) och ”Gluten Reduction after Infancy and risk of Celiac Disease” (GraIn) (14). Syftet med studierna är att undersöka om en strikt glutenfri eller glutenreducerad kost, jämfört med en normalkost, fram till tre års ålder kan minska risken för att senare utveckla celiaki. Endast barn med genetiska förutsättningar för att utveckla celiaki bjuds in till studien, och screening har genomförts genom HLA-testning av navelsträngsblod.
Med hjälp av kostråd från dietister, regelbunden screening för celiakiautoantikroppar och att matintaget följs noga kommer vi framöver förhoppningsvis kunna slå fast om risken för celiaki verkligen kan minska när glutenintaget sänks. Trots att råden som ges inom studien i övrigt går i linje med allmänna rekommendationer för åldersgruppen, behöver också barnens näringsintag jämföras mellan de som äter mindre mängd gluten och de som fortsätter att äta normalkost. Eftersom livsmedel som innehåller gluten utgör viktiga näringskällor för barn i den här åldern måste en glutenmodifierad kost visa sig vara näringsmässigt adekvat innan allmänna kostråd kan ändras.
Författaren uppger inga jävsförhållanden.
Referenser
1. Szajewska H, Shamir R, Auricchio R, Chmielewska A, Dolinsek J, Kivela L, et al. Early diet and the risk of coeliac disease. An update 2024 position paper by the ESPGHAN special interest group on coeliac disease. J Pediatr Gastroenterol Nutr. 2024;79(2):438-45.
2. Stahl M, Koletzko S, Andren Aronsson C, Lindfors K, Liu E, Agardh D, et al. Coeliac disease: what can we learn from prospective studies about disease risk? Lancet Child Adolesc Health. 2024;8(1):63-74.
3. Naredi Scherman M, Lind A, Hamdan S, Lundgren M, Svensson J, Pociot F, et al. Home capillary sampling and screening for type 1 diabetes, celiac disease, and autoimmune thyroid disease in a Swedish general pediatric population: the TRIAD study. Front Pediatr. 2024;12:1386513.
4. Hagopian WA, Erlich H, Lernmark A, Rewers M, Ziegler AG, Simell O, et al. The Environmental Determinants of Diabetes in the Young (TEDDY): genetic criteria and international diabetes risk screening of 421 000 infants. Pediatr Diabetes. 2011;12(8):733-43.
5. Hård af Segerstad EM, Mramba LK, Aronsson CA, Uusitalo U, Virtanen SM, Agardh D, et al. Early Dietary Fiber Intake Reduces Celiac Disease Risk in Genetically Prone Children: Insights From the TEDDY Study. Gastroenterology. 2025.
6. World Health Organization. Carbohydrate intake for adults and children: WHO guideline summary: Geneva: World Health Organization; 2023. Available from: https://iris.who.int/handle/10665/374925.
7. Cai Y, Folkerts J, Folkerts G, Maurer M, Braber S. Microbiota-dependent and -independent effects of dietary fibre on human health. Br J Pharmacol. 2020;177(6):1363-81.
8. Galipeau HJ, Hinterleitner R, Leonard MM, Caminero A. Non-Host Factors Influencing Onset and Severity of Celiac Disease. Gastroenterology. 2024;167(1):34-50.
9. Andren Aronsson C, Lee HS, Hard Af Segerstad EM, Uusitalo U, Yang J, Koletzko S, et al. Association of Gluten Intake During the First 5 Years of Life With Incidence of Celiac Disease Autoimmunity and Celiac Disease Among Children at Increased Risk. JAMA. 2019;322(6):514-23.
10. Hård af Segerstad EM, Liu X, Uusitalo U, Agardh D, Andrén Aronsson C. Sources of dietary gluten in the first 2 years of life and associations with celiac disease autoimmunity and celiac disease in Swedish genetically predisposed children: The Environmental Determinants of Diabetes in the Young (TEDDY) study. Am J Clin Nutr. 2022;116(2):394-403.
11. Hård Af Segerstad EM, Mramba LK, Liu X, Uusitalo U, Yang J, Norris J, et al. Associations of dietary patterns between age 9 and 24 months with risk of celiac disease autoimmunity and celiac disease among children at increased risk. Am J Clin Nutr. 2023;118(6):1099-105.
12. Barroso M, Beth SA, Voortman T, Jaddoe VWV, van Zelm MC, Moll HA, et al. Dietary Patterns After the Weaning and Lactation Period Are Associated With Celiac Disease Autoimmunity in Children. Gastroenterology. 2018;154(8):2087-96 e7.
13. Szajewska H, Shamir R, Auricchio R, Chmielewska A, Dolinsek J, Kivelä L, et al. Early diet and the risk of coeliac disease. An update 2024 position paper by the ESPGHAN special interest group on coeliac disease. J Pediatr Gastroenterol Nutr. 2024;79(2):438-45.
14. Andren Aronsson C, Agardh D. Intervention strategies in early childhood to prevent celiac disease-a mini-review. Front Immunol. 2023;14:1106564.
Samband mellan lågt fiberinnehåll i kosten och mer skadligt plack i hjärtats kranskärl
Notis
Det finns samband mellan kostmönster och både förekomst och typ av plack i kranskärlen. Det visar resultat från den nationella SCAPIS-studien som omfattar drygt 24 000 personer i åldern 50-64 år.
Sambandet mellan kost och hjärthälsa analyserades med ett kostindex som ger höga poäng för hälsosamma livsmedel och låga poäng för ohälsosamma. Därefter undersöktes deltagarnas hjärtan med datortomografi för att upptäcka tidiga tecken på fettinlagringar, åderförfettning, i hjärtats blodkärl. Deltagarna i studien hade inga symtom på hjärtproblem eller diagnostiserad hjärtsjukdom vid studiestart.
Resultat från studien visar att en kost med mer grönsaker, frukt, fullkorn, fiberrika livsmedel, nötter, magra mejeriprodukter, raps- och olivolja och mindre av rött kött, chark, chips och liknande snacks samt sockrade drycker, var kopplade till färre högriskplack. Instabila högriskplack i hjärtats kranskärl kan bidra till bildning av blodproppar och leda till hjärtinfarkt.
Här kan du läsa om studien och SCAPIS via nyheter från Göteborgs universitet: Samband mellan fiberfattig kost och farligare plack i kranskärlen | Göteborgs universitet
Länk till artikel som publicerades den 16 juni 2025 i tidskriften Cardiovascular Research: Low-fibre diet is associated with high-risk coronary plaque features
Ökad järnbrist hos tonårsflickor – en nödvändig konsekvens av klimatvänliga matvanor?
Behovet av järn för tonårsflickor beräknas med en faktoriell metod, vilket innebär att alla komponenter som påverkar järnbehovet adderas: behov för tillväxt, ersättning av basala förluster samt järnförluster som förloras med menstruationsblod. Det sammanlagda behovet justeras därefter för järnets biotillgänglighet för att fastställa det rekommenderade dagliga intaget. Nordiska näringsrekommendationer baseras på 15 procents biotillgänglighet för järn, vilket förutsätter en blandkost. I artikeln visas hur rekommenderat intag av järn för flickor i åldrarna 11-14 år och 15-17 år beräknas.
Järnbrist är vanlig hos tonårsflickor och drabbar nästan var tredje flicka. Detta gäller i större utsträckning för flickor som äter klimatvänligt eller vegetariskt. Även skolmåltider är otillräckliga – både gällande totalt järnintag och biotillgänglighet av järn. Men ökad järnbrist hos tonårsflickor är inte en nödvändig konsekvens av klimatvänliga matvanor. Detta ställer dock krav både på ökad mängd totaljärn och ökad biotillgänglighet. Flickor som äter klimatanpassat eller vegetariskt kan behöva ett högre intag av totaljärn än 15 mg per dag.
>>text: Agneta Sjöberg, seniorprofessor, och Mari Wollmar, filosofie doktor, Institutionen för kost- och idrottsvetenskap, Göteborgs universitet, Göteborg; Magnus Domellöf, professor, Institutionen för klinisk vetenskap, Umeå universitet, Umeå
Järnbrist – definition, förekomst och konsekvenser
Det finns två former av järnbrist: järnbrist och järnbristanemi. Järnbrist (iron deficiency, ID) innebär låga eller tomma järndepåer och definieras som serumferritin <15 µg/L (1). Järnbristanemi (iron deficiency anemia, IDA) definieras som hemoglobin, Hb, <120 g/L i kombination med lågt serumferritin (1). Det är välkänt att individer som växer mycket, och att tonårsflickor och kvinnor som har menstruation, har extra stora järnbehov. Järnbrist är ett av de vanligaste bristtillstånden globalt. Nästan en tredjedel av kvinnor i fertil ålder och tonårsflickor i Sverige bedöms ha järnbrist (2–4). En hälsosam järnstatus är väsentligt både för mental och fysisk arbetsförmåga.
Tonårsflickors järnbehov och rekommendationer
Järnbehovet beräknas med en så kallad faktoriell metod, som för tonårsflickor inkluderar att täcka järnbehovet för tillväxt, basala förluster samt järnförluster vid menstruation (1, tabell 4 i referensen). I denna artikel fokuserar vi på flickor i åldrarna 11-14 år och 15-17 år, eftersom de är en sårbar grupp med både behov för tillväxt och för att täcka järnförluster vid menstruation. I tabell 1a visas järnrekommendationer och järnbehov i de nordiska näringsrekommendationerna 2023 (NNR 2023) och från tidigare versioner av NNR, och i tabell 1b visas detaljerade siffror.
Medelbehovet av järn för tillväxt är 0,32 mg/dag baserat på hela perioden 11-18 år. Flickors tillväxt är som störst i åldern 11-14 år, då järnbehovet för tillväxt uppgår till 0,46 mg/dag, medan det vid 15-17 års ålder sjunker till 0,18 mg/dag (1). Dessa siffror baseras på innehållet av totalt kroppsjärn, som enligt Europeiska myndigheten för livsmedelssäkerhet, Efsa, är 40 mg/kg för 11-åringar och 38 mg/kg för flickor i åldern12-17 år (5). Totalt kroppsjärn multipliceras med tillväxten i kg/år (1) och divideras med årets dagar för att få fram behovet i mg/dag.
Basala förluster av järn beräknas vara 12 µg/kg/dag för barn äldre än 5 år, enligt Efsa (5). Detta resulterar i 0,56 mg/dag för flickor i åldern 11-14 år och 0,69 mg/dag för flickor 15-17 år, för att täcka basala förluster av järn (1).
Den sista komponenten i den faktoriella metoden är att täcka järnförluster vid menstruation. Dessa förluster är snedfördelade och en del av flickor har mycket stora förluster på grund av stora blödningar. Därför används median och den 95:e percentilen för beräkning av järnbehovet. Medianen för järnförluster vid menstruationsblödningar beräknas till 0,45 mg/dag baserat på Hallberg, Harvey och Efsa, Appendix A (5–7). För den 95:e percentilen används 1,32 mg/dag (5, 7). Flickor i Sverige får sin första menstruation ungefär vi 13 års ålder (8), därför ingår endast hälften av flickorna i åldern 11-14 år vid beräkning av den 95:e percentilen. Flickor som börjat menstruera har dock det högre behovet.
Det sammanlagda behovet av järn – för tillväxt, basala förluster och järnförluster vid menstruation – uppgår för medianflickan till 1,47 mg/dag i åldern 11-14 år och1,32 mg/dag i åldern 15-17 år. För den 95:e percentilen, det vill säga för att täcka behovet hos 95 % av alla flickor, är motsvarande siffror 1,90 mg/dag respektive 2,19 mg/dag (1).
För att beräkna det rekommenderade intaget måste även hänsyn tas till järnets biotillgänglighet, eftersom endast en del av järnet som finns i maten kan absorberas. Här räknar man med en biotillgänglighet på 15 %. Detta resulterar i ett medelbehov (average iron requirement) på 9,8 mg/dag för flickor i åldern 11-14 år och 8,8 mg/dag för flickor 15-17 år. För den 95:e percentilen är motsvarande siffror 12,7 mg/dag respektive 14,6 mg/dag, och dessa ligger till grund för de rekommenderade intagen: 13 mg/dag för flickor 11-14 år och 15 mg/dag för flickor 15-17 år (9).
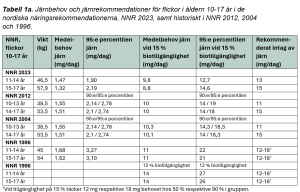
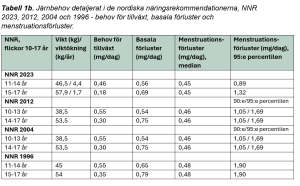
Biotillgänglighet
Det rekommenderade dagliga intaget av järn i NNR 2023 beräknas för att täcka behovet hos 95 % av populationen med koster som har 15 % biotillgänglighet – det vill säga att 15 % av järnet i maten kan absorberas.
Absorptionen av järn från kosten är generellt låg, är välreglerad och styrs i hög utsträckning av individens järnstatus. Detta innebär att individer med höga järndepåer absorberar procentuellt mindre av måltidens järn än individer med låga eller tomma järndepåer. Denna reglering är dock inte tillräcklig om järninnehållet i kosten är lågt eller om måltiden innehåller en hög förekomst av faktorer som hämmar järnabsorptionen. Järnabsorptionen brukar anges variera mellan 5 och 25 %, och ibland nämns en tiofaldig variation beroende på kostens biotillgänglighet. Kostfaktorers hämmande eller främjande effekter sker i huvudsak på måltidsnivå.
Det förekommer olika former av järn i kosten; hemjärn och icke-hemjärn (non-hemjärn), varav hemjärn endast finns i kött, fisk och skaldjur samt i blodprodukter. Icke-hemjärn finns i alla typer av livsmedel utom mjölkprodukter och matfett. Berikningsjärn utgörs av olika former av icke-hemjärn. Hemjärn absorberas i högre grad, medan absorptionen av icke-hemjärn i större utsträckning påverkas av måltidens innehåll av främjande och hämmande faktorer. Vitamin C och den så kallade köttfaktorn, det vill säga kött-, fisk-, fågel- eller skaldjurskött, främjar absorptionen medan fytinsyra, polyfenoler, sojaprotein och kalcium hämmar järnabsorptionen (10). Mjölksyrefermentering av grönsaker leder till ökad absorption genom att göra mer trevärt järn (Fe3+) tillgängligt för absorption (11).
Vitamin C är en viktig främjare av järnabsorptionen som reducerar järnet från trevärt (Fe3+) till tvåvärt (Fe2+), vilket är den form som absorberas i tarmcellen.
En viktig hämmande faktor är fytinsyra som finns i högre halter i fullkornsspannmål, baljväxter, nötter och frön. Fytinsyran komplexbinder järnet som då blir svårare att absorbera. Jäsning och fermentering kan delvis göra järnet tillgängligt liksom vitamin C och köttfaktorn i måltiden. Även kalcium har hämmande effekt, troligen genom att kalcium och järn konkurrerar om absorptionen.
Sojabönor har hög halt av fytinsyra och i sojaprotein/isolat är halten ännu högre. Utöver fytinsyran verkar sojaproteinet ha en ytterligare hämmande effekt på järnabsorptionen (10).
Absorberbart järn har beräknats med en algoritm som väger in hemjärn och icke-hemjärn samt hämmande och främjande faktorer i måltiden (10). I en studie analyserades alla måltider under en vecka hos 28 femtonåriga flickor (12). Resultaten visade att det totala järnintaget i genomsnitt var 11,5 mg/dag, och hos 85 % av flickorna i studien var intaget under 15 mg/dag. Tio av flickorna (36 %) hade järnbrist varav två hade anemi. Absorberbart järn uppgick till 1,09 mg/dag medan individuellt beräknat järnbehov var 1,60 mg/dag.
Klimatvänliga koster och deras påverkan på järnets biotillgänglighet
Att äta klimatvänligt eller vegetariskt innebär för en tonårsflicka en ökad risk för järnbrist. Detta visas i två artiklar som presenterar data för tonårsflickor i Sverige. Den ena artikeln baseras på Riksmaten ungdom, som genomfördes under 2016 och 2017, och visar att 10 %, 30 % respektive 26 % av flickorna i årskurs 5, årskurs 8, och första året i gymnasiet hade järnbrist (3). Flickor som åt en kost med lägst klimatpåverkan hade mer än dubbelt så hög risk för järnbrist jämfört med dem som åt en kost med högst klimatpåverkan. Bland pojkar i årskurs 8 respektive första året i gymnasiet hade 11 % respektive 2 % järnbrist, och det fanns inga samband med kostens klimatpåverkan (3).
I den andra, nyligen publicerade artikeln, hade 38 % av 475 gymnasieflickor järnbrist (13). I studien rapporterade flickorna sitt kostintag via en enkät, och om de åt blandkost, uteslöt rött kött, var pescetarianer (åt vegetariskt samt fisk och skaldjur) eller var vegetarianer/veganer. Nästan 70 % av flickorna som åt vegetariskt eller vegankost hade järnbrist. För järnbristanemi fanns dock inga skillnader beroende på vilken typ av kost deltagarna åt, utan för samtliga grupper låg förekomsten runt 3 %.
Fynden i dessa två studier är inte oväntade och förklaras av tonårsflickors höga järnbehov, att rekommenderat intag i NNR 2023 (9) förutsätter 15 % biotillgänglighet, vilket i princip betyder blandkost, samt att kostintaget ofta inte når rekommenderat intag.
Skolmåltider, järninnehåll och absorberbart järn
Skolmåltider är viktiga i kommuners klimatarbete. Resultat från en studie visade att av 1465 menydagar från 76 kommuner innehöll mer än hälften kött, 54 %, varav 15 % fågelrätter och resten innehöll rött eller processat kött (14). Fisk respektive vegetariska måltider serverades en dag per vecka. I storstadsområdena var 29 % av menydagarna vegetariska och 48 % köttbaserade (14).
Enligt Livsmedelsverket bör en skollunch ge 30 % av rekommenderat energi- och näringsintag (15). För en tonårsflicka blir då rekommenderat järnintag 4,5 mg/lunch och om vi applicerar 30 % även på det beräknade järnbehovet, motsvarar detta 0,44 mg för att täcka medianflickans behov och 0,66 mg för att täcka 95 % av flickornas behov (1, 15).
När kompletta skolluncher beräknades för totaljärn och absorberbart järn (10) fann man att sojabaserade luncher nådde 4,5 mg men dessa hade det lägsta beräknade absorberbara järnet, 0,15 mg (14). Luncher med nötkött innehöll 4,1 mg totaljärn och 0,57 mg absorberbart järn (14). I tabell 2 visas totaljärn och beräknat absorberbart järn för olika rätter, totaljärn varierar mellan 2,3 mg (fisk) och 4,5 mg (sojafärs), och absorberbart järn mellan 0,15 och 0,57 mg. Ingen av luncherna innehöll absorberbart järn för att täcka behovet hos 95 % av flickorna (14).
Det är ett allvarligt problem att skolmåltiderna som beräknades inte nådde rekommenderat intag för totaljärn. Då även biotillgängligheten av järn i de beräknade skolmåltiderna var under 15 % leder det till att skolmåltiderna i ännu lägre utsträckning kan täcka järnbehovet hos flickor med det största behovet.
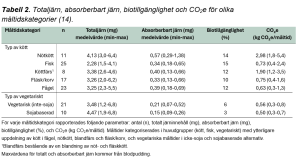
Praktiska lösningar för att förbättra järnnutrition och klimatpåverkan
Vegetariska måltider uppvisade en biotillgänglighet på 6 %, och endast 3 % för måltider med köttsubstitut av soja, se tabell 2 (14). Detta kan förklara den höga förekomsten av järnbrist hos flickor som åt vegetariskt/veganskt jämfört med de som åt blandkost i studien med gymnasieflickor (13). Men järnbehovet styr och även flickor som äter blandkost eller kost med hög klimatpåverkan hade järnbrist (3, 13). Ett första steg kan vara att erbjuda skolluncher som når rekommenderat intag av totaljärn och att tillföra måltidskomponenter som främjar järnabsorptionen.
Ett annat sätt är att arbeta med hybridrätter, så kallade 50/50, då man sänker måltidens klimatpåverkan genom att ersätta köttet delvis med växtbaserade livsmedel (16). Andra framtida möjligheter att förbättra järnsituationen är växtbaserade livsmedel där järnets absorberbarhet ökar genom nedbrytning av fytinsyrakomplex, exempelvis via hydrotermisk behandling, fermentering osv. Men denna produktutveckling tar tid för att upparbeta jämn kvalitet samt för att skala upp produktionen. Kommuners upphandling kan öka efterfrågan genom att ställa kvalitetskrav på köttsubstitut och andra växtbaserade livsmedel. Köttsubstitut är populära bland konsumenter, används mycket i skolmåltider (17, 18) och har visats ha låg biotillgänglighet av järn (19).
Historiskt perspektiv på järnrekommendationer för tonårsflickor
I tabell 1a och 1b visas siffror för järnbehov och järnrekommendationer från tidigare årgångar av de nordiska näringsrekommendationerna (20-22). Det är tydligt att värdena i NNR 2023 är lägre än i de föregående versionerna av NNR. Behov för tillväxt saknar referens i NNR 2004 och NNR 2012, men det verkar som att samma bakgrundsdata används som i NNR 1996 (23). Tidigare baserades de basala järnförlusterna på 0,14 µg/kg/dag (24), medan NNR 2023 använder 0,12 µg/kg/dag (5). Även beräkningen av menstruationsförluster skiljer sig, och i NNR 1996 användes data från 1960-talet som angav en järnförlust på 0,48 mg/dag för mediankvinnan och 1,35 mg/dag för den 90:e percentilen (6). I NNR 2004 och NNR 2012 användes istället 0,46 mg/dag som medianvärde (25).
Den faktoriella beräkningen av järnbehov och rekommenderat intag i NNR 2023 som bygger på aktuell litteratur har lägre beräknade 95:e percentiler än föregångarna (1, 20-22). Rekommenderat intag blir ändå detsamma, 15 mg/dag. I NNR 2023 baseras rekommenderat intag på den 95:e percentilen medan man tidigare lutat sig mot den 90:e percentilen och hävdat att högre järnbehov är svåra att täcka med kosten. Vid bedömning av kostintag från kostundersökningar används medelbehovet för att värdera intaget mot och dessa siffror är lägre, 9-14 mg/dag (1, 20-22). Däremot används rekommenderat intag vid planering av måltider, vilket även Livsmedelsverket gör i sina riktlinjer för skolmåltider (15).
Övriga faktorer som påverkar järnbehovet
Referensen som använts för den 95:e percentilen av menstruationsförluster i NNR 2023 (5, 7) baseras på data från kvinnor i åldern 18-45 år. I studien använde 35,5% p-piller (7). Användning av hormonella preventivmedel är associerat med mindre menstruation vilket kan förklara lägre beräknade järnförluster för den 95:e percentilen i NNR 2023 jämfört med tidigare versioner. En sammanställning baserad på Läkemedelsregistret visar att användningen av hormonella preventivmedel i Sverige under perioden 2008-2015 var endast 1-2 % för flickor i åldern 13-14 år, 29-30 % för flickor 15-17 år och 54-56 % för flickor 18-19 år (26). Med detta drar vi slutsatsen att nuvarande järnrekommendation och faktoriella beräkningar för tonårsflickor sannolikt inte är överskattade.
En ytterligare aspekt är att idrottare, särskilt kvinnliga uthållighetsidrottare, ofta har högre risk för järnbrist än mindre aktiva personer. Detta beror på att fysisk aktivitet ökar järnbehovet eftersom kroppen förlorar järn genom svett och man kan få mikroskador i musklerna som kräver järn för reparation (27).
Screening med blodprov
För de cirka 5 % av tonårsflickorna som har rikliga menstruationer (>80 ml/cykel), är det i princip omöjligt att täcka järnbehovet med kosten. Det rekommenderas därför att skolflickor screenas med blodprov (hemoglobin och ferritin) och att järntillskott ges till dem som har järnbrist.
Slutsats
Järnbrist drabbar nästan var tredje tonårsflicka och ännu större andel av flickor som äter klimatvänligt eller vegetariskt. Flickor som äter klimatanpassat eller vegetariskt kan behöva ett högre intag av totaljärn än 15 mg per dag, se figur 1. Nordiska näringsrekommendationer baseras på 15 % biotillgänglighet vilket förutsätter blandkost.
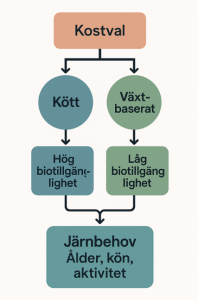
Figur 1. Figuren visar hur kostval påverkar järnbehovet genom järnets biotillgänglighet. I blandkost som innehåller kött – även fågel eller fisk – finns hemjärn med hög biotillgänglighet samt den så kallade köttfaktorn som ökar absorptionen av järn. Växtbaserad kost innehåller enbart icke-hemjärn som har lägre biotillgänglighet. Slutligen påverkas det individuella järnbehovet av faktorer som ålder, kön och fysisk aktivitetsnivå.
Agneta Sjöberg och Mari Wollmar – inga jävsförhållanden. Magnus Domellöf har fått arvode eller föreläsararvode från Baxter Medical AB, Fresenius Kabi Deutschland GmbH och Intertek Health Sciences Inc. samt medel från Arla Foods Ingrediens till Norrlands Universitetssjukhus, Umeå, för forskningsstudie.
Referenser
1. Domellöf M, Sjöberg A. Iron – a background article for the Nordic Nutrition Recommendations 2023. Food & Nutrition Research. 2024;68:10451.
2. Becker W, Lindroos AK, Nälsén C, Warensjö Lemming E, Öhrvik V. Dietary habits, nutrient intake and biomarkers for folate, vitamin D, iodine and iron status among women of childbearing age in Sweden. Upsala journal of medical sciences. 2016;121(4):271–5.
3. Hallström E, Edwall Löfvenborg J, Moreaus L, Sjöberg A, Winkvist A, Lindroos AK. Iron intake and iron status of Swedish adolescents with diets of varying climate impact. European Journal of Nutrition. 2025;64:93(2):1–13.
4. Sjöberg A, Hulthén L. Comparison of food habits, iron intake and iron status in adolescents before and after the withdrawal of the general iron fortification in Sweden. European Journal of Clinical Nutrition. 2015;69(4):494–500.
5. EFSA NDA Panel. Scientific opinion on dietary reference values for iron. EFSA panel on dietetic products, nutrition and allergies (NDA). EFSA Journal. 2015;13(10):4254.
6. Hallberg L, Högdahl AM, Nilsson L, Rybo G. Menstrual Blood Loss–A Population Study: Variation at different ages and attempts to define normality. Acta Obstetrica et Gynecologica Scandinavica. 1966;45:320–51.
7. Harvey LJ, Armah CN, Dainty JR, Foxall RJ, Lewis DJ, Langford NJ, m.fl. Impact of menstrual blood loss and diet on iron deficiency among women in the UK. British Journal of Nutrition. 2005;94:557–64.
8. Gårdstedt-Berghog J, Niklasson A, Sjöberg A, Aronsson A, Pivodic A, Nierop A, m.fl. Timing of menarche and pubertal growth patterns using the QEPS growth model. Frontiers in Pediatrics. 2024;12:1438042.
9. Blomhoff R, Andersen R, Arnesen EK, Christensen JJ, Eneroth H, Erkkola M, m.fl. Nordic Nutrition Recommendations 2023. Copenhagen: Nordic Council of Ministers; 2023.
10. Hallberg L, Hulthén L. Prediction of dietary iron absorption: an algorithm for calculating absorption and bioavailability of dietary iron. The American Journal of Clinical Nutrition. 2000;71(5):1147–60.
11. Scheers N, Rossander-Hulthen L, Torsdottir I, Sandberg AS. Increased iron bioavailability from lactic-fermented vegetables is likely an effect of promoting the formation of ferric iron (Fe3+). Eur J Nutr. 2016;55(1):373–82.
12. Hoppe M, Sjöberg A, Hallberg L, Hulthén L. Iron status in Swedish teenage girls: impact of low dietary iron bioavailability. Nutrition. 2008;24(7):638–45.
13. Stubbendorff A, Borgström Bolmsjö B, Bejersten T, Warensjö Lemming E, Calling S, Wolff M. Iron insight: exploring dietary patterns and iron deficiency among teenage girls in Sweden. Eur J Nutr. 2025;64:107.
14. Wollmar M. Opportunities and challenges with the shift to climate-adapted food consumption: Balancing nutrition, climate impact, and acceptance in public and private meals. Doktorsavhandling Göteborg, Sverige: Göteborgs universitet; Gothenburg Studies in Educational Sciences; vol. 2025. Tillgänglig vid: https://gupea.ub.gu.se/handle/2077/86222
15. Livsmedelsverket. Nationella riktlinjer för måltider i skolan. Förskoleklass, grundskola, gymnasieskola och fritidshem. 2019. Tillgänglig vid: https://www.livsmedelsverket.se/globalassets/publikationsdatabas/broschyrer-foldrar/riktlinjer-for-maltider-i-skolan.pdf
16. Wollmar M, Post A, Elf M, Pettersson J, Prim M, Sjöberg A. Balancing trade-offs — iron bioavailability, carbon footprint, and taste in hybrid school meal recipes. 18 maj 2025, manuskript inskickat efter Minor Revision.
17. Bryngelsson S, Moshtaghian H, Bianchi M, Hallström E. Nutritional assessment of plant-based meat analogues on the Swedish market. International journal of food sciences and nutrition. 2022;73(7):889–901.
18. Pettersson J, Post A, Elf M, Wollmar M, Sjöberg A. Meat substitutes in Swedish school meals: nutritional quality, ingredients, and insights from meal planners. International Journal of Food Science and Nutrition. 2024;75(7):637–49.
19. Mayer-Labba IC, Steinhausen H, Almius L, Bach Knudsen KE, Sandberg AS. Nutritional Composition and Estimated Iron and Zinc Bioavailability of Meat Substitutes Available on the Swedish Market. Nutrients. 2022;14(19):3903.
20. Nordiska Ministerrådet. Nordiska näringsrekommendationer 1996. Köpenhamn: Nordiska Ministerrådet; 1996 s. 229. (Nord). Report No.: 1996:28.
21. Nordic Council of Ministers. Nordic Nutrition Recommendations 2004. Integrating nutrition and physical activity [Internet]. Copenhagen, Denmark: Nordic Council of Ministers; 2004 [citerad 14 april 2025] s. 435. (Nord). Report No.: Nord 2004:13. Tillgänglig vid: https://www.norden.org/en/publication/nordic-nutrition-recommendations-2004
22. Nordic Council of Ministers. Nordic Nutrition Recommendations 2012. Integrating nutrition and physical activity [Internet]. Copenhagen, Denmark: Nordic Council of Ministers; 2014 [citerad 14 april 2025] s. 627. Report No.: Nord 2014: 002. Tillgänglig vid: https://www.norden.org/en/publication/nordic-nutrition-recommendations-2012
23. Commission of the European Communities. Reports of the Scientific Community of Food: Nutrient and energy intakes for the European Community. Luxembourg: Commission of the European Communities; 1993.
24. Green R, Charlton R, Seftel H, Bothwell T, Mayet F, Finch C, m.fl. Body iron excretion in man. American Journal of Medicine. 1968;45:336–53.
25. Hallberg L, Rossander-Hultén L. Iron requirements in menstruating women. Am J Clin Nutr. 1991;54(6):1047–58.
26. Hognert H, Skjeldestad FE, Gemzell-Danielsson K, Heikinheimo O, Milsom I, Lidegaard O, m.fl. Ecological study on the use of hormonal contraception, abortions and births among teenagers in the Nordic countries. BMJ Open. 2018;8:e022473.
27. Solberg A, Reikvam H. Iron Status and Physical Performance in Athletes. Life. 2007;10(13).
Näringsintag och klimatpåverkan – metodval viktigt vid databearbetning
Kommentar till studie
>>text: Anna Stubbendorff, nutritionist och doktorand, Institutionen för kliniska vetenskaper, Lunds universitet, Malmö
En nyligen publicerad studie i The American Journal of Clinical Nutrition visar att valet av metod för att rapportera växthusgasutsläpp (GHGE) från kosten har stor betydelse för vilka slutsatser som kan dras om sambandet mellan klimatpåverkan och näringsintag. Tre vanliga metoder jämfördes:
1. GHGE per dag (totalt utsläpp per individ)
2. GHGE per 1000 kcal (energidensitet)
3. GHGE per dag med justering för energiintag i statistiska modeller
När resultaten analyserades som intag av näringsämnen per dag – vilket överensstämmer med hur de flesta näringsrekommendationer är utformade – framkom att GHGE per dag var starkt kopplat till det totala energiintaget. Kostmönster med lägre GHGE per dag hade ofta också ett lägre energiintag, vilket påverkade näringsintaget negativt. Det kan leda till slutsatsen att mer klimatsmarta kostmönster är mindre näringsrika. Det är dock viktigt att inte bara titta på riktningen i sambandet, utan även på andelen som når upp till rekommenderat intag. För flera näringsämnen låg även kosten med lägst klimatpåverkan över rekommendationerna – vilket innebär att ett ännu högre intag inte är nödvändigt eller eftersträvansvärt.
När GHGE i stället relaterades till energiintaget förändrades bilden. Utsläpp uttryckta per 1000 kcal visade att kostmönster med lägre klimatpåverkan ofta hade högre näringstäthet, vilket skulle kunna tolkas som att de är mer näringsrika.
När GHGE per dag analyserades med energiintag som kovariat i statistiska modeller – det vill säga när man justerade för energiintaget – försvann många av sambanden helt.
Forskarna analyserade också näringsintag per 1000 kcal som utfall, vilket ytterligare påverkade vilka slutsatser som kunde dras.
Studien understryker att metodval inte enbart är en teknisk detalj, utan en avgörande faktor för hur resultaten tolkas. För att kunna dra rättvisa och jämförbara slutsatser om hållbara kostmönster krävs ett medvetet förhållningssätt till hur energiintag hanteras i analyserna – och hur slutsatser dras från resultat med olika metoder för databearbetning.
Varierande nivåer av kolesterolhöjande diterpener i maskinkaffe på arbetsplatser
Det är välkänt att ofiltrerat kaffe såsom kokkaffe innehåller höga nivåer av de kolesterolhöjande ämnena cafestol och kahweol. Med tanke på hur mycket kaffe som dricks på svenska arbetsplatser valde vi att undersöka nivåerna av dessa ämnen i kaffe från fikarumsautomater i en nyligen publicerad studie (1). Alla kaffeprover från den vanligaste typen av maskiner innehöll minst måttliga nivåer av diterpenerna cafestol och kahweol, men med viss variation mellan maskiner och över tid.
>>text: David Iggman, docent, Institutionen för folkhälso- och vårdvetenskap, Uppsala universitet, Uppsala
Kaffedrickande är i observationsstudier främst kopplat till positiva hälsoeffekter såsom minskad risk för hjärt-kärlsjukdom, typ 2-diabetes, vissa cancerformer och andra sjukdomar (2). Även om förväxlingsfaktorer kan påverka den typen av samband finns ingen generell rekommendation för vuxna att undvika kaffe ur hälsosynpunkt. Intaget bör dock begränsas hos gravida med tanke på koffeininnehållet.
De nordiska näringsrekommendationerna, NNR, rekommenderar filtrerat kaffe i första hand och att intaget av ofiltrerat kaffe bör begränsas. Dessa kostråd till befolkningen återfinns även från de norska och finska myndigheterna och innebär att kokkaffe och presskaffe bör begränsas, medan snabbkaffe och bryggkaffe kan vara hälsosammare val. Bakgrunden är att kokkaffe och annat ofiltrerat kaffe höjer kolesterolvärdena i blodet (3). Det upptäcktes på 90-talet att det berodde på lipiderna cafestol och kahweol (4) som finns i kaffebönorna och urlakas till drycken i samband med bryggningen. En metaanalys av randomiserade studier visade att sex koppar kokkaffe dagligen höjer LDL-kolesterolet (det så kallade onda kolesterolet) med cirka 0,40 mmol/L, vilket motsvarar en ökning på drygt 10 procent (5). Kaffe från andra bryggmetoder som använder metallfilter av olika slag (espresso, perkulator etc) brukar innehålla lägre diterpennivåer än kokkaffe men högre än bryggkaffe (6). Dock finns få publicerade studier på den typen av maskinkaffe som dricks på svenska arbetsplatser. Därför valde vi att studera ett mindre urval av maskinkaffe från svenska fikarum, nämligen från 14 sjukvårdsinrättningar vid Akademiska sjukhuset i Uppsala, Falu lasarett och två närliggande vårdcentraler. Studien genomfördes i samarbete mellan Uppsala universitet och Chalmers tekniska högskola.
Analyser av kaffe från 14 bryggmaskiner
Av de 14 maskinerna var 11 av en typ vi kallar bryggmaskin, som snabbt brygger en kopp kaffe i taget från malda bönor. Tre av maskinerna var av liquid-modell, som istället blandar hett vatten med kaffekoncentrat. Två prover togs på olika veckodagar med 2-3 veckors mellanrum, frystes in och skickades till Chalmers tekniska högskola i Göteborg för analys genom så kallad vätskekromatografi-tandem masspektrometri (LC-MS/MS), vilket är en av flera möjliga metoder att mäta koncentrationerna av diterpener. Kaffet från samtliga bryggmaskiner innehöll cafestol och kahweol i nivåer som låg betydligt högre än i samtliga referensprover med vanligt bryggkaffe. Flertalet av dessa prover hade högre koncentrationer än presskaffe och perkulatorkaffe, men lägre än kokkaffe. Att filtrera kokkaffet genom ett tyg sänkte tydligt nivåerna, som fortfarande var högre än efter användning av pappersfilter. För jämförelse insamlades även fyra espressoprover från cafeterior och fikarum omkring Chalmers tekniska högskola. Dessa provers nivåer av diterpener varierade stort, vilket var ett oväntat fynd som vi inte kan förklara i dagsläget.
Fler studier efterfrågas
Eftersom försökspersoner inte ingick i studien är det svårt att uttala sig om hur stor effekt maskinkaffet kan tänkas ha på blodfetterna. Då diterpennivåerna var lägre än i kokkaffe bör den kolesterolhöjande effekten vara mindre. Utifrån kända antaganden från äldre studier (7) uppskattades dock effekten på LDL-kolesterol till en större effekt på +0,58 mmol/L, förutsatt att en person dricker tre koppar kaffe på jobbet fem dagar i veckan. En sådan effekt kan översättas (8) till en kardiovaskulär relativ riskökning på 13 procent efter fem år eller 36 procent efter 40 års intag. Den riskökningen tror vi dock är en överskattning och det vore angeläget att gå vidare med en studie på försökspersoner som får dricka maskinkaffe regelbundet, för att säkrare bestämma effekterna på blodfetterna. Fler prospektiva observationsstudier (studier där individer följs framåt i tiden) på filtrerat visavi ofiltrerat kaffe efterlyses också. Det finns i nuläget endast en norsk studie som påvisat högre kolesterolnivåer och kardiovaskulär dödlighet hos personer som regelbundet dricker kokkaffe, jämfört med bryggkaffe (9).
Sammanfattningsvis innehöll de flesta kaffeprover från svenska arbetsplatser åtminstone måttliga nivåer av kolesterolhöjande ämnen. För personer som dricker kaffe på jobbet regelbundet förefaller ordentligt filtrerat kaffe såsom bryggkaffe eller snabbkaffe vara att föredra med tanke på kolesterolnivåer och framtida hjärt-kärlrisk. Det vore också önskvärt ur folkhälsosynpunkt att arbetsgivare och leverantörer säkerställer att maskinkaffe som tillhandhålls innehåller försumbara nivåer av dessa ämnen.
Författaren uppger inga jävsförhållanden.
Referenser
1. Orrje E, Fristedt R, Rosqvist F, Landberg R, Iggman D. Cafestol and kahweol concentrations in workplace machine coffee compared with conventional brewing methods. Nutr Metab Cardiovasc Dis. 2025 Feb 20:103933.
2. Poole R, Kennedy OJ, Roderick P, Fallowfield JA, Hayes PC, Parkes J. Coffee consumption and health: umbrella review of meta-analyses of multiple health outcomes [published correction appears in BMJ. 2018 Jan 12;360:k194.
3. Aro A, Tuomilehto J, Kostiainen E, et al. Boiled coffee increases serum low density lipoprotein concentration. Metabolism. 1987;36:1027–30.
4. Weusten-Van der Wouw MP, Katan MB, Viani R, Huggett AC, Liardon R, Liardon R, Lund-Larsen PG, Thelle DS, Ahola I, Aro A, et al. Identity of the cholesterol-raising factor from boiled coffee and its effects on liver function enzymes. J Lipid Res. 1994 Apr;35:721-33. Erratum in: J Lipid Res 1994 Aug;35(8):1510.
5. Schoeneck M, Iggman D. The effects of foods on LDL cholesterol levels: A systematic review of the accumulated evidence from systematic reviews and meta-analyses of randomized controlled trials. Nutr Metab Cardiovasc Dis. 2021;31(5):1325-1338.
6. Novaes FJM, Bayan FC, Neto FR de A, et al. The occurrence of cafestol and kahweol diterpenes in different coffee brews; [A ocorrência dos diterpenos cafestol e caveol em diferentes bebidas de café]. Coffee Sci. 2019;14:265–80.
7. Urgert R, Katan MB. The cholesterol-raising factor from coffee beans. Annu Rev Nutr. 1997;17:305–24.
8. Ference BA, Ginsberg HN, Graham I, et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J. 2017;38:2459–72.
9. Tverdal A, Selmer R, Cohen JM, et al. Coffee consumption and mortality from cardiovascular diseases and total mortality: Does the brewing method matter? Eur J Prev Cardiol. 2020;27:1986–93.
Nya kostråd lanserade
I höstas var Livsmedelsverkets uppdaterade kostråd för vuxna ute på remiss och nu är de nya kostråden lanserade. Sammanfattat anger råden att vi bör äta mycket grönsaker, frukt och fullkorn, och mindre av läsk, godis, fikabröd och snacks. Fisk och baljväxter är bra att äta ofta. I tidigare kostråd har detta också varit i fokus och har ytterligare stärkts av aktuell forskning. Man kan gärna äta kött, men inte så mycket och bara en liten del bör vara chark som korv och bacon.
Förra året publicerades de nya nordiska näringsrekommendationerna, NNR 2023, och NNR är den vetenskapliga basen för de nationella kostråden. NNR är en samlad genomgång och bedömning av den vetenskapliga litteraturen om näringsämnen, livsmedel och hälsa och ett nordiskt samarbete där flera hundra forskare och experter arbetar tillsammans.
Kostråden tas fram av respektive land för att spegla befolkningens matvanor, mattraditioner och livsmedelsval, och vad som är viktigt att fokusera på för att förbättra befolkningens matvanor och folkhälsa.
Hälsa är grunden i kostråden men råden tar också hänsyn till miljöpåverkan. I uppdateringen av kostråden ingick ett regeringsuppdrag att beakta en stärkt livsmedelsberedskap och en ökad svensk livsmedelsproduktion. Genom att äta mer enligt kostråden och dessutom välja svenskt stöttar vi svensk livsmedelsproduktion och livsmedelsberedskap, bidrar till en levande landsbygd och minskar matens negativa klimat- och miljöpåverkan.
De nya kostråden för vuxna i korthet:
- Håll igen på det söta, salta och feta – läsk, sötsaker och snacks.
- Ät mycket grönsaker, frukt och bär, minst 500 gram om dagen, gärna mer.
- Ät bönor, ärter och linser ofta – gärna varje dag.
- Välj fullkorn när du äter bröd, pasta och gryn.
- Ät fisk två-tre gånger i veckan.
- Ät gärna kött, men inte så mycket. Helst inte mer än 350 gram per vecka från nöt, gris och lamm. Det motsvarar 400–500 gram före tillagning. Bara en liten del bör vara chark, som korv och bacon.
- Ät mejeriprodukter varje dag, gärna syrade sorter som fil eller yoghurt.
- Välj rapsolja och andra Nyckelhålsmärkta matfetter i matlagning och på smörgås.
- Ät gärna två-tre matskedar osaltade nötter om dagen. Fröer är också bra för hälsan.
- Ät högst 6 gram salt om dagen. Välj joderat salt.
- Håll igen på alkohol.
Länkar med material och rapporter från Livsmedelsverket:
Folder med kortfattad presentation av kostråden för vuxna
Bildmaterial med exempel på vad råden innebär med mängder etc
Kostråden för vuxna i sin helhet, Livsmedelsverkets webb
Motiv och bakgrund till kostråden: Livsmedelsverkets generella kostråd för den vuxna befolkningen
Fördjupad konsekvensanalys av kostrådet om rött kött och chark
Ett steg i att öka kunskapen om matens klimatpåverkan
RISE klimatdatabas tillhandahåller data om klimatpåverkan från olika livsmedel. Sedan 2024 ingår även uppgifter om näringstäthet och påverkan på biologisk mångfald. Klimatdatabasen används som ett verktyg för att främja klimatmedvetna val och stödja organisationer i deras arbete med klimatmål och klimatrapportering.
>>text: Thomas Angervall, ansvarig för RISE klimatdatabas, RISE Research Institutes of Sweden och Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
Drygt 800 livsmedel ingår i klimatdatabasen
Klimatavtrycken i RISE klimatdatabas för livsmedel baseras på livscykelanalyser av drygt 800 livsmedel som är representativa för svensk livsmedelskonsumtion. Metoden livscykelanalys (LCA) är ISO-standardiserad och varje livsmedel har fått ett klimattal som visar vilken klimatpåverkan livsmedlet har.
Klimatdatabasen består av ca 1500 klimatavtryck. Klimatavtryck – eller ’carbon footprint’ – avser produkters klimatpåverkan och uttrycks här i kg koldioxidekvivalenter (CO2e) per kg livsmedel.
En livsmedelsråvaras klimatavtryck påverkas av flera faktorer, bland annat produktionsmetod och geografiskt ursprung, såsom odlingsland, ekologisk eller konventionell odling samt om produktionen sker på friland eller i växthus. Livsmedel i klimatdatabasen är kopplade till Livsmedelsverkets livsmedelsdatabas. Här finns ett utdrag från RISE klimatdatabas som visar klimattal från ett fyrtiotal livsmedel.
Näringstäthetsindex i klimatdatabasen
Från och med 2024 års version av klimatdatabasen ingår också ett näringstäthetsindex för varje livsmedel, desto högre näringstäthetsindex desto näringstätare livsmedel. Indexet är baserat på 11 näringsämnen som bör uppmuntras – protein, fibrer, vitamin A, C, E och D, folat, kalcium, järn, kalium och magnesium och 3 näringsämnen som bör begränsas – mättat fett, tillsatt socker och salt.
Nötkött från Sverige har näringstäthetsindex (NRF 11.3) 0,6 och socker -1,65 per 100 gram och klimattalet för nötkött är 28 och för socker 0,6 CO2e per kilo. Detta visar att nötkött har högre näringskvalitet jämfört med socker men klimatpåverkan är högre för nötkött än för socker.
Mycket arbete med uppbyggnad och utveckling av klimatdatabasen
Det krävs många arbetstimmar per år för att upprätthålla och uppdatera en klimatdatabas, vilket i princip kräver offentlig finansiering på något sätt. Klimatdatabasen är under ständig utveckling och uppdateringar görs årligen. RISE klimatdatabas lanserades för tio år sedan, och första åren gick det inte ihop ekonomiskt men efter tre-fyra år började det bli break even. RISE har dock lyckats med att etablera en klimatdatabas genom leasingavgifter från användare/kunder. Alla intäkter investeras i utveckling och förbättring av klimatdatabasen och dess plattform.
Nyheter 2024 var näringstäthetsindex och biodiversitetsavtryck och arbetet under 2025 fortsätter med att utveckla fler biodiversitetsavtryck och LUC-bidrag (Land Use Change).
Vilka använder klimatdatabasen?
RISE har ca 150 kunder/användare varav merparten är kommuner/regioner och livsmedelsföretag i Sverige och Norge.
Liknande klimatdatabaser finns i andra länder
Det förekommer liknande klimat- och miljödatabaser i andra länder, till exempel i Frankrike (Agribalyse).
Här kan du läsa mer:
RISE klimatdatabas för livsmedel | RISE
RISE Öppna listan 2.3 2024.pdf
Utlysning från Henning och Johan Throne-Holsts stiftelse
Henning och Johan Throne-Holsts stiftelse utlyser stipendier och projektanslag för forskning inom human nutrition och närliggande vetenskaper. Stiftelsen delar årligen ut 1-2 miljoner SEK.
Sista ansökningsdag: 1 mars 2025
För mer information samt ansökningsformulär, se stiftelsens hemsida.
Så äter småbarn – resultat från 1,5- och 4-åringar i Riksmaten småbarn
Livsmedelsverket genomför regelbundet nationella matvaneundersökningar för att samla in data om befolkningens matvanor. Informationen används bland annat till att följa livsmedelskonsumtion och näringsstatus i Sverige och som bas för risk- och nyttovärderingar av livsmedel och näringsämnen. Oönskade ämnen i livsmedel ingår också. Matvaneundersökningarna är en viktig grund vid utformning av kostråd och andra insatser som främjar folkhälsan.
För första gången har matvanorna hos 1,5-åringar undersökts, medan 4-åringarnas matvanor senast undersöktes för tjugo år sedan (1, 2). Resultatet visar att barnen generellt får i sig tillräckligt av de näringsämnen de behöver och risken för brist på vitaminer eller mineraler bedöms vara liten. Däremot äter både 1,5-åringarna och 4-åringarna för mycket rött kött och charkprodukter och 4-åringarna äter för lite grönsaker och frukt. Hälften av 4-åringarna får i sig mer fritt socker än rekommenderat och de flesta barn äter för mycket mättat fett och salt.
>>text: Lotta Moraeus, leg dietist, med dr, Elin Larsson, kostvetare, MSc, Helena Bjermo, MSc, med dr, Jessica Petrelius Sipinen, nutritionist, MSc, Emma Patterson, nutritionist, docent, Karin Stenberg, leg dietist, Sanna Lignell, toxikolog, med dr, och Anna Karin Lindroos, leg dietist, docent, Avdelningen för risk- och nyttovärdering, Livsmedelsverket, Uppsala
Lång process
Planeringen av undersökningen började 2019 med att vi bland annat kartlade och uppdaterade livsmedel och maträtter som småbarn äter och som saknades eller var utdaterade i vår livsmedelsdatabas. Vi inledde ett samarbete med Arbets- och miljömedicin (AMM) och Gymnastik- och idrottshögskolan för mätning av fysisk aktivitet. Sahlgrenska akademin bidrog med analys av avföringsprover. Vi testade också vår webbaserade matdagbok bland föräldrar i målgruppen och upphandlade ett Customer Relation Management (CRM) system för att kunna bjuda in och följa tusentals deltagare. Slutligen genomförde vi en pilotundersökning.
Deltagande
Hösten 2021 startade datainsamlingen. Familjer som var slumpmässigt utvalda av Statistiska centralbyrån (SCB) bjöds in med brev som följdes upp med telefonsamtal och SMS. Vi märkte snart att detta var en svår grupp att nå och att vi behövde bjuda in fler än vi räknat med för att nå det antal deltagare som behövdes i undersökningen. Drygt 1800 småbarnsfamiljer – 1078 1,5-åringar och 750 4-åringar – spridda över hela Sverige deltog i studien, vilket motsvarar en svarsfrekvens på drygt 10 procent. Det var lägre än vi hade hoppats på men inte helt oväntat med tanke på den sjunkande trenden att vilja delta i studier.
Studiepopulationen speglade fördelningen bland svenska småbarn gällande kön, kommuntyp, geografi och hushållets sammansättning. Barn i hushåll med kortare utbildning, lägre inkomst och med båda föräldrarna födda utanför Sverige var underrepresenterande. Nästan alla 4-åringar och två tredjedelar av 1,5-åringarna gick i förskola.
Datainsamling
Information om matvanor och andra levnadsvanor samlades in genom matdagbok och enkät mellan september 2021 och juni 2023. Rörelsemätning under sju dagar var en valbar del för samtliga, medan blod- och urinprovtagning samt avföringsprov var valbara delar i en subgrupp av deltagarna.
Matdagboken fylldes i på webben under två dagar, även när barnet var på förskola, via det webbaserade verktyget RiksmatenFlex. När deltagarna registrerade vad barnet åt och drack kunde de välja livsmedel utifrån en förutbestämd livsmedelslista anpassad för småbarn. För att uppskatta mängder kunde deltagarna välja mellan olika portionsbilder, antal eller hushållsmått som matsked och deciliter. Om barnet var på förskola någon av registreringsdagarna instruerades föräldrarna att be personalen fylla i en pappersdagbok som de sedan förde över till den webbaserade matdagboken.
De deltagare som bodde i en kommun med maximalt 50 km till en AMM-klinik tillfrågades om att lämna blod- och urinprov och drygt 500 barn gjorde detta. Deltagare tillfrågades slumpmässigt och spritt över hela Sverige om att lämna avföringsprov.
Huvudresultat
Livsmedelskonsumtion och näringsintag från de två dagarna i matdagboken långtidsjusterades med den statistiska metoden Multiple Source Method, MSM-metoden, för att bättre spegla det vanliga intaget (3). Denna fungerar bra på mindre grupper, ger data på individnivå samt kan ta hänsyn till nollkonsumenter. Individer som aldrig äter ett visst livsmedel, nollkonsumenter, identifierades genom enkätfrågor vid justeringen till långtidsintaget (exempelvis ”Äter ditt barn fisk”). Beräkningarna gjordes för respektive livsmedelsgrupp och näringsämne uppdelat på kön och åldersgrupp. För att minska effekten av snedvridningen på grund av skillnad i deltagande mellan hushåll med föräldrar som har lång respektive kort utbildning, användes statistiska vikter som SCB tog fram baserat på bortfallet.
Livsmedelskonsumtion
Grönsaker och frukt varje dag
De flesta barn äter grönsaker och frukt varje dag och får i sig tillräckligt mycket fibrer. Det är dock färre än en av tio 4-åringar som når kostrådet om minst 400 gram grönsaker och frukt om dagen (4). 1,5-åringar äter ungefär lika mycket grönsaker och frukt som 4-åringar, trots att 4-åringarna är större och äter mer mat. I snitt äter barnen 275 gram grönsaker och frukt per dag.
Många barn äter fisk och skaldjur
Tre av fyra barn äter fisk varje vecka. En tredjedel äter fisk 2–3 gånger i veckan, vilket kostrådet rekommenderar (4).
För mycket rött kött och chark
De flesta av barnen äter mindre än 500 gram rött kött och chark i veckan men 46 procent av 1,5-åringarna och 65 procent av 4-åringarna äter mer än 350 gram i veckan, vilket är maxgränsen för vuxna i de nordiska näringsrekommendationerna från 2023 (5). Merparten av köttkonsumtionen består av charkprodukter som korv. Pojkar äter mer rött kött och chark än flickor och barn till föräldrar med kortare utbildning äter mer än barn till föräldrar med längre utbildning (figur 1). Ungefär en tredjedel av deltagarna uppgav att familjen äter mindre kött nu än för ett år sedan.

Sötsaker äts mest bland de äldre barnen
En av de tydligaste skillnaderna mellan 1,5- och 4-åringar gäller konsumtion av sötsaker. Drygt en tiondel av de yngre barnen och 80 procent av de äldre äter godis minst en gång i veckan. En tredjedel av de yngre och 60 procent av 4-åringarna äter bullar och kakor minst en gång i veckan. Det är färre som dricker söta drycker, en av tio 1,5-åringar och fyra av tio 4-åringar dricker läsk en gång i veckan eller mer. Bland 4-åringarna var det tydligt att lördagsgodis fortfarande är ett koncept eftersom konsumtionen toppade under helgen och framför allt på lördagen (figur 2).
Bland 1,5-åringarna äter barn till föräldrar med kortare utbildning oftare sötsaker och snacks och dricker oftare söta drycker än de som har föräldrar med längre utbildning. Bland 4-åringarna sågs denna skillnad bara när det gällde godis. När det gäller bullar och kakor var det tvärtom – 4-åringar till föräldrar med längre utbildning åt mer bakverk.

Energigivande näringsämnen
Nästan alla barn äter för mycket mättat fett och för lite omättat fett. De flesta 1,5-åringar får i sig den rekommenderade mängden fleromättat omega-3-fett, jämfört med endast en fjärdedel av 4-åringarna. Samtliga barn hade ett proteinintag per kilo kroppsvikt som översteg både genomsnittsbehovet och rekommenderat intag (5) och 1,5-åringarna hade en högre andel protein i maten än 4-åringarna. Mejeriprodukter samt rött kött och chark – inklusive hela kötträtter – bidrog mest till proteinintaget.
Nästan hälften av 4-åringarna hade ett intag av fritt socker över rekommendationen på 10 E% (5). Bland 1,5-åringarna, där rekommendationen är att fritt socker helt ska undvikas, åt alla barn mer än 0 E%. Få hade dock ett intag över 10 E%.
Vitaminer och mineraler
Resultaten visar att barnen generellt får i sig tillräckligt av de näringsämnen de behöver och risken för brist på vitaminer eller mineraler bedöms vara liten (5). De flesta har tillräckliga nivåer av vitamin D i plasma och ingen har så låga nivåer att det indikerar brist. Även jodhalterna i urin och folathalterna i plasma visar på ett tillräckligt intag bland barnen. Intaget av järn, kalcium och magnesium är också tillräckligt men marginalen till när en risk för brist uppstår är mindre än för de andra vitaminerna och mineralerna (figur 3). För järn visade blodproverna att ungefär 6 procent har järnbrist, en förekomst som enligt WHO:s definition är precis över gränsen för att klassas som ett milt folkhälsoproblem (6). Risken för järnbrist bland svenska småbarn bedöms dock som låg, baserat på den sammantagna bedömningen av intagsdata och biomonitoreringsdata. Småbarn har ett ökat behov av järn och rekommenderas att äta berikade livsmedel så som gröt och välling. Det var dessa livsmedel, rött kött och chark samt bröd som bidrog mest till intaget av järn. Barnen får generellt i sig betydligt mer natrium än rekommenderat (figur 3).

Matvanorna har förbättrats bland 4-åringar
Fyraåringar undersöktes senast för ungefär 20 år sedan, i Riksmaten barn 2003 (2). Sedan dess verkar åldersgruppens matvanor ha förbättrats något. De äter mer grönsaker och frukt och mindre rött kött och chark. Andelen energi som kommer från energitäta och näringsfattiga livsmedel som sötsaker och snacks har också minskat, från 25 till 15 procent av energin.
Det finns metodskillnader mellan undersökningarna och svarsfrekvensen samt andel föräldrar med kort utbildning är lägre i Riksmaten småbarn vilket kan påverka resultaten. Men de förändringar vi ser är så pass stora att de troligtvis representerar en verklig förändring. Vad detta kan bero på kan inte undersökningen påvisa. En möjlig förklaring är att debatten om hur socker och kött påverkar på hälsa och miljö kan ha bidragit. Även om vi ser att det går i en positiv riktning så är det fortfarande en lång bit kvar tills många kostråd och rekommendationer nås.
Vidare rapportering
Under våren 2025 kommer fördjupade analyser att göras, bland annat om hur fysiskt aktiva barnen är, matens miljöpåverkan och analyser av oönskade ämnen i blodet. En rapport om de allra yngsta deltagarna i Riksmaten småbarn, bebisar på 9 månader, kommer också under 2025.
Referenser
1. Moraeus L, Bjermo H, Petrelius Sipinen J, Patterson E, Larsson E, Stenberg K, Lindroos A K. 2024. L 2024 nr 12: Riksmaten småbarn 2021–24 – Så äter småbarn i Sverige. Livsmedelsverkets rapportserie. Uppsala.
2. Enghardt Barbieri, H., Pearson, M. & Becker, W. 2006. Riksmaten – barn 2003. Livsmedels- och näringsintag bland barn i Sverige. Tillgänglig: Livsmedelsverkets webbplats (https://www.livsmedelsverket.se) [Hämtad 2024-10-15].
3. Harttig, U., Haubrock, J., Knuppel, S. & Boeing, H. 2011. The MSM program: web-based statistics package for estimating usual dietary intake using the Multiple Source Method. Eur J Clin Nutr, 65 Suppl 1, S87-91. DOI: https://doi.org/10.1038/ejcn.2011.92
4. Eneroth, H. & Björk, L. 2015. Bra livsmedelsval för barn 2-17 år – baserat på nordiska näringsrekommendationer 2012. (Livsmedelsverkets rapportserie Rapport 11 – 2015.) Livsmedelsverket. Tillgänglig: Livsmedelsverkets webbplats (https://www.livsmedelsverket.se) [Hämtad 2024-10-15].
5. Blomhoff, R., Andersen, R., Arnesen, E. K., Christensen, J. J., Eneroth, H., Erkkola, M., Gudanaviciene, I., Meltzer, H. M., Pitsi, T., Schwab, U., Siksna, I., Dorsdottir, I. & Trolle, E. 2023. Nordic Nutrition Recommendations 2023. Nordic Council of Ministers.
6. WHO. 2020. WHO guideline on use of ferritin concentrations to assess iron status in individuals and populations. Licence: CC BY-NC-Sa 3.0 IGO.) World Health Organization (WHO). Tillgänglig: WHOs webbplats (https://iris.who.int) [Hämtad 2024-10-15].
Förslag till nya kostråd är ute på remiss
Nu finns möjlighet att lämna synpunkter på förslaget till nya kostråd fram till den 22 oktober 2024. Livsmedelsverket kommer att presentera de färdiga kostråden i början av 2025.
NNR är den vetenskapliga basen för de nationella kostråden
Förra året publicerades de nya nordiska näringsrekommendationerna, NNR 2023, och under året har Livsmedelsverket arbetat med uppdateringen av de svenska kostråden. Hälsa är grunden i kostråden men råden tar också hänsyn till miljöpåverkan. I nuvarande uppdatering av kostråden ingår också ett regeringsuppdrag att beakta en stärkt livsmedelsberedskap och en ökad svensk livsmedelsproduktion.
Mer frukt och grönt och mindre rött kött
Några förändringar sedan förra kostråden 2015 är att rådet om mängden frukt och grönt har höjts något beroende på att baljväxter inte längre ingår i rådet om minst 500 gram frukt och grönt per dag. Baljväxter lyfts i ett eget råd – ät baljväxter ofta, gärna varje dag.
Rådet om mängden rött kött (nöt, gris, får och vilt) har sänkts, från högst 500 gram per vecka till 350 gram. Endast en liten del bör vara charkprodukter som korv och skinka.
Förslagen till de nya kostråden är publicerade i rapporten Livsmedelsverkets generella kostråd för den vuxna befolkningen. I rapporten beskrivs också potentiella effekter och konsekvenser av de uppdaterade kostråden. I analyserna används två scenarier – befolkningens matvanor blir 5 respektive 20 procent mer lika de nya kostråden. Beräkningarna visar på förbättrad folkhälsa och att många dödsfall i kranskärlssjukdom, stroke, cancer eller typ 2-diabetes kan förhindras.
Kostråden i korthet:

Se hearingen i efterhand
Vid Livsmedelsverkets hearing den 25 september 2024 presenterades de nya kostråden, hur arbetet med kostråden gått till, presentationer om vilka effekter kostråden kan få på folkhälsan och hur vi gör verklighet av kostråden.
Här finns information om hur du lämnar synpunkter på rapporten.
Rekommendationerna om ätande under det första levnadsåret i NNR 2023
Agneta Hörnell har tillsammans med Hanna Lagström skrivit den artikel som utgör basen för rekommendationerna kring amning och tillvänjning (1) som finns i de nya nordiska näringsrekommendationerna (NNR) från 2023 (2).
Rekommendationerna kring amningen är detsamma som i NNR2012 – fullgångna, normalviktiga barn rekommenderas exklusiv amning i 6 månader med vitamin D som enda tillskott, följt av fortsatt amning tillsammans med fast föda det första året eller så länge mamman och barnet vill. Detta baseras på de många positiva effekter amningen har – för barnets och mammans hälsa, för folkhälsan och inte minst för miljön.
I sin artikel går Agneta Hörnell och Hanna Lagström igenom amning, bröstmjölkens innehåll, amningsstatistik i de nordiska och baltiska länderna, samt hälsoeffekter av små barns kost. Ett nytt omfattande avsnitt handlar om tillvänjningen till fast föda. Det inkluderar även viktiga aspekter på en huvudsakligen vegetarisk kost till spädbarn, eftersom intresset hos föräldrar sannolikt kommer att öka som en följd av det globala rådet att minska andelen animalier i kosten.
>> text: Agneta Hörnell, professor i kostvetenskap, legitimerad dietist, Institutionen för Kost- och Måltidsvetenskap, Umeå universitet, Umeå
Den första tiden
Bröstmjölk är en naturlig och hållbar föda för spädbarn. Globalt rekommenderar de flesta officiella organ enbart amning de första 6 månaderna och fortsatt amning till 1 eller 2 år – eller längre om mamman och barnet vill. I de nordiska och baltiska länderna ammas mellan 30 och 60 procent av 12-månader gamla barn. Bröstmjölk ger det nyfödda barnet näringsämnen i en effektivt absorberbar kombination och innehåller en lång rad bioaktiva faktorer med viktiga hälsofrämjande biologiska funktioner. Amning har positiva hälsoeffekter för både barnet och den ammande mamman. Ur ett folkhälsoperspektiv är det därför viktigt att skydda, stödja och främja amning.
Modersmjölksersättning
Om mamman inte vill amma alls eller om det finns problem med amningen innan barnet är 4 månader gammalt måste barnet få modersmjölksersättning. Orsaken kan vara att bröstmjölken inte räcker till trots kvalificerad amningsrådgivning och mer intensiv amning, eller att amningen måste avslutas av medicinska eller andra skäl. Det är bra om amningen kan fortsätta delvis eftersom även små mängder bröstmjölk har positiva effekter.
Ålder vid start av fast föda
De flesta rekommendationer anger att fast föda bör introduceras omkring 6 månaders ålder och inte före 4 månader. Det finns flera utvecklingsmässiga milstolpar som signalerar att ett spädbarn är fysiskt redo att börja processen att byta från mjölkmatning till familjens mat, till exempel att de kan sitta utan stöd och hålla huvudet stadigt eller att de försöker plocka upp saker och stoppa dem i munnen. Dessa milstolpar kommer ibland redan vid 3–4 månader, men oftast omkring 5–7 månader. Tidiga signaler innebär inte att det finns ett näringsmässigt behov att starta med puréer. När tillvänjningen till fast föda inleds bör barnet få mat från alla livsmedelsgrupper. Järnrika livsmedel bör ingå och även potentiellt allergiframkallande livsmedel eftersom forskning visat att risken för senare allergiutveckling på så sätt minskar.
Känsliga respektive kritiska perioder är begrepp som används i samband med lämplig ålder för start av tillvänjningen. Det är viktigt att skilja mellan dessa. Under en känslig period är det lättare att lära sig ett nytt beteende. Efter den perioden är inlärning fortfarande möjlig men kan ta lite längre tid. Kritiska perioder är mer av ett möjlighetsfönster, det vill säga om exponering inte sker under den perioden blir inlärning mycket svårare. Att lära sig att tugga verkar till exempel ha en kritisk period mellan 6 och 9 månaders ålder, och om barn fortsätter att få huvudsakligen puréad mat ökar risken för senare problem med att äta. Smakpreferenser handlar mer om känsliga perioder, och det är aldrig för sent att lära sig tycka om ny mat.
Att påverka matpreferenser
Små barn bör inte få sötade livsmedel eftersom det förstärker den medfödda förkärleken för söt smak som alla barn har. Barn har också en medfödd aversion mot bittra smaker, som finns i många grönsaker. För att komma över den initiala aversionen är det bra att ge många varianter av grönsaker tidigt eftersom det vanligtvis krävs betydligt fler upprepningar för att nå acceptans än för sötare livsmedel, som exempelvis frukt.
Det mamman äter under graviditeten och amningen påverkar smaken på fostervattnet och bröstmjölken och därmed barnets senare matpreferenser. Om mamman äter mycket grönsaker blir tillvänjningen enklare. Unga vuxna äter relativt lite grönsaker vilket alltså är negativt både för dem själva och för deras barn. En mer växtbaserad kost är även bra av miljöskäl för alla åldrar.
Barn är evolutionärt förberedda att lära sig och anpassa sig utifrån ledtrådar i sin omgivning. Att äta tillsammans i en trevlig miljö där föräldern fokuserar på barnet genom samtal och ögonkontakt är också viktigt vid tillvänjningen. Hunger och mättnadssignaler bör styra matningen och mat ska normalt inte användas som tröst eller belöning.
Hur snabbt ett spädbarn accepterar nya livsmedel beror på flera faktorer. Om de ammas eller får modersmjölksersättning har betydelse. Samma gäller för de smakpreferenser de föds med. Ytterligare en faktor är sensorisk känslighet och ålder vid introduktion. Sättet som nya livsmedel introduceras påverkar också. Människor är flockdjur. Barns vilja att smaka påverkas av att få vara med vid matbordet redan innan tillvänjningen. Att se andra barn äta kan vara extra viktigt. Barn kan lära sig uppskatta nya livsmedel på flera andra sätt, till exempel genom att få smaka på det ”nya” upprepade gånger så det känns mer och mer bekant eller att få ny mat tillsammans med något redan accepterat.
Växtbaserat till barn
Vi bör äta en större andel växtbaserad mat, både av hälsoskäl och miljöskäl och intresset för att ge även små barn en vegetarisk kost har ökat. Oavsett om föräldrar väljer att ge sina barn blandkost eller vegetarisk kost är det avgörande med kunskap för att planera och laga en adekvat kost för att säkra barnets omedelbara och framtida hälsa. Naturligt näringsrika livsmedel är generellt att föredra. Ju fler livsmedel och livsmedelsgrupper som utesluts desto viktigare blir näringsinnehållet i det som barnet faktiskt äter.
Den stora andelen barn med övervikt och fetma tydliggör konsekvenserna av en dåligt planerad blandkost med för stor andel ”utrymmesmat” – mat med hög andel mättat fett, socker och salt. Den kosten medför också en ökad risk för att senare få cancer, hjärt-kärlsjukdomar och diabetes.
Synen på vegetarisk kost till barn har förändrats radikalt under de senaste decennierna. Numera anger befintliga riktlinjer i de flesta länder att välplanerade vegetariska och veganska koster, som inkluderar relevanta berikade livsmedel och kosttillskott, är näringsmässigt adekvata och lämpliga för alla livets stadier, inklusive graviditet, amning, och barndom.
Vikten av noggrann planering och inkludering av kosttillskott och berikade livsmedel är avgörande för vegansk eller vegetarisk kost för barn eftersom de behöver en mer näringsrik kost än vuxna för att säkerställa normal tillväxt och utveckling. Konsekvenserna av lågt intag av vissa näringsämnen, till exempel B12, kalcium och järn, kan vara allvarliga och oåterkalleliga. Det är viktigt att föräldrar har kunskap om att nivåerna av berikning av liknande livsmedel kan variera kraftigt. De behöver därför läsa information på förpackningarna noggrant, så att deras barns intag inte överskrider övre gränser för näringsämnen, till exempel jod. Ett för högt intag kan nås om barnet äter flera sorters berikade livsmedel med höga nivåer av berikning – och, särskilt om de också äter kosttillskott. Därför gäller det att räkna samman innehållet av näringsämnen i alla livsmedel. Det är också viktigt att veta att ekologiska produkter bara får berikas med lagstadgade näringsämnen – i dagsläget innebär det att de enbart berikas med D-vitamin.
För små barn kan det också vara svårt att äta tillräckligt med mat för att täcka energibehovet eftersom växtbaserad mat vanligtvis har stor volym på grund av högt fiberinnehåll och relativt lågt energiinnehåll. Föräldrar måste därför se till att barnen följer sina tillväxtkurvor. Om familjen äter en vegetarisk eller vegansk kost rekommenderas fortsatt amning efter ett års ålder. För veganfamiljer där spädbarnet kräver mer mjölk än bröstmjölk är alternativen begränsade. För närvarande finns det inga veganska modersmjölksersättningar till salu i butiker i de nordiska länderna, även om det kan köpas online.
Hälsoeffekter av spädbarnskost
Bröstmjölk innehåller många näringsämnen och biologiskt aktiva ämnen, inklusive vitaminer, mineraler, fettsyror och immunfaktorer, och många av dessa har positiva effekter på hälsan. Näringsämnen i bröstmjölken har flera funktioner relaterade till optimal tillväxt, utveckling och fysiologiska funktioner. Brister under de första två åren kan orsaka permanenta skador.
Många studier har visat långsiktiga fördelaktiga effekter av amning på hälsan för både barnet och den ammande kvinnan. Bröstmjölk har liknats vid personlig medicin för spädbarn. Forskningen har varit omfattande inte minst på grund av det stora intresset för den effekt som kost kan ha på framtida hälsa. De positiva hälsoeffekterna beror till stor del på själva bröstmjölken och dess unika sammansättning och hur länge barnen ammas. Men även kroppskontakten under amningen kan påverka. Kroppskontakt går naturligtvis att ha även om barnet flaskmatas, men det kräver mer aktiv planering.
En viktig faktor när man ska jämföra studier är också vad icke-ammade eller delvis ammade spädbarn matas med istället för bröstmjölk. Att tolka resultaten av olika studier försvåras av att definitionen av amning varierar mellan studier och att metoden som används för att bedöma amning ofta är oklar. Påverkan av amning och bevisnivån varierar också för olika hälsoresultat.
Det finns övertygande bevis för att amning har en skyddande effekt mot infektioner, akut öroninflammation, mag-tarminfektioner och luftvägsinfektioner även i höginkomstländer. Detta beror sannolikt på de många skyddande faktorer som bröstmjölken innehåller. Amning har också en trolig skyddande effekt mot övervikt och fetma. Orsakerna till detta är mer oklara, men några möjliga vägar är att förändringen av bröstmjölkens sammansättning under ett amningstillfälle skulle kunna göra att det ammade barnet får lättare att känna igen mättnadssignaler – och att bröstmjölk har ett lägre proteininnehåll än modersmjölksersättning, välling och komjölk. Det kan också handla om epigenetiska (länk mellan arv och miljö) effekter och programmering kopplade till bröstmjölken.
Vad gäller celiaki (glutenintolerans), diabetes, hjärt-kärlsjukdom och allergier är sambanden med amning mer oklara och vad barnet i övrigt äter kan vara viktigare. Viss forskning visade tidigare att introduktion av gluten under samtidig amning skyddade mot både celiaki och diabetes typ-1. Numera är fokus mer på själva glutenintaget och rekommendationen är att introducera gluten i små mängder när tillvänjningen startar och behålla mängderna små under det första levnadsåret. Rekommendationen är liknande vad gäller allergena livsmedel, som jordnötter och ägg. Flera studier har visat att tidig introduktion är bättre än de tidigare råden om att undvika dessa livsmedel under det första levnadsåret.
Exakt hur tidigt introduktionen av allergena livsmedel bör ske debatteras dock, bland annat eftersom tidig introduktion skulle kunna påverka amningen negativt. Denna risk bedöms större om en allmän rekommendation skulle vara att starta med allergena livsmedel redan omkring 4 månader eller till och med tidigare. Att så tidig introduktion inte visat negativa effekter på amningen i studier där amning uppmuntras, innebär inte att amningen skulle förbli opåverkad i allmänhet. Det är därför sannolikt klokt att i nuläget rekommendera att introduktion av allergiframkallande livsmedel bör börja när tillvänjningen startar, men inte före 4 månader.
Referenser
1. Hörnell A, Lagström H. Infant feeding – a scoping review for Nordic Nutrition Recommendations 2023. Food and Nutrition Research 2024;68:10456. https://doi.org/10.29219/fnr.v68.10456).
2. Blomhoff R, Andersen R, Arnesen EK, Christensen JJ, Eneroth H, Erkkola M, et al. Nordic Nutrition Recommendations 2023 – Integrating environmental aspects. Copenhagen: Nordic Council of Ministers, 2023. https://www.norden.org/en/publication/nordic-nutrition-recommendations-2023
Läkemedel som stöd för viktminskning – och fler är på gång
Obesitas kräver en strukturerad behandling som i grunden handlar om att minska intaget av energi. Det är en mycket krävande behandling för den enskilde. För att underlätta viktminskning och möjligheten att behålla den nya vikten finns läkemedel som tillägg eller verktyg till grundbehandlingen. Samtliga läkemedel i denna sammanställning ska ordineras av läkare efter noggrann utredning. Behandlingen måste följas upp för att kontrollera effekten och eventuella biverkningar. Artikeln är den andra delen om obesitas och medicinsk behandling. Se också del 1, Obesitas – så säger forskningen om medicinsk behandling.
>> text: Ingrid Larsson, näringsfysiolog, docent, universitetssjukhusöverdietist, Enheten för klinisk nutrition och Regionalt obesitascentrum, Sahlgrenska universitetssjukhuset, Göteborg
Orlistat
Orlistat finns sedan mer än två decennier och är en så kallad pankreaslipashämmare. Orlistat ska kombineras med energireducerad kost och regelbunden fysisk aktivitet. Verkningsmekanismen för orlistat är att läkemedlet hindrar absorptionen av cirka 30 procent av fettet i maten genom att hämma enzymet lipas från bukspottskörteln (pankreas). Det betyder att en del av energin i maten inte absorberas utan följer med avföringen ut. Den ytterligare viktminskningen med orlistat är 3 till 4 kilo på 4 års sikt (1). Om man äter en fettrik kost kommer biverkningarna – oljiga diarréer och gasbildning – att öka varför det är viktigt att kombinera orlistat med ändrade matvanor. Orlistat ges i kapselform.
Naltrexon/bupropion (Mysimba)
Naltrexon/bupropion dämpar aptiten och ökar mättnaden efter måltiden. Läkemedlet i tablettform ska kombineras med energireducerad kost och regelbunden fysisk aktivitet. Vid behandling med naltrexon/bupropion kan matens mättnadsökande effekt bidra till läkemedlets effekt på vikten. Vid behandling av naltrexon/bupropion uppnås drygt 9 procent viktminskning på 12 månaders sikt (2).
Liraglutid och semaglutid (Saxenda och Wegovy)
Liraglutid minskar aptiten och ökar mättnaden genom att förstärka effekten av mättnadshormonet GLP-1. Både liraglutid och semaglutid ges i form av injektioner, antingen en per dag (liraglutid) eller en gång per vecka (semaglutid). Behandling med liraglutid respektive semaglutid ska kombineras med energireducerad kost och regelbunden fysisk aktivitet. Vid behandling med liraglutid eller semaglutid känner patienten förutom minskad aptit och ökad mättnad också minskad lust att äta söt och fet mat.
En studie visar att liraglutid i kombination med fysisk aktivitet gav en större viktminskning jämfört med liraglutid som ensam behandling (3). Den studien inleddes med 8 veckor komplett kostersättning och därefter kostintervention för bibehållande av vikt. I en annan studie jämfördes liraglutid med semaglutid som tillägg till energireducerad kost (-500 kcal per dag) och ökad fysisk aktivitet. Resultatet gav en viktminskning på 15,8 procent för semaglutid och 6,4 procent för liraglutid (4).
Av ovanstående beskrivna läkemedel ingår orlistat i den statliga läkemedelsförmånen medan liraglutid och semaglutid för närvarande (2024) inte gör det vid behandling av obesitas.
Det finns ytterligare läkemedelssubstanser som är aktuella vid obesitasbehandling. De är ännu inte tillgängliga på den svenska marknaden.
Tirzepatid
Ett av kommande läkemedel på den svenska marknaden är tirzepatid (godkänd december 2023) som är en kombination av GLP-1 och GIP (glukosberoende insulintrofisk polypeptid). Mekanismen för viktminskning är densamma som för semaglutid, att minska aptiten. Tirzepatid ska kombineras med energireducerad kost och regelbunden fysisk aktivitet. Tirzepatid ges i form av en injektion en gång per vecka. I en 12-månadersstudie minskade vikten med drygt 20 procent i gruppen som fick högsta dosen av läkemedlet (5).
Mättnadseffekter av maten beroende av sammansättning
Läkemedelsbehandling vid obesitas ska ges som tillägg till energireducerad kost och ökad fysisk aktivitet. Vid användning av orlistat är det även viktigt att fettintaget är begränsat för att begränsa biverkningar. När det gäller liraglutid, semaglutid, tirzepatid och naltrexon/bupropion kan matvanornas verkan på mättnaden optimeras så att dessa leder till förstärkning av läkemedelseffekten. Det är också viktigt att kosten har optimal näringstäthet. Almandoz och medarbetare har sammanställt nutritionella hänsynstaganden vid behandling med läkemedel mot obesitas (6).
En voluminös kost som är rik på fiber och fullkorn är mer mättande än en kost med liten volym utan fiber. Den senare har oftast högre energidensitet än den förra. Större volym medför oftast glesare med energi. De nordiska näringsrekommendationerna lyfter fram en större andel grönsaker, frukt, baljväxter, fullkornsrika cerealier för att få hälsosamma matvanor (7).
Mättnaden av en måltid kan även ökas med hjälp av bland annat följande:
- äta grönsakerna först i måltiden
- välja fiberrika grönsaker framför fibersnåla
- fullkornsvarianter av bröd, pasta, gryn, müsli
- frukt/fruktsallad som dessert
- gröt eller yoghurt och müsli i stället för smörgås
- maträtter som grytor och soppor
- proteinrika livsmedel såsom fisk, ägg, kött, fågel, baljväxter, magra mejerier
En regelbunden måltidsordning har också positiv påverkan på energiintag och mättnad och är en av de grundläggande delarna i nutritionsbehandling vid obesitas. Det är viktigt att förstå att läkemedel mot obesitas är ett verktyg till ändrade matvanor. Dessutom är det mycket viktigt att näringsintaget optimeras enligt rekommendationerna för hälsosamma matvanor (6).
Det är för närvarande (2024) inte klarlagt hur länge medicinering med obesitasläkemedel kan ske. Oavsett längden på läkemedelsbehandlingen är det av yttersta vikt att patienter som genomgår obesitasbehandling ges råd om hälsosamma, näringstäta matvanor som minskar risken för hjärt- och kärlsjukdom och andra obesitasrelaterade sjukdomar.
Sammanfattningsvis har kost och nutrition en mycket central roll i obesitasbehandlingen för en lägre vikt oberoende vilken metod för viktminskning man använder. Kostens sammansättning kan optimera mättnaden och underlätta viktminskning och att bibehålla denna. Tillsammans med aptitdämpande läkemedel kan denna effekt förstärkas på sätt som inte tidigare varit möjligt.
Det är ett krävande och omfattande arbete att förändra sina matvanor, andra vanor och beteenden för att nå en lägre vikt. För att ändra vanor för en bibehållen lägre vikt krävs tålamod och långsiktig uthållighet. Det är därför helt naturligt att behöva stöd i förändringsarbetet.
Referenser
1. Torgerson JS, Hauptman J, Boldrin MN, Sjöström L. XENical in the prevention of diabetes in obese subjects (XENDOS) study: a randomized study of orlistat as an adjunct to lifestyle changes for the prevention of type 2 diabetes in obese patients. Diabetes Care. 2004;27(1):155-61.
2. Wadden TA, Foreyt JP, Foster GD, Hill JO, Klein S, O’Neil PM, et al. Weight loss with naltrexone SR/bupropion SR combination therapy as an adjunct to behavior modification: the COR-BMOD trial. Obesity (Silver Spring). 2011;19(1):110-20.
3. Lundgren JR, Janus C, Jensen SBK, Juhl CR, Olsen LM, Christensen RM, et al. Healthy Weight Loss Maintenance with Exercise, Liraglutide, or Both Combined. N Engl J Med. 2021;384(18):1719-30.
4. Rubino DM, Greenway FL, Khalid U, O’Neil PM, Rosenstock J, Sorrig R, et al. Effect of Weekly Subcutaneous Semaglutide vs Daily Liraglutide on Body Weight in Adults With Overweight or Obesity Without Diabetes: The STEP 8 Randomized Clinical Trial. Jama. 2022;327(2):138-50.
5. Jastreboff AM, Aronne LJ, Ahmad NN, Wharton S, Connery L, Alves B, et al. Tirzepatide Once Weekly for the Treatment of Obesity. N Engl J Med. 2022;387(3):205-16.
6. Almandoz JP, Wadden TA, Tewksbury C, Apovian CM, Fitch A, Ard JD, et al. Nutritionalconsiderations with antiobesity medications. Obesity (Silver Spring). 2024.
7. Blomhoff R, Andersen, R., Arnesen, E.K., Christensen, J.J., Eneroth, H., Erkkola, M., Gudanaviciene, I., Halldorsson, T.I., Høyer-Lund, A., Lemming, E.W., Meltzer, H.M., Pitsi, T., Schwab, U., Siksna, I., Thorsdottir, I., Trolle, E. Nordic nutrition rcommendations 2023. Copenhagen: Nordic Council of Ministers; 2023.
Antiinflammatorisk kost som behandling av reumatoid artrit
Reumatoid artrit – ledgångsreumatism – är en vanlig kronisk sjukdom. Namnet till trots drabbar den inflammatoriska sjukdomen inte bara kroppens leder utan även andra organ. Många upplever att sjukdomen och symtomen påverkas av maten. Men resultaten av de koststudier som gjorts är dock inte helt entydiga.
I den randomiserade crossoverstudien ADIRA (Anti-inflammatory Diet In Rheumatoid Arthritis) undersöktes effekterna på sjukdomsaktivitet och livskvalitet av en föreslagen antiinflammatorisk kost. Det var en kost rik på fullkorn, fet fisk, frukt, grönsaker, probiotika och hälsosamma fetter. Även deltagarnas vanliga energi- och näringsintag utvärderades. Maten levererades hem till patienterna, som i stort följde denna diet, det vill säga följsamheten till studiekosterna var god.
Resultaten indikerar att den föreslagna antiinflammatoriska kosten kan ge viss förbättring i sjukdomsaktivitet och fysisk funktion, framför allt hos patienter med stabil läkemedelsbehandling. Det dagliga intaget innan studiestart av mättat fett var högt, medan intaget av fiber samt flertalet vitaminer och mineraler var lågt hos dessa patienter.
Artikeln är baserad på avhandlingen Diet as a complementary therapy in Rheumatoid Arthritis – On the menu: An anti-inflammatory portfolio diet
>> text: Anna Turesson Wadell, leg. dietist, medicine doktor, Avdelningen för invärtesmedicin och klinisk nutrition, Institutionen för medicin, Sahlgrenska akademin, Göteborgs universitet, Göteborg
Reumatoid artrit
I Sverige är 0,7 procent av befolkningen drabbade av den kroniska, inflammatoriska sjukdomen reumatoid artrit, också kallad ledgångsreumatism (1). Ungefär tre fjärdedelar av de drabbade är kvinnor och de flesta insjuknar i åldern 50 till 70 år (2, 3). Inflammationen sätter sig främst i lederna, med svullnad, ömhet och stelhet som symptom. Utan behandling förstörs så småningom leden helt. Det är inte bara lederna som drabbas av inflammation. Hud, lungor och njurar är exempel på andra organ där sjukdomen kan få fäste. Patienterna löper en stor risk att även drabbas av andra sjukdomar. Hjärt-kärlsjukdom, depression och osteoporos (benskörhet) är vanligt förekommande i patientgruppen (4). Sjukdomssymtomen och samsjukligheten innebär förstås mycket besvär för patienterna, med minskad livskvalitet som följd (5).
Läkemedelsbehandlingen har utvecklats enormt de senaste decennierna och de läkemedel som idag används vid reumatoid artrit är mycket effektiva för att dämpa inflammation och förhindra leddestruktion. Trots detta upplever många patienter kvarvarande symtom (6, 7). Dessutom är biverkningar av läkemedel en av de faktorer som ligger bakom den ökade risken för andra sjukdomar (8, 9). Det finns således ett stort behov av att hitta en effektiv behandling som ett komplement till dessa läkemedel.
Kostbehandling vid reumatoid artrit
Många patienter med reumatoid artrit upplever att vissa livsmedel förbättrar deras symtom – medan andra livsmedel förvärrar dem. Det finns också indikationer på att kosten kan ha en både direkt och indirekt antiinflammatorisk verkan. Exempelvis kan omega-3-fettsyror minska produktionen av inflammatoriska eikosanoider och cytokiner (10). Fiber fungerar som bränsle till våra tarmbakterier och kan på så sätt leda till en ökad produktion av kortkedjiga fettsyror i tarmen. Detta både stärker tarmens barriär och påverkar olika immunceller (11). Det har gjorts flertalet studier på symtomlindrande effekter av hela koster, livsmedel, kostkomponenter och enskilda näringsämnen hos patienter med reumatoid artrit. Medelhavskost, vegansk kost, blåmusslor, pre- och probiotika, omega-3-fettsyror och antioxidanter är några exempel.
Ett antal av dessa studier visar på positiva resultat, men på grund av studiernas olikheter och ofta låga kvalitet är det svårt att dra några säkra slutsatser kring kostens effekter på symtom av reumatoid artrit (12). Ofta har dessutom resultaten enbart inneburit små förändringar och det är då tveksamt om förbättringen verkligen varit av klinisk relevans.
Patienterna efterfrågar ofta sjukdomsspecifika kostråd. Men enligt de riktlinjer som reumatologiska organisationer i både Europa och USA tagit fram är det endast de generella kostråden som bör rekommenderas – på grund av bristen på vetenskaplig evidens (13-15). Riktlinjerna avråder till och med från att rekommendera patienterna att följa någon specifik diet. Undantaget är medelhavskost, som verkar kunna minska smärta men framför allt är en hjärtvänlig kost (14, 15). Det är dock osäkert om kosten även har någon effekt på några andra symtom.
Upplevelsen av att specifika livsmedel förvärrar sjukdomssymtomen gör att patienterna, trots avsaknad av professionell rådgivning, utesluter livsmedel och provar olika typer av dieter på egen hand (16, 17). Dessutom leder sjukdomen för många patienter till en minskad fysisk funktion och fatigue (trötthet). Dessa faktorer kan förstås också påverka både inköp och tillagning av mat. Flera studier visar att patienternas näringsintag riskerar att bli otillräckligt (18-23).
Antiinflammatorisk kost
Åren 2017 och 2018 genomfördes interventionsstudien ADIRA – Anti-inflammatory Diet In Rheumatoid Arthritis – vid Göteborgs universitet och Sahlgrenska universitetssjukhuset i Göteborg (24). Majoriteten av de studier om kost som behandling vid reumatoid artrit gjorda tidigare har fokuserat på enskilda kostkomponenter. I ADIRA sattes flera av dessa ihop till en föreslagen antiinflammatorisk kost rik på fullkorn, fet fisk, frukt, bär, grönsaker, probiotika, och med fett av god kvalitet. I studien jämfördes den föreslagna antiinflammatoriska kosten med en kontrollkost motsvarande ett generellt svenskt näringsintag enligt Riksmaten vuxna 2010-11 (25).
ADIRA var en randomiserad crossoverstudie vilket innebar att alla deltagare åt båda kosterna och de slumpades till vilken kost de skulle börja med. Varje kost åts under tio veckor, och mellan de två studiekosterna ingick en washoutperiod (mellanperiod) där deltagarna åt precis som vanligt under 2 till 5 månader. Under båda kostperioderna levererades mat motsvarande hälften av intaget – frukost, en huvudmåltid och ett mellanmål – fem dagar i veckan hem till deltagarna veckovis och helt utan kostnad. Menyn bestod av färdiga eller väldigt lättlagade maträtter. För övriga måltider instruerades deltagarna att äta på ett liknande sätt. I studien ingick 50 deltagare med reumatoid artrit, alla boendes i Göteborgsområdet. Ungefär tre fjärdedelar av deltagarna var kvinnor, medianåldern var 63 år och mer än hälften hade övervikt eller obesitas (26).
Kosten i denna intervention innehöll mycket fullkorn från havre och vete, lax, rapsolja, frukt, bär, grönsaker, probiotikaberikad juiceshot, a-fil, och en måttlig mängd magra mejeriprodukter. Det innebar att kosten var rik på fiber (inklusive prebiotika), omega-3-fetter, probiotika, vitamin D, selen och andra antioxidanter. Alla kostkomponenter hade i tidigare studier visat olika grad av symtomlindring var för sig, men aldrig studerats i den här kombinationen.
Hur ett näringsämne bryts ned, tas upp och används i kroppen påverkas av flera faktorer. Således är effekten av ett isolerat näringsämne sannolikt olik den man får när olika näringsämnen och kostkomponenter kombineras (27). Hypotesen var att de olika kostkomponenterna i kombination skulle stärka varandra i sina symtomlindrande egenskaper.
Kostdagböcker, intervjuer och biomarkörer i plasma/serum visade att deltagarna i ADIRA-studien följde kosterna i studien (28). Detta gällde framför allt instruktionerna om intag av fullkorn, fisk och skaldjur, matlagningsfett och rött kött. Kostdagböckerna visade också att deltagarnas intag av frukt- och grönsaker följde instruktionerna. Däremot visade de biomarkörer som användes i studien, karotenoider, på motsatsen. Förklaringen är att de frukter som deltagarna fick under perioden med interventionskost inte är särskilt rika på karotenoider, medan tomatbaserade rätter och juice under kontrollkostperioden innehåller en stor mängd karotenoider. Slutsatsen drogs ändå att det generellt var en mycket god följsamhet till studiekosterna.
Sjukdomsaktivitet mättes som Disease Activity Score-28 (DAS28) – ett vedertaget sätt att mäta hur aktiv patienternas sjukdom är. (29). Det är också det mått som används mest i klinik och forskning. Måttet innefattar ett inflammationsmått (sänka eller C-reaktivt protein, CRP), antal ömma och antal svullna leder av sammanlagt 28, samt patientens bedömning av sin hälsa på en visuell analog skala (VAS). Tillsammans ger dessa ett värde mellan 0 och 9,4. Mindre än 2,6 innebär en mildare form av sjukdomen (30). Ett DAS28 på mer än 5,1 visar på en hög sjukdomsaktivitet (31). Alla deltagarna i ADIRA-studien hade vid start en aktiv sjukdom. Hos drygt hälften var sjukdomsaktiviteten måttlig medan 9 procent av deltagarna hade en hög sjukdomsaktivitet.
Den föreslagna antiinflammatoriska kosten gav viss förbättring av sjukdomen. I huvudanalyserna, där alla deltagare som genomfört minst en av kostperioderna ingick, var DAS28 lägre efter interventionsperioden jämfört med kontrollperioden (medelskillnad: -0,29) men skillnaden var inte statistiskt signifikant (P=0,12) (26). Det var däremot skillnaden inom interventionsperioden.
DAS28 minskade alltså under perioden med den föreslagna antiinflammatoriska kosten. I ojusterade analyser sågs en statistiskt signifikant skillnad även mellan kostperioderna (P=0,04). I sensitivitetsanalyser där endast deltagare som inte gjort några ändringar i sina anti-reumatiska läkemedel ingick (n=25) var skillnaden mellan perioderna något större och trots att antalet deltagare inkluderade i analysen var betydligt färre sågs här en trend till statistisk signifikans (P=0,07).
Det gjordes även en analys där endast de deltagare som inte påbörjat någon ny eller som helt avslutat en anti-reumatisk behandling ingick (n=38). Skillnaden i DAS28 mellan kostperioderna var då större och statistiskt signifikant (medelskillnad: -0,49, P=0,009) (32). En skillnad i DAS28 på 0,6 bedöms vara en klinisk relevant förändring i sjukdomsaktivitet (33).
Slutsatsen är att de förbättringar som identifierades i ADIRA-studien anses vara ganska små – och det är svårt att säga hur värdefulla de är för den enskilda individen.
Den föreslagna antiinflammatoriska kosten ledde även till viss förbättring i fysisk funktion. I ADIRA-studien ingick instrument som mäter olika aspekter av hälsorelaterad livskvalitet: 36-item Short Form Survey (SF-36), Health Assessment Questionnaire (HAQ), VAS för smärta, trötthet och stelhet, samt en skala för hur länge morgonstelhet varade.
Inga skillnader sågs i huvudanalyserna, men fysisk funktion mätt med SF-36 förbättrades under perioden med interventionskost. När endast deltagare med stabil läkemedelsbehandling ingick i analysen (n=25) var även skillnaden mellan perioderna statistiskt signifikant (medelskillnad: 7,9, P=0,036) (34).
Näringsintag
Alla deltagare i ADIRA-studien, inklusive de som exkluderades vid screeningbesöket, ombads skriva en 3-dagars kostdagbok innan de påbörjade studiens första kostperiod. Dessa kostdagböcker, tillsammans med 3-dagars kostdagböcker från washoutperioden, när deltagarna skulle äta precis som de brukar, användes för att utvärdera deltagarnas vanliga intag av energi och näring.
Totalt 44 deltagare skrev två kostdagböcker och registrerade således sitt intag under 6 dagar, och 18 deltagare bidrog med en kostdagbok (35). Medianintaget av energi var 1711 kcal/dag för kvinnorna och 2154 kcal/dag för männen. Intaget av mättat fett var över det rekommenderade intaget på ≥10 energiprocent (E%) för 95 procent av deltagarna. Nio av tio nådde inte upp till rekommendationerna om ≥25 gram fiber om dagen. Medianintaget av flertalet vitaminer och mineraler var lägre än rekommenderat intag. Särskilt lågt var intaget av vitamin D där 82 procent av kvinnorna och 75 procent av männen inte nådde upp till genomsnittsbehovet. Även intaget av tiamin var lågt, framför allt hos männen där 67 procent låg under genomsnittsbehovet. Ungefär hälften av männen fick inte heller i sig genomsnittsbehovet av riboflavin eller vitamin A.
Det är viktigt att komma ihåg att ADIRA-studien endast inkluderade deltagare som till vardags äter en blandad kost. Skälet till detta urval var att studiekosterna var blandkoster som innehöll både kött, fisk och mejeriprodukter. Koststudier har dessutom en tendens att attrahera personer med ett visst kostintresse som också har en mer hälsosam livsstil. Det kan också mycket väl vara så att näringsintaget är ännu sämre bland patienter med reumatoid artrit som inte ingick i studien, där både sjukare patienter, vegetarianer och andra som äter specialkost samt mindre kostintresserade patienter ingår.
Den ökade risken för både hjärt-kärlsjukdom och osteoporos innebär också att det är särskilt viktigt för dessa patienter att äta en näringstät kost med hälsosam fettkvalitet.
Slutsats
Den föreslagna antiinflammatoriska kosten i ADIRA, som var rik på fullkorn, fet fisk, frukt, grönsaker, probiotika och fett av god kvalitet, verkar kunna ge viss förbättring av sjukdomen och fysisk funktion hos patienter med reumatoid artrit.
Framtida studier bör inkludera andra populationer med reumatoid artrit, undersöka långtidseffekterna och utvärdera hur väl kostbehandlingen fungerar i den verkliga kliniska verksamheten där patienter inte kan få kostnadsfri mat hemlevererad utan endast kostråd. I dagsläget finns inte tillräckligt med evidens för att rekommendera patienter med reumatoid artrit någon specifik kost för symtomlindring utan de hänvisas till de generella kostråden. Undantaget är medelhavskost som möjligtvis kan minska smärta. Den kan framför allt rekommenderas i syfte att minska risken för hjärt-kärlsjukdom.
Patienter med reumatoid artrit i denna studie hade ett otillräckligt näringsintag. Intaget av mättat fett var högt medan intaget av fiber och flertalet vitaminer och mineraler var lågt. Många hade dessutom övervikt eller obesitas. Detta talar för att dietisten har en viktig roll i patienternas behandling. En dietist kan individanpassa kostråd för att optimera näringsintag, vid behov stötta till viktnedgång och möjligtvis även lindra sjukdomssymtom. Detta skulle sannolikt kunna minska risken för samsjuklighet i patientgruppen.
Författaren uppger inga jävsförhållanden.
Referenser
1. Neovius M, Simard JF, Askling J. Nationwide prevalence of rheumatoid arthritis and penetration of disease-modifying drugs in Sweden. Ann Rheum Dis. 2011;70(4):624-9.
2. Myasoedova E, Davis J, Matteson EL, Crowson CS. Is the epidemiology of rheumatoid arthritis changing? Results from a population-based incidence study, 1985-2014. Ann Rheum Dis. 2020;79(4):440-4.
3. Eriksson JK, Neovius M, Ernestam S, Lindblad S, Simard JF, Askling J. Incidence of Rheumatoid Arthritis in Sweden: A Nationwide Population‐Based Assessment of Incidence, Its Determinants, and Treatment Penetration. Arthritis Care Res (Hoboken). 2013;65(6):870-8.
4. Hill J, Harrison J, Christian D, Reed J, Clegg A, Duffield SJ, et al. The prevalence of comorbidity in rheumatoid arthritis: a systematic review and meta-analysis. Br J Community Nurs. 2022;27(5):232-41.
5. Matcham F, Scott IC, Rayner L, Hotopf M, Kingsley GH, Norton S, et al. The impact of rheumatoid arthritis on quality-of-life assessed using the SF-36: A systematic review and meta-analysis. Semin Arthritis Rheum. 2014;44(2):123-30.
6. Druce KL, Bhattacharya Y, Jones GT, Macfarlane GJ, Basu N. Most patients who reach disease remission following anti-TNF therapy continue to report fatigue: results from the British Society for Rheumatology Biologics Register for Rheumatoid Arthritis. Rheumatology (Oxford). 2016;55(10):1786-90.
7. Altawil R, Saevarsdottir S, Wedren S, Alfredsson L, Klareskog L, Lampa J. Remaining Pain in Early Rheumatoid Arthritis Patients Treated With Methotrexate. Arthritis Care Res (Hoboken). 2016;68(8):1061-8.
8. Taylor PC, Atzeni F, Balsa A, Gossec L, Müller-Ladner U, Pope J. The Key Comorbidities in Patients with Rheumatoid Arthritis: A Narrative Review. J Clin Med. 2021;10(3).
9. Ashai S, Harvey NC. Rheumatoid arthritis and bone health. Clin Med (Lond). 2020;20(6):565-7.
10. Calder PC. Mechanisms of action of (n-3) fatty acids. J Nutr. 2012;142(3):592s-9s.
11. Sidhu SRK, Kok CW, Kunasegaran T, Ramadas A. Effect of Plant-Based Diets on Gut Microbiota: A Systematic Review of Interventional Studies. Nutrients. 2023;15(6).
12. Turk MA, Liu Y, Pope JE. Non-pharmacological interventions in the treatment of rheumatoid arthritis: A systematic review and meta-analysis. Autoimmun Rev. 2023:103323.
13. Gwinnutt JM, Wieczorek M, Balanescu A, Bischoff-Ferrari HA, Boonen A, Cavalli G, et al. 2021 EULAR recommendations regarding lifestyle behaviours and work participation to prevent progression of rheumatic and musculoskeletal diseases. Ann Rheum Dis. 2023;82(1):48-56.
14. England BR, Smith BJ, Baker NA, Barton JL, Oatis CA, Guyatt G, et al. 2022 American College of Rheumatology Guideline for Exercise, Rehabilitation, Diet, and Additional Integrative Interventions for Rheumatoid Arthritis. Arthritis Rheumatol. 2023.
15. Daien C, Czernichow S, Letarouilly JG, Nguyen Y, Sanchez P, Sigaux J, et al. Dietary recommendations of the French Society for Rheumatology for patients with chronic inflammatory rheumatic diseases. Joint Bone Spine. 2022;89(2):105319.
16. Salminen E, Heikkilä S, Poussa T, Lagström H, Saario R, Salminen S. Female Patients Tend to Alter Their Diet Following the Diagnosis of Rheumatoid Arthritis and Breast Cancer. Prev Med. 2002;34(5):529-35.
17. Grygielska J, Klak A, Raciborski F, Manczak M. Nutrition and quality of life referring to physical abilities – a comparative analysis of a questionnaire study of patients with rheumatoid arthritis and osteoarthritis. Reumatologia. 2017;55(5):222-9.
18. Andersson J, Gustafsson K, Fjellström C, Sidenvall B, Nydahl M. Five-day food intake in elderly female outpatients with Parkinson’s disease, rheumatoid arthritis or stroke. J Nutr Health Aging. 2004;8(5):414-21.
19. Gomez-Vaquero C, Nolla JM, Fiter J, Ramon JM, Concustell R, Valverde J, et al. Nutritional status in patients with rheumatoid arthritis. Joint Bone Spine. 2001;68(5):403-9.
20. Berube LT, Kiely M, Yazici Y, Woolf K. Diet quality of individuals with rheumatoid arthritis using the Healthy Eating Index (HEI)-2010. Nutr Health. 2017;23(1):17-24.
21. Comee L, Taylor CA, Nahikian-Nelms M, Ganesan LP, Krok-Schoen JL. Dietary patterns and nutrient intake of individuals with rheumatoid arthritis and osteoarthritis in the United States. Nutrition. 2019;67-68:110533.
22. Bae S-C, Kim S-J, Sung M-K. Inadequate Antioxidant Nutrient Intake and Altered Plasma Antioxidant Status of Rheumatoid Arthritis Patients. J Am Coll Nutr. 2003;22(4):311-5.
23. Hejazi J, Mohtadinia J, Kolahi S, Bakhtiyari M, Delpisheh A. Nutritional status of Iranian women with rheumatoid arthritis: an assessment of dietary intake and disease activity. Womens Health (Lond). 2011;7(5):599-605.
24. Winkvist A, Bärebring L, Gjertsson I, Ellegård L, Lindqvist HM. A randomized controlled cross-over trial investigating the effect of anti-inflammatory diet on disease activity and quality of life in rheumatoid arthritis: the Anti-inflammatory Diet In Rheumatoid Arthritis (ADIRA) study protocol. Nutr J. 2018;17(1):44.
25. Amcoff E, Edberg A, Enghardt Barbieri H, Lindroos AK, Nälsén C, Pearson M, et al. Riksmaten – vuxna 2010-11. Livsmedels- och näringsintag bland vuxna i Sverige. [Internet]. Uppsala: Livsmedelsverket; 2012.
26. Vadell AKE, Bärebring L, Hulander E, Gjertsson I, Lindqvist HM, Winkvist A. Anti-inflammatory Diet In Rheumatoid Arthritis (ADIRA)-a randomized, controlled crossover trial indicating effects on disease activity. Am J Clin Nutr. 2020;111(6):1203-13.
27. Jacobs DR, Jr., Gross MD, Tapsell LC. Food synergy: an operational concept for understanding nutrition. Am J Clin Nutr. 2009;89(5):1543s-8s.
28. Wadell AT, Bärebring L, Hulander E, Gjertsson I, Landberg R, Lindqvist H, et al. Dietary biomarkers and food records indicate compliance to study diets in the ADIRA (Anti-inflammatory Diet In Rheumatoid Arthritis) trial. Front Nutr. 2023;10:1209787.
29. Canhão H, Rodrigues AM, Gregório MJ, Dias SS, Melo Gomes JA, Santos MJ, et al. Common Evaluations of Disease Activity in Rheumatoid Arthritis Reach Discordant Classifications across Different Populations. Front Med (Lausanne). 2018;5:40.
30. van Riel PLCM. The development of the disease activity score (DAS) and the disease activity score using 28 joint counts (DAS28). Clin Exp Rheumatol. 2014;32(5 Suppl 85):S.
31. van Gestel AM, Haagsma CJ, van Riel PL. Validation of rheumatoid arthritis improvement criteria that include simplified joint counts. Arthritis Rheum. 1998;41(10):1845-50.
32. Hulander E. Nutritional impact on health in patients with Rheumatoid Arthritis. Borås: University of Gothenburg; 2022.
33. Sköldstam L, Hagfors L, Johansson G. An experimental study of a Mediterranean diet intervention for patients with rheumatoid arthritis. Ann Rheum Dis. 2003;62(3):208-14.
34. Turesson Wadell A, Bärebring L, Hulander E, Gjertsson I, Hagberg L, Lindqvist HM, et al. Effects on health-related quality of life in the randomized, controlled crossover trial ADIRA (Anti-inflammatory Diet In Rheumatoid Arthritis). PLoS One. 2021;16(10):e0258716.
35. Turesson Wadell A, Bärebring L, Hulander E, Gjertsson I, Lindqvist HM, Winkvist A. Inadequate Dietary Nutrient Intake in Patients With Rheumatoid Arthritis in Southwestern Sweden: A Cross-Sectional Study. Front Nutr. 2022;9:915064.
Obesitas – så säger forskningen om medicinsk behandling
Hörnstenarna i obesitasbehandling är förändringar av matvanor, fysisk aktivitet och beteenden. Till denna behandlingsgrund kan läkemedel och obesitaskirurgi läggas till som verktyg. Obesitasbehandling ska genomföras inom ramen för en tydlig struktur och samtliga delar måste vara evidensbaserade var och en för sig och sammantagna. På så sätt blir förväntningarna tydliga och behandlingen säker. Denna översikt belyser evidensen bakom medicinsk (utan kirurgi) obesitasbehandling med fokus på nutritionens roll. Längre fram kommer vi att publicera en översikt om läkemedel som stöd för viktminskning.
>> text: Ingrid Larsson, näringsfysiolog, docent, universitetssjukhusöverdietist, Enheten för klinisk nutrition och Regionalt obesitascentrum, Sahlgrenska universitetssjukhuset, Göteborg
Under de senaste fyra decennierna har förekomsten av obesitas ökat i Sverige och i världen, utan att några åldersgrupper har varit förskonade (1, 2). Det går inte att peka på en avgörande faktor som ensam är anledningen till den ökande och höga förekomsten (3). Obesitas är en multifaktoriell sjukdom, det vill säga att många faktorer bidrar till förekomsten. Det finns också flera hundra varianter av gener som är associerade med obesitas och som vardera ger ett litet bidrag till kroppsvikten (3). Om det finns gott om energität och välsmakande mat lättillgängligt och om en stillasittande tillvaro gynnas, så ökar dessa genvarianter risken för att utveckla obesitas.
Den vanligaste formen av obesitas kallas polygen obesitas (3). Den andra formen, monogen form av obesitas, är ytterst ovanlig. Den genetiska effekten vid monogen form av obesitas är stor och gendefekten interagerar inte med omgivningen (3). Ett exempel på monogen obesitas är den som orsakas av leptinbrist (4, 5). Leptinbrist innebär att personen saknar mättnadskänsla trots att fettmassan är stor och ökar på grund av högt energiintag. Regelbundna injektioner av leptin leder till återvunnen mättnadskänsla, att energiintaget och vikten minskar (5).
Reglering av energibalansen – en fråga om dynamik
Energibalansen, det vill säga balansen mellan energiintag och energiomsättning styrs av en homeostatisk reglering, av en hedonisk reglering och av psykologiska aspekter på regleringen av energibalansen (6-9). Den homeostatiska regleringen av energibalansen är en dynamisk process (10). Med homeostas menas att mekanismer verkar tillsammans för att något ska hålla sig stabilt trots förändringar. När det sker en förändring av energiintaget påverkas mättnadshormoner så att man antingen blir mer hungrig eller mindre hungrig för att återställa energibalansen. Centralt i den homeostatiska regleringen av energibalansen är att man äter när man är hungrig för att upprätthålla kroppens energikrävande funktioner (11).
I den homeostatiska regleringen av energibalansen ingår bland andra mättnadshormonerna leptin från fettvävnaden och insulin från bukspottskörteln (11). Om en obalans mellan energiintag och energiomsättning upprätthålls över tid kan man upptäcka att den dynamiska processen är ojämn i sin återställning av energibalansen. Människan är genetiskt konstruerad så det sker en mer kraftfull korrigering för att återställa en viktminskning än att dämpa en viktökning (10).
Den hedoniska (av grekiskans hedoni, lust) regleringen av energibalansen innebär att man äter trots att man inte är hungrig. Hedonisk reglering av energibalansen kan sätta sig över den homeostatiska regleringen om det finns god tillgång på energität, välsmakande mat med hög hedonisk verkan (7, 9). Ingen biologisk broms har identifierats som hindrar oss att äta när det finns gott om mat (12). Sverige och resten av västvärlden kännetecknas av mycket god tillgång på mat med hög hedonisk verkan. Maten är energität, den är välsmakande, den säljs oftast i stora förpackningar och den är relativt billig. Samhällen med god tillgång på sådan mat i kombination med att en stillasittande tillvaro gynnas kallas för obesogena samhällen (12).
Psykologiska aspekter av ätandet interagerar både med den homeostatiska och den hedoniska regleringen av energibalansen (13). Det betyder exempelvis att känslostyrt ätande kan ge en omedelbar kraftfull och positiv effekt av tillfredsställelse – för att sedan övergå till negativa känslor: ”Detta borde jag inte ha ätit!”.
Syfte med obesitasbehandling
Det övergripande syftet med evidensbaserad obesitasbehandling är riskreduktion genom att minska nivåer av riskmarkörer för sjukdomar som hög blodsockernivå, höga insulinnivåer, höga nivåer av blodfetter samt högt blodtryck. När nivåerna av riskmarkörer sjunker minskas risken över tid för obesitasrelaterad sjukdom. I ett mycket långt tidsperspektiv har obesitasbehandling också som syfte att minska risken för förtidig död. En ökad livskvalitet är också ett av obesitasbehandlingens syften, inte minst ökad rörlighet i vardagen som oftast upplevs positivt. Viktminskning medför också behov av färre läkemedel för högt blodtryck och underlättar behandling av typ 2-diabetes. Samtliga syften med obesitasbehandling uppnås genom viktminskning.
Viktminskning – centralt i obesitasbehandlingen
Viktminskning är fundamental i obesitasbehandlingen därför att den direkt påverkar obesitasrelaterade riskmarkörer och därmed sjukdomsrisk. Fettmassans storlek är en av de viktigaste förklaringarna till varför obesitas är relaterat till flera sjukdomar (14), då det i fettmassan produceras inflammationsmarkörer som ingår i den låggradiga inflammationen som är central för obesitassjukdomen. Ju större fettmassa desto högre koncentrationer av inflammationsmarkörer i blodet relaterade till sjukdomar som hjärt-kärlsjukdom, typ 2-diabetes och vissa cancerformer. (15). Vid viktminskning reduceras nivåerna av inflammationsmarkörer.
Riskerna med långvarig obesitas är höga eller mycket höga. Det finns teorier om att vissa personer med obesitas har en ”hälsosam form” av sjukdomen (16). Men forskningen har visat att en sådan form inte finns. Det hjälper inte med hälsosamma levnadsvanor, som att äta flera portioner grönsaker och frukt dagligen, vara rökfri, ha en låg konsumtion av alkohol och vara dagligt fysiskt aktiv (17). Med bibehållen obesitas över tid ökar i alla fall risken för bland annat metabola syndromet, diabetes (18, 19), hjärt-kärlsjukdom (20, 21), död i hjärt-kärlsjukdom, hjärtsvikt, död i hjärtsvikt och respiratoriska sjukdomar (20).
Rutinmässiga blodprover vid ”hälsosam obesitas” som visar på normala nivåer av vanliga riskmarkörer, fångar inte upp den metabola påverkan (16, 22, 23). Personer med ”hälsosam obesitas” har även lägre livskvalitet (22). Personer med obesitas med normala nivåer av riskmarkörer bör därför erbjudas behandling (16).
Viktminskning – att uppnå energibalans vid en lägre vikt
För att minska i vikt måste energiintaget vara lägre än energiförbrukningen över tid, en negativ energibalans. Skillnaden mellan energiintag och energiförbrukning bör vara så pass stor att man får en mätbar viktminskning på en till två veckors tid. Det finns några sätt att reducera energiintaget på:
• 30 procent reduktion från det dagliga energibehovet för viktstabilitet
• Reducera det dagliga energiintaget med 500 till 1000 kcal
• Ha ett specificerat energiintag på en viss nivå (23):
1200 – 1500 kcal per dag för de flesta kvinnor
1500 – 1800 kcal per dag för de flesta män
Rekommendationen vid obesitas utan etablerad samsjukdom är att äta inom ramen för energiintagsreduktionen och enligt de rekommendationer för hälsosamma matvanor som finns för befolkningen i stort då de matvanorna är relaterade till sänkt risk för hjärt-kärlsjukdom (24). Har man en etablerad sjukdom som typ 2-diabetes, högt blodtryck eller hjärt-kärlsjukdom följer man aktuella kostrekommendationer för respektive sjukdom.
Det viktigaste – och samtidigt det mest utmanande – med obesitasbehandling är att behålla den lägre vikten under lång tid. För detta krävs både att hålla fast vid en nivå på energiintaget anpassad till den lägre vikten – och att de nya matvanorna passar in i vardagen. Detta i kombination med andra levnadsvanor relaterade till kroppsvikten, exempelvis daglig fysisk aktivitet.
I nationella och internationella behandlingsriktlinjer av obesitas understryks vikten av stöd inom ramen för en strukturerad behandling och uppföljning (25-28). Det betyder att riktlinjerna tydliggör det omfattande arbete den enskilde individen behöver göra för att förändra sina levnadsvanor och sin livsstil för en bibehållen lägre vikt över lång tid.
Nutritionens roll i obesitasbehandling
Nutritionens roll i obesitasbehandlingen har tre övergripande syften:
• bidra till att minska energiintaget
• säkerställa optimalt näringsämnesintag
• bidra till generell hälsa och minskad sjukdomsrisk
Ett fjärde mer specifikt syfte bör synliggöras inom obesitasbehandlingen: vikten av att bli mätt av de nya matvanorna.
Utan negativ energibalans sker ingen viktminskning. En varierad kost inom ramen för hälsosamma matvanor säkerställer ett optimalt intag av makronutrienter (kolhydrater, protein och fetter) och mikronutrienter (vitaminer och mineraler). De nordiska näringsrekommendationerna (24) framhåller näringstäta kostmönster såsom medelhavskost och liknande kostmönster. Dessa har en bred så väl som djup vetenskaplig evidensbas som visar på att de innehåller tillräckligt med näringsämnen samt att kosten främjar hjärt-kärlhälsan genom sitt varierade livsmedelsinnehåll.
Hälsosamma livsmedelsval enligt nordiska rekommendationerna (24) är:
Större andel av:
grönsaker, rotfrukter, baljväxter
frukt och bär
fullkornsbröd och -mjöl samt -gryn
magra mejeriprodukter
fisk och skaldjur
fågel och ägg
vegetabiliska oljor och matfetter
nötter, mandel och frön
Mindre andel av:
rött kött och charkuterier
sötsaker, bakverk och snacks
sockersötade drycker
salt
alkohol*

Hälsosamma livsmedelsval medför inte automatiskt lägre vikt (29). Det finns livsmedelsgrupper med mycket hög energitäthet – vegetabiliska oljor och matfetter, nötter, mandel och frön – bland de livsmedel som vi är rekommenderade att äta en större andel av vilket tydliggör vikten av att begränsa portionerna i obesitasbehandling.
Tallriksmodellen är ett väletablerat verktyg för att få hälsosamma proportioner på grönsaker, kolhydratrika och proteinrika livsmedel i en måltid men det är fortfarande energiinnehållet i maten och energibehovet för viktminskning som bestämmer portionsstorleken.
Under flera decennier har man studerat om en viss sammansättning av protein, fett och kolhydrater ger större viktminskning jämfört med någon annan (30). Ingen kostsammansättning har identifierats kunna ge större viktminskning än någon annan. Det är graden av viktminskning och följsamheten till denna som leder till viktminskning (30).
Lågenergipulverdrycker
Vid obesitas kan måltidsersättning användas för att minska intaget av energi. Det innebär att en till två måltider per dag byts ut mot en portion lågenergipulverdryck, som man antingen blandar själv eller är drickfärdig eller mot en så kallad måltidsbar (31). Med hjälp av måltidsersättning inom ramen för en strukturerad obesitasbehandling kan en omfattande viktminskning behållas över lång tid (32).
Studier visar att en komplett kostersättning som använts i strikta perioder, framför allt i början av behandlingen, ger gynnsamma effekter på vikt, HbA1c (”långtidsblodsocker”) och även remission i typ 2-diabetes (som innebär att HbA1c hålls på en önskvärd nivå utan mediciner) (33, 34). Komplett kostersättning vid obesitasbehandling ingår i internationella rekommendationer för behandling av typ 2-diabetes (35) och i en systematisk litteratursökning om mat vid diabetes från Statens beredning för medicinisk och social utvärdering (36). Användning av lågenergipulverdrycker som komplett kostersättning vid obesitasbehandling måste i sin tur ske inom ramen av ett strukturerat behandlingsprogram med noggrann uppföljning. Det är inte en behandling att göra på egen hand, utan medicinsk kontakt, inte minst om man har andra sjukdomar förutom obesitas.
Bibehållen viktminskning över tid – att nå en lägre body weight set-point
Teorin bakom body weight set-point (det saknas en svensk översättning) är att den färdigväxta människan har ”sin egen” kroppsvikt med små variationer runt denna (37). Senare års forskning föreslår att fettmassan varierar inom ett område med en nedre nivå och en övre nivå så att man snarare kan prata om en ”settling point (37, 38).
Vid homeostatisk reglering av energibalansen leder ett ökat energiintag till en ökad mättnadssignalering som resulterar i ett sänkt energiintag och energibalansen återtas (10). Vid viktminskning sker den motsatta signaleringen, ökad aptit samt signalering för att hämma nedbrytning av energireserven i fettvävnaden. Resultatet är ökat energiintag och återställd energibalans och vikt (10).
Den homeostatiska regleringen av energibalansen sker när energiintaget varierar inom begränsade gränser, det vill säga när man håller vikten över tid. Den homeostatiska regleringen fungerar bäst när det finns ”lagom” tillgång på energi och när man behöver upprätthålla en viss nivå av fysisk aktivitet för att klara vardagen.
För att nå och behålla en större viktminskning, exempelvis 10 procent lägre vikt, behöver energiintaget vara konsekvent reducerat över tid. När man nått den lägre vikten ska energiintaget återigen variera inom ett nytt begränsat intervall. Viktminskningen leder också till en minskad viloomsättning (energiförbrukningen i vila) eftersom en viss andel muskler och annan fettfri massa försvinner (39). Därför spelar den dagliga fysiska aktiviteten en viktig roll för att bibehålla en viktminskning över tid.
Vid bibehållen viktminskning, som kräver minskat energiintag, är nivån av grehlin (hungerhormon) fortsatt förhöjd, precis som den subjektiva hungern (39-41). Mättnadshormonerna (exempelvis PYY, GLP-1 och CCK) skiljer sig inte över tid jämfört med nivåerna före viktminskning. I studier där man funnit reducerade nivåer av mättnadshormoner efter initial viktminskning har deltagarna varit i positiv energibalans och ökat i vikt (40). Studier visar att hos personer som har kunnat behålla en omfattande viktminskning över tid skiljer sig inte mättnadshormonerna från före viktminskning, mättnaden har ökat och den subjektiva önskan om att äta har dämpats (41-44).
Slutsatsen av de senaste årens studier är att regleringen av aptit och mättnadskänsla inte direkt svarar på viktminskning men anpassar sig mot en lägre vikt (45, 46). Det är viktigt att förstå att aptitökningen vid omfattande viktminskning varierar i styrka mellan individer (44). En del känner inte alls av någon aptitökning, andra känner av en måttlig och hanterbar aptitökning. En tredje grupp får en svårbemästrad aptitökning. Det är till denna grupp som aptitdämpande läkemedel kan vara aktuella.
Varför ökar så många människor i vikt efter en viktminskning? Det finns många orsaker såsom psykologiska, sociala, ärftliga – och faktorer i omgivningen som interagerar med varandra och med fysiologin (13). Om vi endast koncentrerar oss på de fysiologiska mekanismerna, är den huvudsakliga orsaken en positiv energibalans som upprätthåller aptiten och underlättar viktökning efter initial viktminskning.
I praktiken är man som mest sårbar för viktökning när man just har minskat mycket i vikt. Det är då det är avgörande att hålla fast vid det reducerade energiintaget och den dagliga fysiska aktiviteten. Det går inte att ”äta lite extra för att det går så bra med viktminskningen” eller att ”äta som vanligt” som före viktminskningen. Resultatet blir ett ökat energiintag och viktökning. När energiintaget hålls nere och den dagliga fysiska aktiviteten fortsätter kommer aptit- och mättnadsregleringen att anpassas till den nya lägre vikten – som med tiden blir etablerad och det nya normala.
Den fysiologiska regleringen av kroppsvikten visar på vikten av ett långsiktigt stöd. Det kan också behövas verktyg, inte minst läkemedel som dämpar aptiten och ökar mättnadskänslan.
Kunskapen och förståelsen för den fysiologiska regleringen av vikten har ökat. Men det innebär inte att det blivit lättare för den enskilde individen. Därför är det viktigt med flera verktyg till den grundläggande behandlingen med matvaneförändringar, fysisk aktivitet och beteendeförändringar.
Referenser
1. Folkhälsomyndigheten. Statistik om övervikt och fetma hos vuxna 2022. Available from: https://www.folkhalsomyndigheten.se/livsvillkor-levnadsvanor/mat-fysisk-aktivitet-overvikt-och-fetma/overvikt-och-fetma/statistik-om-overvikt-och-fetma/overvikt-och-fetma-hos-vuxna/.
2. Collaboration NCDRF. Worldwide trends in underweight and obesity from 1990 to 2022: a pooled analysis of 3663 population-representative studies with 222 million children, adolescents, and adults. Lancet. 2024;403(10431):1027-50.
3. Loos RJF, Yeo GSH. The genetics of obesity: from discovery to biology. Nat Rev Genet. 2022;23(2):120-33.
4. Zhang Y, Proenca R, Maffei M, Barone M, Leopold L, Friedman JM. Positional Cloning Of the Mouse Obese Gene and Its Human Homologue. Nature. 1994;372:425-32.
5. Farooqi S, O’Rahilly S. Genetics of obesity in humans. Endocr Rev. 2006;27(7):710-18.
6. Hussain SS, Bloom SR. The regulation of food intake by the gut-brain axis: implications for obesity. Int J Obes (Lond). 2013;37(5):625-33.
7. Egecioglu E, Skibicka KP, Hansson C, Alvarez-Crespo M, Friberg PA, Jerlhag E, et al. Hedonic and incentive signals for body weight control. Rev Endocr Metab Disord. 2011;12(3):141-51.
8. Lutter M, Nestler EJ. Homeostatic and hedonic signals interact in the regulation of food intake. J Nutr. 2009;139(3):629-32.
9. Lee PC, Dixon JB. Food for Thought: Reward Mechanisms and Hedonic Overeating in Obesity. Curr Obes Rep. 2017;6(4):353-61.
10. Seeley RJ, Woods SC. Monitoring of stored and available fuel by the CNS: implications for obesity. Nat Rev Neurosci. 2003;4(11):901-9.
11. Lowe MR, Butryn ML. Hedonic hunger: a new dimension of appetite? Physiol Behav. 2007;91(4):432-9.
12. Lund J, Lund C, Morville T, Clemmensen C. The unidentified hormonal defense against weight gain. PLoS Biol. 2020;18(2):e3000629.
13. Bluher M. Obesity: global epidemiology and pathogenesis. Nat Rev Endocrinol. 2019;15(5):288-98.
14. Heymsfield SB, Wadden TA. Mechanisms, Pathophysiology, and Management of Obesity. N Engl J Med. 2017;376(15):1492.
15. Hotamisligil GS. Inflammation and metabolic disorders. Nature. 2006;444(7121):860-7.
16. Bluher M. Metabolically Healthy Obesity. Endocr Rev. 2020;41(3).
17. Heath L, Jebb SA, Aveyard P, Piernas C. Obesity, metabolic risk and adherence to healthy lifestyle behaviours: prospective cohort study in the UK Biobank. BMC Med. 2022;20(1):65.
18. Hsu TL, Tantoh DM, Chou YH, Hsu SY, Ho CC, Lung CC, et al. Association between osteoporosis and menopause in relation to SOX6 rs297325 variant in Taiwanese women. Menopause. 2020;27(8):887-92.
19. Wei Y, Wang J, Han X, Yu C, Wang F, Yuan J, et al. Metabolically healthy obesity increased diabetes incidence in a middle-aged and elderly Chinese population. Diabetes Metab Res Rev. 2020;36(1):e3202.
20. Zhou Z, Macpherson J, Gray SR, Gill JMR, Welsh P, Celis-Morales C, et al. Are people with metabolically healthy obesity really healthy? A prospective cohort study of 381,363 UK Biobank participants. Diabetologia. 2021;64(9):1963-72.
21. Kramer CK, Zinman B, Retnakaran R. Are metabolically healthy overweight and obesity benign conditions?: A systematic review and meta-analysis. Ann Intern Med. 2013;159(11):758-69.
22. Lopez-Garcia E, Guallar-Castillon P, Garcia-Esquinas E, Rodriguez-Artalejo F. Metabolically healthy obesity and health-related quality of life: A prospective cohort study. Clin Nutr. 2017;36(3):853-60.
23. Almandoz JP, Wadden TA, Tewksbury C, Apovian CM, Fitch A, Ard JD, et al. Nutritional considerations with antiobesity medications. Obesity (Silver Spring). 2024.
24. Blomhoff R, Andersen, R., Arnesen, E.K., Christensen, J.J., Eneroth, H., Erkkola, M., Gudanaviciene, I., Halldorsson, T.I., Høyer-Lund, A., Lemming, E.W., Meltzer, H.M., Pitsi, T., Schwab, U., Siksna, I., Thorsdottir, I., Trolle, E. Nordic nutrition rcommendations 2023. Copenhagen: Nordic Council of Ministers; 2023.
25. Yumuk V, Tsigos C, Fried M, Schindler K, Busetto L, Micic D, et al. European Guidelines for Obesity Management in Adults. Obes Facts. 2015;8(6):402-24.
26. Hassapidou M, Vlassopoulos A, Kalliostra M, Govers E, Mulrooney H, Ells L, et al. European Association for the Study of Obesity Position Statement on Medical Nutrition Therapy for the Management of Overweight and Obesity in Adults Developed in Collaboration with the European Federation of the Associations of Dietitians. Obes Facts. 2023;16(1):11-28.
27. Raynor HA, Morgan-Bathke M, Baxter SD, Halliday T, Lynch A, Malik N, et al. Position of the Academy of Nutrition and Dietetics: Medical Nutrition Therapy Behavioral Interventions Provided by Dietitians for Adults With Overweight or Obesity, 2024. J Acad Nutr Diet. 2024;124(3):408-15.
28. Socialstyrelsen. Nationella riktlinjer för vård vid obesitas. Prioriteringsstöd till beslutsfattare och chefer. Stockholm; 2023.
29. Hjelmesaeth J, Sjoberg A. Human body weight, nutrients, and foods: a scoping review. Food Nutr Res. 2022;66.
30. Yannakoulia M, Poulimeneas D, Mamalaki E, Anastasiou CA. Dietary modifications for weight loss and weight loss maintenance. Metabolism. 2019;92:153-62.
31. Heymsfield SB. Meal replacements and energy balance. Physiol Behav. 2010;100(1):90-4.
32. Look ARG. Eight-year weight losses with an intensive lifestyle intervention: the look AHEAD study. Obesity (Silver Spring). 2014;22(1):5-13.
33. Lean MEJ, Leslie WS, Barnes AC, Brosnahan N, Thom G, McCombie L, et al. Durability of a primary care-led weight-management intervention for remission of type 2 diabetes: 2-year results of the DiRECT open-label, cluster-randomised trial. Lancet Diabetes Endocrinol. 2019;7(5):344-55.
34. Taheri S, Zaghloul H, Chagoury O, Elhadad S, Ahmed SH, El Khatib N, et al. Effect of intensive lifestyle intervention on bodyweight and glycaemia in early type 2 diabetes (DIADEM-I): an open-label, parallel-group, randomised controlled trial. Lancet Diabetes Endocrinol. 2020;8(6):477-89.
35. Diabetes, Nutrition Study Group of the European Association for the Study of D. Evidence-based European recommendations for the dietary management of diabetes. Diabetologia. 2023;66(6):965-85.
36. SBU. Mat vid diabetes. En systematisk litteraturöversikt. Statens beredning för medicinsk och social utvärdering; 2022.
37. Speakman JR, Hall KD. Models of body weight and fatness regulation. Philos Trans R Soc Lond B Biol Sci. 2023;378(1888):20220231.
38. Geary N. Control-theory models of body-weight regulation and body-weight-regulatory appetite. Appetite. 2020;144:104440.
39. Doucet E, Imbeault P, St-Pierre S, Almeras N, Mauriege P, Despres JP, et al. Greater than predicted decrease in energy expenditure during exercise after body weight loss in obese men. Clin Sci (Lond). 2003;105(1):89-95.
40. Sumithran P, Prendergast LA, Delbridge E, Purcell K, Shulkes A, Kriketos A, et al. Long-term persistence of hormonal adaptations to weight loss. N Engl J Med. 2011;365(17):1597-604.
41. Melby CL, Paris HL, Foright RM, Peth J. Attenuating the Biologic Drive for Weight Regain Following Weight Loss: Must What Goes Down Always Go Back Up? Nutrients. 2017;9(5).
42. Nymo S, Coutinho SR, Eknes PH, Vestbostad I, Rehfeld JF, Truby H, et al. Investigation of the long-term sustainability of changes in appetite after weight loss. Int J Obes (Lond). 2018;42(8):1489-99.
43. Nymo S, Coutinho SR, Jorgensen J, Rehfeld JF, Truby H, Kulseng B, et al. Timeline of changes in appetite during weight loss with a ketogenic diet. Int J Obes (Lond). 2017;41(8):1224-31.
44. Nymo S, Coutinho SR, Rehfeld JF, Truby H, Kulseng B, Martins C. Physiological Predictors of Weight Regain at 1-Year Follow-Up in Weight-Reduced Adults with Obesity. Obesity (Silver Spring). 2019;27(6):925-31.
45. Martins C, Dutton GR, Hunter GR, Gower BA. Revisiting the Compensatory Theory as an explanatory model for relapse in obesity management. Am J Clin Nutr. 2020;112(5):1170-9.
46. Martins C, Gower BA, Hill JO, Hunter GR. Metabolic adaptation is not a major barrier to weight-loss maintenance. Am J Clin Nutr. 2020;112(3):558-65.
Därför är frukt och grönt så nyttigt
Ett högt intag av frukt och grönt tycks skydda mot flera av våra vanliga sjukdomar. Det finns flera möjliga förklaringar, som alla troligen spelar en roll. Frukt och grönt är generellt näringstäta livsmedel med lågt energiinnehåll och innehåller många viktiga vitaminer och mineraler. De består också av olika slags kostfibrer som har en rad gynnsamma effekter på hälsan. De innehåller även tusentals så kallade fytokemikalier som potentiellt har en betydande inverkan på hälsan via många olika mekanismer. Det återstår ännu mycket att kartlägga inom detta område.
>>text: Magdalena Rosell, nutritionist, docent, Institutionen för biovetenskaper och näringslära, Karolinska Institutet, Stockholm
Frukt och grönt tycks skydda mot en rad sjukdomar
De flesta känner till att det är nyttigt att äta mycket frukt och grönt och detta påstående stärks ytterligare i de nya nordiska näringsrekommendationerna 2023 (NNR2023) (1). Det finns idag stark evidens för att ett högt intag av grönsaker, frukt och bär skyddar mot en rad sjukdomar, som cancer i magsäck och lunga, hjärt- och kärlsjukdom och en förtidig död. Svagare effekter har observerats för typ 2-diabetes. Det finns också studier som visar på skyddande effekter mot osteoporos, depression, kognitiva störningar och skörhet hos äldre (2).
Det vetenskapliga underlaget utgörs till stor del av observationsstudier, som inkluderar studier av biomarkörer för frukt och grönt. Men även interventionsstudier bidrar till underlaget (2). En ytterligare viktig del i det vetenskapliga underlaget är studier som undersöker de bakomliggande biologiska mekanismerna för sambanden. Nedan följer en överblick över forskningen om hur grönsaker, frukt och bär påverkar hälsan.
Möjliga mekanismer
Lågt energiinnehåll
Även om grönsaker, frukt och bär är en heterogen livsmedelsgrupp ur näringssynpunkt, innehåller de vanligtvis mycket vatten och lite energi. Morötter, äpplen, grönkål, broccoli, spenat, och aubergine består till 90 procent av vatten och energiinnehållet ligger på omkring 40 kcal per 100 gram. Även fetare grönsaker, som avokado och oliver, innehåller 70 till 80 procent vatten och i runda tal 200 respektive 130 kcal per 100 gram. Skillnaden mot godis och snacks är stor. Vatteninnehållet i choklad och kex utgör endast några få procent och energiinnehållet ligger på närmare 500 kcal per 100 gram.
Mycket vatten och lågt energiinnehåll skulle kunna leda till ett minskat totalt energiintag och därmed bidra till en bättre kontroll av kroppsvikt. Epidemiologiska studier ger ett visst stöd för detta, men underlaget är här osäkert (3, 4). Mer intressant är effekter som är direkt kopplade till olika ämnen i frukt och grönt.
Fibrer
Gemensamt för grönsaker, frukt och bär och även andra livsmedelsgrupper från växtriket är att de innehåller kostfibrer av olika slag, som har en rad dokumenterade hälsoeffekter (5). Lösliga och viskösa fibrer binder vatten, vilket ökar volymen och leder till långsammare magtömning. Detta kan i sin tur bidra till en bibehållen mättnadsnivå och minskad höjning av glukos och fetter i blodet efter måltider (5).
Kostfibrer fermenteras av bakterier i tjocktarmen. Det gäller i synnerhet de lösliga fibrerna och resistent stärkelse. Resistent stärkelse som står emot nedbrytningen i tunntarmen finns bland annat i kall kokt potatis. I fermenteringsprocessen produceras en betydande mängd kortkedjiga fettsyror, ungefär 20 gram per dag, som i hög grad absorberas i tjocktarmen (5). De mest vanliga fettsyrorna är smörsyra (butyrat), propionsyra (propionat) och ättiksyra (acetat).
Smörsyra har främst en lokal effekt genom att binda till olika receptorer i tjocktarmens ytskikt och påverkar därigenom processer i cellerna på ett gynnsamt sätt som till exempel cellreparation. Dessa mekanismer utgör viktiga pusselbitar till varför intag av fibrer till exempel kan minska risken för tjocktarmscancer (5).
Propionsyra och ättiksyra distribueras i större utsträckning ut i kroppen. De används som energi av hjärnan, muskler och lever. De kan också påverka energibalans och aptitreglering genom mekanismer som bland annat involverar hypotalamus och centrala nervsystemet (5).
Olösliga fibrer fermenteras inte i lika hög grad och har i stället en bulkeffekt. Det innebär att de ökar volymen, vilket gör att innehållet passerar tarmkanalen snabbare. Detta minskar tiden för möjliga cancerogena ämnen att påverka tarmen och skulle på så sätt kunna minska risken för utveckling av cancer (5). Fibrer kan även påverka upptaget av fetter och proteiner. Detta medför att återabsorptionen av gallsyror i tunntarmen minskar, vilket är en av huvudförklaringarna till att fibrer sänker halten av kolesterol i blodet (5). Intaget av fiber påverkar även tarmflorans sammansättning och främjar bland annat tillväxten av gynnsamma bakterier, ökar motståndskraften mot patogena bakterier och förbättrar tarmbarriärens funktion (5, 6).
Det finns mer att kartlägga om hur olika typer av kostfibrer påverkar vår hälsa. De flesta studier på mekanismerna är gjorda på djur, men randomiserade studier på människor över längre tid ger stöd till att lösliga fibrer har gynnsamma effekter på blodfetter och inflammatoriska markörer (7). Sammantaget finns det mycket som stödjer att fibrer, bland annat från frukt och grönt, kan skydda mot sjukdomar som obesitas, typ 2-diabetes, hjärt- och kärlsjukdomar och tjock- och ändtarmscancer (1, 5).
Vitaminer och mineraler
Forskning visar också att hälsoeffekterna av grönsaker, frukt och bär kan bero på innehållet av vissa näringsämnen som också fungerar som antioxidanter, som vitamin E, vitamin C, β‑karoten, selen, zink – och även andra näringsämnen som folat (8). Randomiserade kontrollerade studier som har undersökt effekter av tillskott av olika vitaminer och mineraler har dock generellt inte lyckats med att påvisa skyddande effekter på hjärt- och kärlsjukdom, diabetes eller cancer hos friska människor utan kliniska bristsymptom (8, 9). Negativa effekter har i vissa fall påvisats för cancersjukdomar, främst tillskott av β‑karoten och risk för lungcancer hos rökare eller tidigare rökare (9, 10). Världscancerfonden avråder idag från att använda kosttillskott för att förebygga cancer (10). Sammantaget tyder detta på att hälsoeffekterna av grönsaker, frukt och bär troligen inte kan förklaras av enskilda näringsämnen, utan av en kombination av olika substanser som samverkar med varandra.
Fytokemikalier
Förutom de etablerade näringsämnena innehåller vegetabiliska livsmedel tusentals andra bioaktiva föreningar, så kallade fytokemikalier. Dessa inkluderar fenoler, alkaloider, karotenoider, svavelhaltiga föreningar, kvävehaltiga föreningar och fytosteroler (11). Fenoler är den största gruppen och innefattar bland annat fenolsyror, flavonoider, lignaner, kumariner och stilbener. Gruppen flavonoider kan i sin tur delas in en rad undergrupper (11).
Fytokemikalierna har främst uppmärksammats på grund av sina starka antioxidativa egenskaper och de skulle därmed kunna spela en viktig roll i förebyggandet och behandlingen av många kroniska sjukdomar (12, 13). Studier in vitro och in vivo har även visat att de verkar antiinflammatoriskt och antimikrobiellt och kan motverka uppkomsten av cancer och obesitas (14-17). De föreslagna mekanismerna är mångfaldiga och innefattar förutom antioxidativa effekter, även effekter på enzymaktiviteter, signalvägar och genuttryck.
Resveratrol är en fytokemikalie som har studerats mycket. Den ingår i gruppen stilbener och finns bland annat i bär, vindruvor och jordnötter (13). Metaanalyser av studier där man har gett tillskott av resveratrol till människor med metabola och/eller inflammatoriska sjukdomar, indikerar gynnsamma effekter på exempelvis inflammation, blodtryck, kroppsvikt och reglering av blodsocker (13). Men effekterna av resveratrol är små och det vetenskapliga underlaget osäkert. Höga doser av vissa antioxidanter eller fytokemikalier skulle också kunna ha skadliga effekter. Observationsstudier visar dock generellt att en växtbaserad kost rik på antioxidanter och fytokemikalier är förknippad med en minskad risk för kroniska sjukdomar kopplade till oxidativ stress (13).
Den stora mångfalden av fytokemikalier bidrar inte bara till det färggranna utseendet hos grönsaker, frukt och bär utan också till de varierande möjliga hälsofrämjande egenskaperna hos olika undergrupper av dessa livsmedel. Korsblommiga grönsaker, som broccoli, brysselkål, kål, blomkål, grönkål och rovor har bland annat uppmärksammats på grund av sitt höga innehåll av organiska svavelföreningar och den möjliga effekten att kunna motverka cancer (11). Gröna bladgrönsaker som spenat, mangold och sallad är rika på karotenoider och flavonoider (11). Gula, orangea och röda grönsaker som tomat, morot, pumpa och gul och röd paprika innehåller också mycket karotenoider, medan lökgrönsaker som lök, vitlök och purjolök karaktäriseras av ett högt innehåll av organiska svavelföreningar och flavonoider (11).
Frukter är också rika på flavonoider (18) och särskilt citrusfrukter har ett högt innehåll av bland annat alkaloider, kumariner och limonoider (19). Bär som blåbär, jordgubbar, björnbär och tranbär, innehåller mycket flavonoider, inklusive antocyaniner, ellagitanniner och fenolsyror (20, 21).
Observationsstudier ger ett visst stöd för att korsblommiga grönsaker, gröna bladgrönsaker, lökgrönsaker, äpplen och päron, och citrusfrukter kan vara särskilt hälsofrämjande, medan gynnsamma effekter av bär har främst visats i interventionsstudier (2).
En stor del av fytokemikalierna är fortfarande okända och kunskapen om deras biotillgänglighet, bioaktivitet och hur de interagerar med varandra är begränsad (22). Tarmfloran spelar också in, eftersom bakterierna producerar enzymer som kan bryta ner fytokemikalier och underlätta deras absorption (13).
Sammanfattning
Det finns flera möjliga mekanismer som skulle kunna förklara de gynnsamma effekterna av att äta mycket frukt och grönt. Denna livsmedelsgrupp innehåller generellt mycket näring och vatten, kombinerat med lite energi. De är rika på olika slags kostfibrer som har en rad dokumenterade gynnsamma effekter. Förutom att bidra med många viktiga vitaminer och mineraler, innehåller de också en mångfald av fytokemikalier, vars upptag, samverkan och inverkan på hälsan i stor utsträckning återstår att kartlägga.
Det finns dock mycket som tyder på att dessa ämnen, tillsammans med fibrer, spelar en viktig roll för hälsan. Det finns indikationer på att vissa grupper av grönsaker, frukt och bär kan ha särskilt gynnsamma effekter. Men underlaget är idag inte tillräckligt starkt för att ge mer specifika råd. Rekommendationen i NNR2023 är därför att äta olika sorters grönsaker, frukt och bär, totalt 500 till 800 gram per dag eller mer (1). Betydelsen av fibrer betonas särskilt.
Referenser
1. Blomhoff R, Andersen R, Arnesen EK, Christensen, J.J., Eneroth H, et al. Nordic Nutrition Recommendations 2023. Copenhagen: Nordic Council of Ministers; 2023.
2. Rosell M, Fadnes LT. Vegetables, fruits, and berries – a scoping review for Nordic Nutrition Recommendations 2023. Food Nutr Res. 2024;68.
3. Nour M, Lutze SA, Grech A, Allman-Farinelli M. The Relationship between Vegetable Intake and Weight Outcomes: A Systematic Review of Cohort Studies. Nutrients. 2018;10(11).
4. Schlesinger S, Neuenschwander M, Schwedhelm C, Hoffmann G, Bechthold A, Boeing H, et al. Food Groups and Risk of Overweight, Obesity, and Weight Gain: A Systematic Review and Dose-Response Meta-Analysis of Prospective Studies. Adv Nutr. 2019;10(2):205-18.
5. Carlsen H, Pajari AM. Dietary fiber – a scoping review for Nordic Nutrition Recommendations 2023. Food Nutr Res. 2023;67.
6. Fuller S, Beck E, Salman H, Tapsell L. New Horizons for the Study of Dietary Fiber and Health: A Review. Plant Foods Hum Nutr. 2016;71(1):1-12.
7. Soliman GA. Dietary Fiber, Atherosclerosis, and Cardiovascular Disease. Nutrients. 2019;11(5).
8. Alissa EM, Ferns GA. Dietary fruits and vegetables and cardiovascular diseases risk. Crit Rev Food Sci Nutr. 2017;57(9):1950-62.
9. Zhang FF, Barr SI, McNulty H, Li D, Blumberg JB. Health effects of vitamin and mineral supplements. BMJ. 2020;369:m2511.
10. International WCRF. Cancer prevention recommendations https://www.wcrf.org/ [accessed 2024-04-29]
11. Blekkenhorst LC, Sim M, Bondonno CP, Bondonno NP, Ward NC, Prince RL, et al. Cardiovascular Health Benefits of Specific Vegetable Types: A Narrative Review. Nutrients. 2018;10(5).
12. Zhang YJ, Gan RY, Li S, Zhou Y, Li AN, Xu DP, et al. Antioxidant Phytochemicals for the Prevention and Treatment of Chronic Diseases. Molecules. 2015;20(12):21138-56.
13. Myhrstad MCW, Wolk A. Antioxidants and phytochemicals – a scoping review for Nordic Nutrition Recommendations 2023. Food Nutr Res. 2023;67.
14. Barbieri R, Coppo E, Marchese A, Daglia M, Sobarzo-Sánchez E, Nabavi SF, et al. Phytochemicals for human disease: An update on plant-derived compounds antibacterial activity. Microbiol Res. 2017;196:44-68.
15. Zhu F, Du B, Xu B. Anti-inflammatory effects of phytochemicals from fruits, vegetables, and food legumes: A review. Crit Rev Food Sci Nutr. 2018;58(8):1260-70.
16. Ranjan A, Ramachandran S, Gupta N, Kaushik I, Wright S, Srivastava S, et al. Role of Phytochemicals in Cancer Prevention. Int J Mol Sci. 2019;20(20).
17. Ahmad B, Friar EP, Vohra MS, Garrett MD, Serpell CJ, Fong IL, et al. Mechanisms of action for the anti-obesogenic activities of phytochemicals. Phytochemistry. 2020;180:112513.
18. Gayer BA, Avendano EE, Edelson E, Nirmala N, Johnson EJ, Raman G. Effects of Intake of Apples, Pears, or Their Products on Cardiometabolic Risk Factors and Clinical Outcomes: A Systematic Review and Meta-Analysis. Curr Dev Nutr. 2019;3(10):nzz109.
19. Lv X, Zhao S, Ning Z, Zeng H, Shu Y, Tao O, et al. Citrus fruits as a treasure trove of active natural metabolites that potentially provide benefits for human health. Chem Cent J. 2015;9:68.
20. Nile SH, Park SW. Edible berries: bioactive components and their effect on human health. Nutrition. 2014;30(2):134-44.
21. Govers C, Berkel Kasikci M, van der Sluis AA, Mes JJ. Review of the health effects of berries and their phytochemicals on the digestive and immune systems. Nutr Rev. 2018;76(1):29-46.
22. Phan MAT, Paterson J, Bucknall M, Arcot J. Interactions between phytochemicals from fruits and vegetables: Effects on bioactivities and bioavailability. Crit Rev Food Sci Nutr. 2018;58(8):1310-29.
Graviditeten – en unik möjlighet att främja kvinnors hälsa och välmående
En stor andel kvinnor har övervikt och obesitas vid graviditetens start och ungefär hälften av gravida kvinnor i Sverige går upp mer i vikt än rekommenderat av internationella riktlinjer. Detta är oroande eftersom både ett för högt BMI och en för hög viktuppgång under graviditeten ökar risken för negativa konsekvenser på hälsan, som till exempel graviditetsdiabetes, kejsarsnitt och hög födelsevikt. Risken ökar även för övervikt senare i livet hos såväl mor som barn. Det behövs alltså insatser för att motverka denna trend, insatser som går att anpassa efter olika förutsättningar och som samtidigt är kostnadseffektiva.
Ett exempel på en framgångsrik insats för att stävja den oroande trenden och som utgör ett komplement till rådande mödrahälsovård är det digitala verktyget HealthyMoms, en livsstilsintervention tillhandahållen i appformat, som utvärderats i en randomiserad kontrollerad studie. Studien visade positiva effekter på kostvanor och viktökning hos 305 gravida kvinnor och har nu potential att implementeras i rutinmässig mödrahälsovård.
>>text: Johanna Sandborg, PhD, Postdoktoral forskare, Institute of Physical Activity and Nutrition, Deakin University, Melbourne, Australien och Marie Löf, Professor i nutrition, Institutionen för Biovetenskaper och Näringslära, Karolinska Institutet, Stockholm
Förekomst och risker
Övervikt och obesitas är idag ett stort folkhälsoproblem, både globalt och nationellt (1). De senaste årtiondens utveckling visar på en oroväckande trend med ökad förekomst av övervikt och obesitas i stort sett i alla åldersgrupper och Socialstyrelsens prognos visar inga tecken på att utvecklingen håller på att avstanna (1). Detta är oroväckande ur flera aspekter eftersom övervikt och obesitas innebär en ökad risk för framtida ohälsa för den enskilde och därmed också ett ökat tryck på den svenska sjukvården.
Så många som 45 procent av gravida kvinnor i Sverige hade övervikt eller obesitas vid inskrivningsbesöket i mödravården år 2021 (2). Detta är oroande eftersom övervikt och obesitas innebär en ökad risk för komplikationer under graviditeten, exempelvis graviditetsdiabetes och havandeskapsförgiftning, och under förlossningen till exempel kejsarsnitt. Riskerna ökar också för bebisen, till exempel prematur födsel och hög födelsevikt (3, 4). Förutom vikten innan graviditet har viktuppgången under graviditeten en betydande roll. Både en för låg och en för hög viktuppgång ökar riskerna för ovannämnda komplikationer. Dessutom ökar risken för övervikt senare livet hos både mamma och barn (5, 6).
En svensk studie som undersökte förekomsten av ohälsosamt BMI och viktuppgång samt sambandet med graviditetskomplikationer hos en halv miljon kvinnor visade att så mycket som 30-50 procent gick upp för mycket och 14-35 procent gick upp för lite i vikt under graviditeten (7). Viktigt att notera är att 60 procent av de normalviktiga kvinnorna gick upp för mycket i vikt. Detta visar på betydelsen av att främja en hälsosam viktuppgång hos alla kvinnor – oavsett BMI innan graviditet.
Orsaker och insatser
Den grundläggande orsaken till övervikt och obesitas är en obalans i energiintag och energiåtgång, alltså följden av ett ökat intag av energirika livsmedel och en mer stillasittande livsstil (8). Insatser för att främja en mer hälsosam livsstil och därmed motverka övervikt och obesitas samt främja en hälsosam viktuppgång under graviditet behöver ske på flera nivåer.
Mödravården har en central roll för gravidas välmående (9) och för att ge stöd för en hälsosam viktuppgång (10). En stor utmaning är att mödravården ofta har begränsade resurser och tid (11), däribland för att främja hälsosamma levnadsvanor hos kvinnor med annat modersmål än svenska (12), och barnmorskor vittnar om svårigheter att diskutera vikt med sina patienter(13).
Interventioner riktade till den gravida kvinnan och som kan ges kontinuerligt under hela graviditeten har potential att överkomma dessa hinder och underlätta sjukvårdspersonalens uppdrag att främja en hälsosam graviditet. Den här typen av insatser med fokus på en hälsosam kost och fysisk aktivitet på individnivå har visat sig minska risken för en för hög viktuppgång under graviditet (10, 14, 15) medan andra insatser inte har haft någon effekt (16-18). Majoriteten av tidigare livsstilsinterventioner under graviditeten har varit mycket resurs- och personalkrävande och därmed haft begränsad möjlighet att nå ut storskaligt.
Under de senaste årtiondena har användningen av digital teknik, som mobilappar, blivit en alltmer vanlig metod för att tillhandahålla livsstilsinterventioner. Några fördelar med det digitala formatet är större räckvidd och tillgänglighet. Tekniken ger också möjlighet till mer individanpassat innehåll, till exempel olika språk. Dagens gravida kvinnor är vana appanvändare och användning av kommersiella appar för att följa graviditeten samt mäta vikt och kost är idag vanligt förekommande (19-21). Med andra ord representerar det en möjlighet att nå ut med kunskapsunderlag och kontinuerligt stöd till en större massa för att på så sätt främja en hälsosam livsstil och viktuppgång under graviditeten.
Komplement i mödravården
Vi har nyligen genomfört en randomiserad kontrollerad studie i Region Östergötland (22-24). Syftet var att undersöka om en sex månader lång livsstilsintervention via en app – HealthyMoms kunde vara ett stöd för en hälsosam viktuppgång under graviditeten (23). Totalt 305 kvinnor rekryterades via mödrahälsovården i Region Östergötland. Kvinnornas kost, fysiska aktivitet, vikt, kroppssammansättning (fett och fettfri massa), kondition och muskelstyrka mättes i tidig (graviditetsvecka 14) och sen graviditet (graviditetsvecka 37).
Efter det första mättillfället delades kvinnorna upp slumpmässigt till antingen kontroll- eller interventionsgrupp. Kontrollgruppen fick enbart standardvård medan interventionsgruppen även fick tillgång till HealthyMoms. Nära 90 procent (271/305) av kvinnorna återkom i graviditetsvecka 37. Resultaten från studien visade en positiv effekt på kvinnornas kostvanor. Kvinnor med ett pre-gravid BMI över 25 (övervikt eller obesitas) i interventionsgruppen hade dessutom en lägre viktuppgång, i genomsnitt ~1,7 kg lägre jämfört med kontrollgruppen.
Detta är lovande resultat då traditionella mer resurskrävande interventioner rapporterat liknande resultat (10). HealthyMoms var också uppskattad av kvinnorna som använde den i stor utsträckning. Innehållet uppfattades som trovärdigt och värdefullt med användbara funktioner och relevant information (24). HealthyMoms har även stor potential att vara ett värdefullt verktyg för arabisktalande och somalisktalande kvinnor (12).
Sammantaget visar resultaten från studien att HealthyMoms kan vara ett stöd för hälsosamma vanor och viktuppgång under graviditeten. Nästa steg för HealthyMoms är att göra den tillgänglig för fler genom att implementera den i rutinmässig mödrahälsovård. HealthyMoms är också grunden till systerprojekten SPARK och HealthyMoms4MentalHealth, där digitala stöd för behandling av graviditetsdiabetes och främjande av mental hälsa hos gravida utvärderas i pågående forskningsprojekt.
Referenser
1. Övervikt och fetma – Folkhälsomyndigheten. Accessed September 21, 2023. https://www.folkhalsomyndigheten.se/livsvillkor-levnadsvanor/mat-fysisk-aktivitet-overvikt-och-fetma/overvikt-och-fetma/
2. Socialstyrelsen. Statistik Om Graviditeter, Förlossningar Och Nyfödda Barn 2021. 2022. Accessed October 19,2022. https://www.socialstyrelsen.se/globalassets/sharepointdokument/artikelkatalog/statistik/2022-12-8275.pdf
3. Santos S, Voerman E, Amiano P, et al. Impact of maternal body mass index and gestational weight gain on pregnancy complications: an individual participant data meta-analysis of European, North American and Australian cohorts. BJOG An Int J Obstet Gynaecol. 2019;126(8):984-995. doi:10.1111/1471-0528.15661
4. Voerman E, Santos S, Golab BP, et al. Maternal body mass index, gestational weight gain, and the risk of overweight and obesity across childhood: An individual participant data meta-analysis. PLoS Med. 2019;16(2). doi:10.1371/journal.pmed.1002744
5. Voerman E, Santos S, Inskip H, et al. Association of Gestational Weight Gain With Adverse Maternal and Infant Outcomes. JAMA. 2019;321(17):1702-1715. doi:10.1001/jama.2019.3820
6. Goldstein RF, Abell SK, Ranasinha S, et al. Association of gestational weight gain with maternal and infant outcomes: A systematic review and meta-analysis. JAMA – J Am Med Assoc. 2017;317(21):2207-2225. doi:10.1001/jama.2017.3635
7. Henriksson P, Sandborg J, Blomberg M, et al. Body mass index and gestational weight gain in migrant women by birth regions compared with Swedish-born women: A registry linkage study of 0.5 million pregnancies. PLoS One. 2020;15(10):e0241319. doi:10.1371/journal.pone.0241319
8. World Health Organization. Obesity and overweight. Published June 9, 2021. Accessed September 27, 2021. https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight
9. The Royal Australian and New Zealand College of Obstetricians, and Gynaecologists (RANZCOG). Maternity Care in Australia. 2017. Accessed February 9, 2023. http://ranzcog.edu.au/wp-content/uploads/2022/01/Maternity-Care-in-Australia-Web.pdf
10. Teede HJ, Bailey C, Moran LJ, et al. Association of Antenatal Diet and Physical Activity-Based Interventions With Gestational Weight Gain and Pregnancy Outcomes: A Systematic Review and Meta-analysis. JAMA Intern Med. 2022;182(2):106-114. doi:10.1001/JAMAINTERNMED.2021.6373
11. Alexandrou C, Müssener U, Thomas K, Henriksson H, Löf M. Adapting a Parental Support App to Promote Healthy Diet and Physical Activity Behaviors (MINISTOP) for a Multi-Ethnic Setting: A Qualitative Study on the Needs and Preferences of Parents and Nurses within Swedish Child Health Care. Nutrients. 2021;13(7). doi:10.3390/NU13072190
12. Söderström E, Müssener U, Löfgren M, Sandell L, Thomas K, Löf M. Healthcare Professionals Perceptions of Promoting Healthy Lifestyle Behaviors in Pregnant Migrant Women and the Potential of a Digital Support Tool-A Qualitative Study. Int J Environ Res Public Health. 2022;19(4). doi:10.3390/IJERPH19042328
13. Christenson A, Torgerson J, Hemmingsson E. Attitudes and beliefs in Swedish midwives and obstetricians towards obesity and gestational weight management. BMC Pregnancy Childbirth. 2020;20(1). doi:10.1186/S12884-020-03438-1
14. Shieh C, Cullen DL, Pike C, Pressler SJ. Intervention strategies for preventing excessive gestational weight gain: systematic review and meta-analysis. Obes Rev. 2018;19(8):1093-1109. doi:10.1111/obr.12691
15. Morison PN, Bacardi-Gascon M, Lopez-Corrales M, Jimenez-Cruz A. Combined dietary-exercise intervention for gestational weight gain and birthweight: A meta-analysis. Asia Pac J Clin Nutr. 2018;27(4):860-868. doi:10.6133/apjcn.112017.02
16. Ronnberg AK, Ostlund I, Fadl H, Gottvall T, Nilsson K. Intervention during pregnancy to reduce excessive gestational weight gain – A randomised controlled trial. BJOG An Int J Obstet Gynaecol. 2015;122(4):537-544. doi:10.1111/1471-0528.13131
17. Dodd JM, Deussen AR, Louise J. A randomised trial to optimise gestational weight gain and improve maternal and infant health outcomes through antenatal dietary, lifestyle and exercise advice: The OPTIMISE randomised trial. Nutrients. 2019;11(12). doi:10.3390/nu11122911
18. Kunath J, Günther J, Rauh K, et al. Effects of a lifestyle intervention during pregnancy to prevent excessive gestational weight gain in routine care – the cluster-randomised GeliS trial. BMC Med. 2019;17(1):5. doi:10.1186/s12916-018-1235-z
19. Hughson JAP, Oliver Daly J, Woodward-Kron R, Hajek J, Story D. The rise of pregnancy apps and the implications for culturally and linguistically diverse women: Narrative review. JMIR mHealth uHealth. 2018;6(11):e189. doi:10.2196/mhealth.9119
20. O’higgins A, Murphy OC, Egan A, Mullaney L, Sheehan S, Turner MJ. The use of digital media by women using the maternity services in a developed country. Ir Med J. 2014;107(10).
21. Wang N, Deng Z, Wen LM, Ding Y, He G. Understanding the use of smartphone apps for health information among pregnant Chinese women: Mixed methods study. J Med Internet Res. 2019;21(6):e12631. doi:10.2196/12631
22. Henriksson P, Sandborg J, Blomberg M, et al. A smartphone app to promote healthy weight gain, diet, and physical activity during pregnancy (HealthyMoms): Protocol for a randomized controlled trial. JMIR Res Protoc. 2019;8(3). doi:10.2196/13011
23. Sandborg J, Söderström E, Henriksson P, et al. Effectiveness of a Smartphone App to Promote Healthy Weight Gain, Diet, and Physical Activity During Pregnancy (HealthyMoms): Randomized Controlled Trial. JMIR mHealth uHealth. 2021;9(3):e26091. doi:10.2196/26091
24. Sandborg J, Henriksson P, Larsen E, et al. Participants’ Engagement and Satisfaction With a Smartphone App Intended to Support Healthy Weight Gain, Diet, and Physical Activity During Pregnancy: Qualitative Study Within the HealthyMoms Trial. JMIR mHealth uHealth. 2021;9(3):e26159. doi:10.2196/26159
Den livsviktiga och livsfarliga maten från sensoriskt och holistiskt perspektiv – kan smaken vara ett problem?
I sex decennier har mat varit mitt stora intresse och centralt i mitt yrke.
Fortsätt läsa Den livsviktiga och livsfarliga maten från sensoriskt och holistiskt perspektiv – kan smaken vara ett problem?
Nutritionsfakta lanserar rapport om processade livsmedel
Den 25 maj lanserade Nutritionsfakta rapporten Processade livsmedel i samband med ett seminarium vid Örebro universitet.
Fortsätt läsa Nutritionsfakta lanserar rapport om processade livsmedel
Seminarium om processade livsmedel den 25 maj
Nutritionsfakta bjuder in till seminarium om processade livsmedel. Seminariet sker i samband med lansering av den vetenskapliga rapporten ”Processade livsmedel”. Hoppas vi ses!
Datum: torsdagen den 25 maj
Tid: kl 13-16
Plats: hörsal P2, Prismahuset, Örebro universitet
Program
Moderator: Marie Brodin, Kommunikation och samverkan, Örebro universitet
- Inledning
- Varför processar man livsmedel? Andreas Håkansson, Livsmedelsteknik, Lunds universitet
- Hur påverkar processning livsmedels näringsinnehåll och biotillgänglighet? Inger-Cecilia Mayer Labba, Livsmedelsvetenskap och nutrition, Chalmers
- Klassificeringssystem med syfte att mäta grad av processning. Cecilia Nälsén, Nutritionsfakta, Örebro universitet
- Vilka samband finns mellan klassificeringssystemen och hälsoeffekter? Yan Borné, Nutritionsepidemiologi, Lunds universitet
- Paneldiskussion med:
Susanne Bryngelsson, Hållbar nutrition, RISE
Ulrika Ericson, Nutritionsepidemiologi, Lunds universitet
Filippa Juul, Global Public Health, New York University
Vi bjuder på fika under eftermiddagen.
Länk till anmälan. Sista anmälningsdag: 22 maj.
Hitta hit: https://www.oru.se/om-universitetet/hitta-hit/
Kontaktperson: Cecilia Nälsén, cecilia.nalsen@oru.se
Varmt välkomna!
Uppdaterade nordiska näringsrekommendationer är ute på remiss
Nu finns möjlighet för forskare och andra intresserade att lämna synpunkter på förslaget till nya näringsrekommendationer, NNR, fram till den 26 maj 2023.
Några förändringar sedan förra utgåvan är till exempel att mer grönsaker, frukt och bär rekommenderas, minst 500-800 gram per dag och mindre rött kött, max 350 gram i veckan. Den minskade köttkonsumtionen bör ersättas med baljväxter och andra växtbaserade livsmedel.
Det rekommenderade intaget för flera vitaminer och mineraler har ändrats något, exempelvis för vitamin B12 och järn. Tillsatt socker omfattar nu även så kallat fritt socker som sockerarter från juice och honung.
De nya nordiska näringsrekommendationerna kommer att publiceras den 20 juni 2023.
Kraftig ökning av vikt hos 4-åringar under pandemin visar ny studie
Notis
Övervikt och obesitas ökade bland 4-åringar under covid-19-pandemins första år 2020. Det visar resultatet av en omfattande nationell studie av forskare vid Uppsala universitet som nyligen publicerats.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
I studien deltog 200 000 4-åringar från 18 av Sveriges 21 regioner. Barnhälsovården mätte vikt och längd i samband med 4-årsbesöket 2018 och 2020. Resultaten visade att förekomsten av övervikt och obesitas var högre under pandemins första år 2020 jämfört med 2018. Andelen med övervikt och obesitas av 4-åringarna var 11,4 procent 2018 och ökade till 13,3 procent 2020. Liknande resultat har man också sett i studier från andra länder.
Ökningen från 2018 till 2020 var särskilt stor för obesitas, 32 procent, medan ökningen för övervikt var 13 procent. Fler flickor än pojkar hade övervikt eller obesitas 2018 men ökningen från 2018 till 2020 var större bland pojkarna – 21 procent – än bland flickorna – 14 procent.
Skillnad mellan regionerna
Viktökningen varierade i regionerna, men i 13 av 18 regioner sågs en ökning av övervikt och obesitas. Orsakerna till att resultaten skiljer sig i olika delar av Sverige – och mellan flickor och pojkar – är oklara.
Forskarna konstaterar att ökningen av övervikt och obesitas bland barn kräver snabba generella och riktade insatser inom både vård och i hela samhället.
Vad är en hållbar kost?
Notis
Inspelning från seminarium 9 november 2022
Nyligen arrangerades ett seminarium med titeln ”What is a sustainable diet? The protein shift – challenges and opportunities”. På seminariet presenterades och diskuterades näringsmässiga, miljömässiga och politiska aspekter av att producera växtbaserade proteiner och livsmedel. Här finns möjlighet att ta del av det inspelade seminariet från IVA:s webbplats: https://www.iva.se/event/what-is-a-sustainable-diet/
Seminariet arrangerades av Kungliga Ingenjörsvetenskapsakademien (IVA) Avdelning 10 Bioteknik, Kungliga Skogs- och Lantbruksakademien (KSLA) och Kungliga Vetenskapsakademiens (KVA) Nationalkommitté för Nutrition och Livsmedelsvetenskap.
Undernäring hos äldre
Undernäring är ett allvarligt tillstånd, som är förknippat med ökad risk för komplikationer, förlängda vårdtider och minskad livskvalitet. Obehandlat kan det leda till döden. Sköra äldre utgör en specifik riskgrupp. Risken för undernäring ökar med stigande ålder beroende på ett försämrat immunförsvar och ökad förekomst av sjuklighet. Det finns flera typer av undernäring, orsakade av sjukdom med eller utan systemisk inflammation. Systemisk inflammation leder till nedbrytningen av kroppens vävnader, fram för allt av skelettmuskulaturen. God nutrition är en förutsättning för att motverka risken för undernäring hos äldre. Rätt nutritionsvård kräver ett tvärprofessionellt samarbete mellan flera olika hälso- och sjukvårdsprofessioner. Ett personcentrerat förhållningssätt är viktigt i nutritionsvården. Den äldre personen och närstående ska ses som jämbördiga partners till vårdpersonalen.
>> text: Elisabet Rothenberg, biträdande professor, Fakulteten för hälsovetenskap, Högskolan Kristianstad
Bakgrund
Äldre, personer över 65 år, utgör den snabbast växande andelen av befolkningen (1). De flesta lever aktiva och självständiga liv, med ingen eller relativt liten påverkan av sjukdom. Studier har också visat att äldre fortsätter med goda matvanor så länge hälsan är god. Ålder i sig är emellertid den största riskfaktorn för sjukdom och funktionsnedsättningar och från 80 års ålder ökar hjälpbehovet markant (4).
Inom den äldsta åldersgruppen, från 95 år, hade 86 procent av kvinnorna och 75 procent av männen någon form av socialtjänstinsats, mätt 31 oktober 2021. Siffrorna speglar tydligt hur behovet av hjälp och stöd från äldreomsorgen ökar med stigande ålder. Orsaken är tilltagande åldersskörhet (frailty på engelska), som innebär minskad adaptiv förmåga (anpassning) och minskad kapactiet hos kroppen att reparera skador på både celler och organ (5, 6). Åldersskörhet leder till minskade marginaler i samtliga fysiologiska system, och därmed till ökad sårbarhet för sjukdomar och funktionsnedsättning.
Inflammation
Immunförsvaret drabbas av denna försvagning som kommer med stigande ålder. Denna försvagning kallas på engelska ”immunosenescence” (7) och kan sammanfattas som en pågående försämring av viktiga funktioner i både det medfödda och cellmedierade immunförsvaret (8). Processen leder till sämre svar på vaccinering, ökad risk för infektioner och ökad förekomst av kroniska sjukdomar som högt blodtryck, kardiovaskulära sjukdomar, kronisk obstruktiv lungsjukdom (KOL), cancer och Alzheimers sjukdom (5, 9).
Det som på engelska benämns ”inflammageing” utgör en del av åldersförändringarna i immunförsvaret (8). De underliggande mekanismerna är inte fullständigt kartlagda, men tillståndet kännetecknas av en låggradig, kronisk inflammation, orsakad av förändrad balans mellan pro-inflammatoriska och anti-inflammatoriska cytokiner (10, 11). Resultatet är en dominas av pro-inflammatoriska cytokiner. ”Inflammageing” har en långsiktigt negativ inverkan på hela det fysiologiska systemet med ökad sårbahet för sjukdomar som följd. Covid-19 är ett tydligt exempel på hur obalansen mellan olika typer av cytokiner kan orsaka en så kallad cytokinstorm till följd av åldersförändringar i immunförsvaret. Denna förändring var en viktig orsak till att personer i höga åldrar drabbades värst av pandemin.
Den samlade effekten ett försämrat immunförsvar och en ökad sårbarhet för sjukdom utgör tillsammans är en viktig förklaring till att risken för sjukdomsrelaterad undernäring ökar med stigande ålder. Graden av inflammation mäts med hjälp av så kallat akutfasprotein (CRP).
Denna översikt beskriver kunskapsläget vad gäller förekomst (prevalens), riskgrupper – och vad som kan göras för att förebygga undernäring hos äldre personer.
Undernäring – orsak och verkan
Undernäring (malnutrition på engelska) definieras i Socialstyrelsens termbank som en ”näringsrubbning i form av brist på näringsämnen” och kännetecknas av brist på energi, protein eller andra näringsämnen som orsakar mätbara och ogynnsamma förändringar i kroppens sammansättning, funktion eller av ett sjukdomsförlopp (12). Orsaken är en kombination av ett för lågt energiintag till följd av minskad aptit och aktiv nedbrytning (katabolism) av skelettmuskelmassan orsakat av inflammation (figur 1). Det är ett tillstånd som innebär ofrivillig viktförlust och som obehandlat kan leda till undernäring. Skelettmuskelmassan är en förutsättning för fysisk och motorisk funktion, men är också kroppens proteinreserv. Skelettmuskelmassan behövs för att möta ett ökat behov av energi beroende på inflammationen vid undernäring och för att omvandla muskelproteiner till andra proteiner, till exempel brukar serumalbumin sjunka medan akutfasprotein (CRP) ökar, i samband med inflammation.

Figur 1. Orsak till vävnadsförlust och undernäring.
Undernäring leder till psykiska förändringar som trötthet, inaktivitet, depression och apati. Vanliga fysiska komplikationer är infektioner, försämrad sårläkning och nedsatt förmåga till rehabilitering samt ökad sjuklighet och försämrad livskvalitet (13). Konsekvenserna innebär inte bara lidande för den enskilda, utan också betydande samhällsekonomiska kostnader (14, 15). Vanliga kroniska sjukdomar som kan leda till undernäring är cancer, kroniskt obstruktiv lungsjukdom (KOL), hjärt- och njursvikt och reumatoid artrit.
Undernäring – klassifikation
Det finns olika former av undernäring relaterat till bakomliggande orsaker (16, 17) (figur 2).
 Figur 2. Klassifikation av undernäring enligt Cederholm m.fl. (16, 17).
Figur 2. Klassifikation av undernäring enligt Cederholm m.fl. (16, 17).
- Risk för undernäring är ett medicinskt tillstånd med ökad risk för sjuklighet och dödlighet som alltid bör utredas.
- Sjukdomsrelaterad undernäring med inflammation orsakas inte enbart av ett otillräckligt näringsintag. Systemisk inflammation leder till nedbrytningen av kroppens vävnader, fram för allt av skelettmuskulaturen. Kakexi är ett närbesläktat tillstånd, som definieras av påtaglig förlust av fram för allt skelettmuskelmassa (katabola processer), där inflammation är drivande, orsakad av den underliggande sjukdomen. Det är ett vanligt tillstånd vid cancersjukdom.
- Sjukdomsrelaterad undernäring utan inflammation är ett tillstånd förknippat med sjukdomar som på olika sätt påverkar förmågan att äta. Det kan vara neurologiska sjukdomar, till exempel Parkinsons sjukdom, sjukdomar som orsakar sväljproblem (dysfagi) och psykiatriska sjukdomar som anorexia nervosa eller depression.
- Icke sjukdomsrelaterad undernäring kan relatera till svält, socioekonomi, till exempel utbildning, eller psykologiska faktorer, till exempel ensamhet och depression.
Undernäring – diagnostik
En vetenskapligt väl dokumenterad och etablerad metod för att diagnostisera undernäring är GLIM-kriterierna (Global Leadership Initiative on Malnutrition) (tabell 1), som är resultat av samarbetet mellan en rad globala nutritionsorganisationer (18). Diagnosen kan ställas genom olika kombinationer av mätvärden och index (fenotypiska) och bakomliggande (etiologiska) kriterier. Värt att notera är att personer med ett högt BMI kan diagnostiseras som undernärda, om de oavsiktligt tappar vikt eller muskelmassa, i kombination med ett av de etiologiska kriterierna (tabell 1). Det är vidare möjligt att fastställa graden av undernäring i två steg: måttlig respektive svår undernäring. Svårighetsgraden är av betydelse för prognosen och för att kunna besluta om behandlingsinsatser.
Tabell 1. Undernäringsdiagnostik (17, 18).

Prevalens
Förekomsten av undernäring, prevalensen, varierar mellan olika studier beroende på vilka kriterier som tillämpats för att fastställa tillståndet, och vilken population som studerats.
Nationellt heltäckande data saknas för Sverige. Brittiska data uppskattar att cirka 10 procent av de över 65 år är drabbade, och förekomsten ökar med stigande ålder (19). I en svensk avhandling från 2013 studerades äldres nutritionsstatus i samband med inläggning på sjukhus i en framåtsiktande (prospektiv) kohortstudie av individer från 65 år (n = 1767). Av de undersökta individerna bedömdes då 55 procent riskera undernäring och drygt 9 procent vara undernärda. (20-23). Data baserades på fullständig Minimal Nutrition Assessment (MNA), ett riskvärderingsinstrument speciellt avsett för riskbedömning av äldre personer (23). En uppföljning gjordes drygt fyra år (50 månader) senare. Under perioden för uppföljningen dog 37 procent av deltagarna i studien. Vid uppföljningens slut var överlevnaden 75 procent för välnärda deltagare, 60 procent för dem med risk för undernäring och 34 procent för undernärda deltagare. Total risk för död var 1,56 gånger högre i gruppen med risk för undernäring och 3,71 gånger högre i den undernärda gruppen. Nutritionsstatus identifierat med MNA visade sig vara en oberoende riskfaktor för tidig död bland personer 65 år och äldre.
En annan svensk avhandling från 2021 (24), baserad på data från det vårdpreventiva kvalitetsregistret Senior alert för personer från 65 år, och på data från Umeå85+/Gerontological Regional Database-study med personer från 85 års ålder, visar på förekomst av undernäring mätt med MNA. Förekomsten av undernäring varierade mellan 5 och 12 procent i fyra undersökta grupper (kohorter), och risken för undernäring låg mellan 32 och 37 procent. Förekomsten av undernäring var högre bland kvinnor än män. Lägre dödlighet noterades bland dem med god nutritionsstatus. Sammanfattningsvis visades högre BMI, inklusive svår fetma, vara fördelaktigt för överlevnaden.
I en internationell sammanställning av tidigare publicerade data, med 4 500 deltagare över 65 år och med en medelålder på 82 år, var prevalensen av undernäring på 51 procent inom geriatrisk rehabilitering, 39 procent på sjukhus, 14 procent bland individer på vårdboenden (”nursing home”) och 6 procent hos äldre som bodde hemma (22).
I en annan mycket omfattande systematisk översikt (25) rapporterades prevalensdata baserat på 240 studier med totalt 113 967 personer. Förekomsten varierade stort beroende på var studierna var genomförda. Prevalensen varierade från 3 procent bland äldre personer som bodde hemma, till 29 procent inom långtidsvård, och rehabilitering/mindre akut vård. Det finns betydande skillnader mellan de individuella studierna för respektive vårdform, vilket berodde på studiernas kvalitet. Både förekomst av undernäring och de risker som följer kunde kopplas till de olika vårdformernas nivå på hjälp och stöd. Således var prevalensen av undernäring högst inom vårdformer för äldre med de mest omfattande behoven av hjälp och stöd. Orsaksförhållandet mellan nutritionsstatus och nivå av beroende kunde dock inte fastställas, men är en viktig fråga för framtida forskning.
Rutiner för att förebygga och behandla undernäring
Enligt Socialstyrelsens föreskrifter och allmänna råd (HSLF-FS 2022:49) om förebyggande av och behandling vid undernäring (26) ställs särskilda krav på att hälso- och sjukvården och socialtjänsten ska upprätta rutiner för att förebygga och behandla undernäring. Hur dessa rutiner ska utformas i detalj varierar mellan vårdformer, men det är viktigt att det finns en strukturerad process – nutritionsvårdprocessen – med definierade ansvarsområden för olika vårdprofessioner. Denna kan delas in i steg:
Riskbedömning
Riskbedömning med något riskbedömningsinstrument, till exempel MNA (23). Ett alternativ är två enkla frågor om oavsiktlig viktförlust och ätsvårigheter, i kombination med en bedömning Body Mass Index (BMI) – om det är mindre än 22 kg/m2 för personer 70 år och äldre (17). En riskbedömning ska göras på alla nya patienter/vårdtagare, beroende på vårdform och i nära anslutning till vårdkontakten.
Utredning
Utredning görs med hjälp av GLIM-kriterierna (figur 2), tillsammans med en fördjupad analys av bakomliggande orsaker och olika symtom. Minskat kostintag kan utöver att relateras till graden av inflammation också handla om oro, ångest kopplat till sjukdom och behandling. Bland personer i riktigt höga åldrar är kognitiva funktionsnedsättningar till följd av demenssjukdom en bidragande orsak ett lågt kostintag. Svårigheter att tugga och svälja (dysfagi) och biverkningar av läkemedelsbehandling är andra tänkbara bakomliggande orsaker.
Förebygga och behandla undernäring
Här är mat med mer energi och protein oftast den viktigaste åtgärden. Det innebär en kost med små portioner som på olika sätt berikats med livsmedel med hög halt av energi och protein. Det kan till exempel handla om att berika maten med matolja, ägg eller grädde, men också att begränsa mat med stor volym men lågt energiinnehåll, till exempel råkost. För personer som har problem med att tugga och svälja (dysfagi) är det viktigt att också ta ställning till om anpassning av kostens konsistens kan underlätta ätandet och därmed intag av energi och näringsämnen (27).
Kosttillägg är en annan både vanlig och viktig åtgärd. Kosttillägg ska ses som komplement till den vanliga maten när den inte räcker för att täcka behovet av energi och/eller näringsämnen (27). Det finns en stor variation i energiinnehåll och fördelning av de energigivande näringsämnena. Den vanligaste formen av kosttillägg är näringsdrycker med en hög näringstäthet, alltså högt innehåll av energi och protein.
En del äldre personer lider av grava sväljsvårigheter, kanske i sviterna efter en stroke. Per oralt intag – mat genom munnen – är då förknippat med stora risker för felsväljning. Alternativt är sväljförmågan helt satt ur funktion. I den situationen kan det vara aktuellt med i första hand sondnäring (enteral näringstillförsel). Oavsett vilken behandling som ordineras är det viktigt att också sätta mål för vad som ska uppnås med behandlingen, och att kontinuerligt utvärdera om insatserna har önskad effekt.
Samverkan
Samverkan mellan olika yrkesfunktioner inom vård och omsorg är en viktig förutsättning för att nutritionsbehandlingen ska fungera. Dietistens roll är central för att utreda nutritionsproblem och ordinera behandling. Sjuksköterskan leder och ansvarar för omvårdnadsarbetet som omfattar ett helhetsperspektiv på patientens situation. Nutrition ingår som en del i helheten. Läkaren har det övergripande ansvaret för den medicinska behandlingen. Här är nutrition också en del. Fysioterapeuten och arbetsterapeuten kan till exempel bidra med förslag på lämplig sittställning under måltid och hjälpmedel som specialbestick för olika typer av funktionsnedsättningar. En utredning av logoped är också viktig när personen har svårt att svälja, för att ta ställning till lämplig konsistens på mat och dryck.
Den orala hälsan är vital och tandläkare och tandhygienist är centrala aktörer för att bidra till goda förutsättningar för att äta. Nutritionsvården måste också präglas av ett personcentrerat synsätt vilket innebär att den äldre personen ses som en resurs och där professionella vårdare tillsammans med personen och närstående ingår ett partnerskap (28).
Sammanfattning
- Sköra äldre utgör en specifik riskgrupp, med avseende på risk för undernäring, beroende på försämrat immunförsvar och ökad förekomst av sjuklighet.
- Undernäring är ett allvarligt tillstånd, som är förknippat med ökad risk för komplikationer, förlängd vårdtid och minskad livskvalitet. Obehandlat kan det leda till döden.
- Det finns flera typer av undernäring, orsakade av sjukdom med eller utan systemisk inflammation.
- För god nutritionsvård krävs ett tvärprofessionellt samarbete mellan flera olika hälso- och sjukvårdsprofessioner.
- Ett personcentretat förhållningssätt är viktigt i nutritionsvården, där den äldre personen och dennes närstående ses som jämbördiga partners med vårdpersonalen.
Författaren uppger inga jävsförhållanden. Författaren har föreläst för olika nutritionsföretag och har ett forskningssamarbete med Pfizer. Detta bedöms inte påverka artikelns innehåll och därav inte som jäv.
Referenser
1. Sveriges Officiella Statistik. Sveriges framtida befolkning 2021–2070. 2021 April 2021. Contract No.: 2021:1.
2. Eiben G, Andersson CS, Rothenberg E, Sundh V, Steen B, Lissner L. Secular trends in diet among elderly Swedes — cohort comparisons over three decades. Public health nutrition. 2004;7(5):637-44.
3. Samuelsson J, Rothenberg E, Lissner L, Eiben G, Zettergren A, Skoog I. Time trends in nutrient intake and dietary patterns among five birth cohorts of 70-year-olds examined 1971-2016: results from the Gothenburg H70 birth cohort studies, Sweden. Nutr J. 2019;18(1):66.
4. Socialstyrelsen. Statistik om socialtjänstinsatser till äldre 2021. Stockholm: Socialstyrelsen; 2022. p. 4.
5. Niccoli T, Partridge L. Ageing as a risk factor for disease. Current biology : CB. 2012;22(17):R741-52.
6. Kirkwood TB. Understanding the odd science of aging. Cell. 2005;120(4):437-47.
7. Rodrigues LP, Teixeira VR, Alencar-Silva T, Simonassi-Paiva B, Pereira RW, Pogue R, et al. Hallmarks of aging and immunosenescence: Connecting the dots. Cytokine & growth factor reviews. 2021;59:9-21.
8. Aiello A, Farzaneh F, Candore G, Caruso C, Davinelli S, Gambino CM, et al. Immunosenescence and Its Hallmarks: How to Oppose Aging Strategically? A Review of Potential Options for Therapeutic Intervention. Frontiers in immunology. 2019;10:2247.
9. Morrisette-Thomas V, Cohen AA, Fülöp T, Riesco É, Legault V, Li Q, et al. Inflamm-aging does not simply reflect increases in pro-inflammatory markers. Mechanisms of ageing and development. 2014;139:49-57.
10. Michaud M, Balardy L, Moulis G, Gaudin C, Peyrot C, Vellas B, et al. Proinflammatory cytokines, aging, and age-related diseases. Journal of the American Medical Directors Association. 2013;14(12):877-82.
11. Minciullo PL, Catalano A, Mandraffino G, Casciaro M, Crucitti A, Maltese G, et al. Inflammaging and Anti-Inflammaging: The Role of Cytokines in Extreme Longevity. Archivum immunologiae et therapiae experimentalis. 2016;64(2):111-26.
12. Socialstyrelsen. Termbanken. Stockholm [cited 2020 06-29]. Available from: http://termbank.socialstyrelsen.se/
13. Baldwin C, Kimber KL, Gibbs M, Weekes CE. Supportive interventions for enhancing dietary intake in malnourished or nutritionally at-risk adults. Cochrane Database Syst Rev. 2016;12:CD009840.
14. Elia M, Russell CA, Stratton RJ. Malnutrition in the UK: policies to address the problem. Symposium 2: The skeleton in the closet: malnutrition in the community Malnutrition in the UK: policies to address the problem. The Proceedings of the Nutrition Society. 2010;69(4):470-6.
15. Martínez-Reig M, Aranda-Reneo I, Peña-Longobardo LM, Oliva-Moreno J, Barcons-Vilardell N, Hoogendijk EO, et al. Use of health resources and healthcare costs associated with nutritional risk: The FRADEA study. Clinical nutrition (Edinburgh, Scotland). 2018;37(4):1299-305.
16. Cederholm T, Barazzoni R, Austin P, Ballmer P, Biolo G, Bischoff SC, et al. ESPEN Guidelines on Definitions and Terminology of Clinical Nutrition. Clinical Nutrition. 2017;36 (1):49-64.
17. Socialstyrelsen. Att förebygga och behandla undernäring. Kunskapsstöd i hälso- och sjukvård och socialtjänst. Stockholm, Socialstyrelsen; 2020 April. Contract No.: 2020-4-6716.
18. Cederholm T, Jensen GL, Correia M, Gonzalez MC, Fukushima R, Higashiguchi T, et al. GLIM criteria for the diagnosis of malnutrition – A consensus report from the global clinical nutrition community. Clinical nutrition (Edinburgh, Scotland). 2018.
19. Malnutrition among Older People in the Community: Policy Recommendations for Change. London, Alliance ENfH; 2006 May 17th 2006.
20. Soderstrom L, Thors Adolfsson E, Rosenblad A, Frid H, Saletti A, Bergkvist L. Mealtime habits and meal provision are associated with malnutrition among elderly patients admitted to hospital. Clinical nutrition (Edinburgh, Scotland). 2013;32(2):281-8.
21. Cereda E. Mini nutritional assessment. Current opinion in clinical nutrition and metabolic care. 2012;15(1):29-41.
22. Kaiser MJ, Bauer JM, Ramsch C, Uter W, Guigoz Y, Cederholm T, et al. Frequency of malnutrition in older adults: a multinational perspective using the mini nutritional assessment. Journal of the American Geriatrics Society. 2010;58(9):1734-8.
23. Vellas B, Guigoz Y, Garry PJ, Nourhashemi F, Bennahum D, Lauque S, et al. The Mini Nutritional Assessment (MNA) and its use in grading the nutritional state of elderly patients. Nutrition (Burbank, Los Angeles County, Calif). 1999;15(2):116-22.
24. Burman M. Malnutrition and obesity among older adults, assessed by Mini Nutritional Assessment and the body mass index, respectively: prevalence and associations with mortality and urinary tract infection. Umeå: Umeå University; 2021.
25. Cereda E, Pedrolli C, Klersy C, Bonardi C, Quarleri L, Cappello S, et al. Nutritional status in older persons according to healthcare setting: A systematic review and meta-analysis of prevalence data using MNA(®). Clinical nutrition (Edinburgh, Scotland). 2016;35(6):1282-90.
26. Föreskrifter och allmänna råd (HSLF-FS 2022:49) om förebyggande av och behandling vid undernäring (2022).
27. Rothenberg E. 3. Särskilda näringsbehov hos sköra äldre. I Mat och måltider inom äldreomsorgen – vetenskapligt underlag om måltidsmiljö och verksamhetsstruktur, fysiologiska och sensoriska aspekter av åldrandet samt särskilda näringsbehov hos sköra äldre. Uppsala: Livsmedelsverket; 2017 2017-10-09.
28. Edvardsson D. Personcentrerad omvårdnad i teori och praktik. Lund: Studentlitteratur; 2010.
Lästips:
Faxén Irving G.; Karlström B.; Rothenberg E. Geriatrisk nutrition. 2. uppl. ed. Lund: Studentlitteratur; 2016.
Vårdhandboken, avsnitt nutrition. https://www.vardhandboken.se/vard-och-behandling/nutrition/
Kolin – det okända men viktiga näringsämnet
Kolin är ett essentiellt näringsämne som är nödvändigt för bland annat fettomsättning och bildning av signalsubstansen acetylkolin. Kolin kan tillgodogöras via maten eller nybildas i kroppen, men nybildningen är inte tillräcklig för att fylla behovet och kolin anses därför vara ett essentiellt näringsämne.
Kolin förekommer i en mängd livsmedel. Kött, mejeriprodukter, ägg och spannmål är de vanligaste livsmedelskällorna i Norden. Kolin klassades som essentiellt näringsämne i USA 1998, men det var först 2016 som näringsrekommendationer för intag av kolin publicerades för Europa av den Europeiska myndigheten för livsmedelsäkerhet (EFSA).
Studier hos både människa och djur har visat att intag av kolin är viktigt för fosterutveckling under graviditeten och kan medverka i utvecklingen av ett flertal sjukdomar hos vuxna. Men det finns ett stort behov av fler studier.
>> text: Therese Karlsson, leg dietist, forskare, Avdelningen för invärtesmedicin och klinisk nutrition, Institutionen för medicin, Sahlgrenska Akademin, Göteborgs universitet; Avdelningen för livsmedelsvetenskap, Institutionen för biologi och bioteknik, Chalmers tekniska högskola, Göteborg
Metabolism och funktion
Kolin kan fås från maten eller nybildas i kroppen. Nybildningen är inte tillräcklig och kolin anses därför vara ett essentiellt näringsämne. Kolin har många funktioner i kroppen och spelar en viktig roll i fettransport och fettmetabolism, och bildning av signalsubstansen acetylkolin (1).
1. Kolin behövs för bildning av fosfolipider som fosfatidylkolin och sfingomyelin, och i första hand fosfatidylkolin som utgör 95 procent av kroppens totala kolinpool (3). Fosfatidylkolin är en viktig beståndsdel i cellmembran eftersom de utgör 40 till 50 procent av fosfolipider i cellerna, som har betydelse för cellers struktur och normala funktion. Fosfatidylkolin är nödvändig för triglycerid- och kolesteroltransport från levern.
2. Kolin är involverat i reaktioner som ger de metylgrupper som behövs för att bilda en rad livsnödvändiga molekyler, bland annat DNA och aminosyror.
3. Kolin är nödvändigt för syntesen av nervsignalsubstansen acetylkolin.
4. Kolin som inte absorberas kan användas som substrat av bakterier i tarmen och bilda trimetylamin (TMA), och därefter trimetylamin N-oxid (TMAO) i levern. Högre nivåer av cirkulerande TMAO har satts i samband med ökad risk för diabetes och hjärt-kärlsjukdom (4). Men det är oklart om höga nivåer av TMAO är orsak till, eller en konsekvens, av sjukdom. Även andra näringsämnen kan omvandlas till TMA i tarmen och kolin är därför inte unikt för bildningen av TMAO.
Kolin finns i flera olika former både i kroppen och i maten, och de vanligaste formerna är fritt kolin, fosfokolin, glycerofosfokolin, sfingomyelin och fosfatidylkolin. I maten beräknas totalt kolin som summan av dessa olika former.
Absorption i tarmen och metabolismen skiljer sig för de olika formerna. De vattenlösliga – fritt kolin, glycerofosfokolin och fosfokolin – når levern via portavenen och de fettlösliga – sfingomyelin och fosfatidylkolin absorberas i kylomikroner (fett- och proteinpartiklar som transporterar fett) och transporteras med lymfa (2). Intag av de olika formerna skulle kunna ha olika effekt och bör i tillägg till totalt kolinintag beaktas i studier av kolins effekter.
Kolinbrist
Kolin kan bildas i kroppen men inte i tillräcklig mängd. Vi behöver därför få kolin via maten och brist på kolin leder till lever- och muskelskador (5). Hos djur har kolin länge ansetts vara ett essentiellt näringsämne. Behovet hos människan uppmärksammades egentligen först när man såg att personer med total parenteral nutrition (näringsdropp) utvecklade leverskador (5).
Zeisel och medarbetare har utfört studier på människor där deltagarna har fått en kost med mycket lågt innehåll av kolin. Vid ett dagligt intag på mindre än 50 mg/70 kg kroppsvikt utvecklade fler än hälften av deltagarna leverskador, mätt genom nivåer av leverenzymer i serum. Nivåerna återgick till det normala då deltagarna åter gavs 500 mg kolin om dagen (2). I uppföljande studier såg man också att behovet skilde sig mellan kvinnor före och efter klimakteriet – och män. Kvinnor före klimakteriet hade visst skydd mot leverskador vilket förklaras av att syntesen av kolin i kroppen är ökad vid högre mängd östrogen (6).
Betydelse för hälsa
Graviditet och barnets hälsa
Under graviditet och amning ökar behovet av kolin, till det växande fostret och sedan för bröstmjölksproduktion. Kolin är viktigt för fostrets tillväxt och utvecklingen av fostrets hjärna (7). Ett lägre intag av kolin har satts i samband med ökad risk för neuralrörsdefekter till exempel ryggmärgsbråck. En ny systematisk översikt och meta-analys inkluderade 1131 mödrar med barn födda med olika neuralrörsdefekter. För mödrar med ett lägre kolinintag var sannolikheten högre att få barn med ryggmärgsbråck (7). I detta fall är randomiserade kontrollerade studier oetiskt, men denna meta-analys tillsammans med djurstudier tyder på att ett tillräckligt kolinintag är viktigt för att förebygga neuralrörsdefekter hos barnet – men fler studier behövs. Några randomiserade kontrollerade studier har visat positiva effekter av kolintillskott under graviditeten hos friska kvinnor på vissa aspekter av barnets kognitiva utvecklig, till exempel inlärning och minne (7). I dessa studier var dock kolinintaget högre än rekommendationerna, de studerade kognitiva utfallen var olika mellan studierna och det var relativt få deltagare – så fler stora studier behövs.
Kardiovaskulär sjukdom
I och med sin roll i fettmetabolismen och i produktionen av TMAO har kolin undersökts i samband med hjärt-kärlsjukdom. Den genomgång som gjordes inför publiceringen av EFSA:s kolinrekommendationer fann forskarna inte något samband mellan kolinintag och framtida risk för hjärt-kärlsjukdom (2). Slutsatsen stöds av resultat från senare studier som inte heller rapporterat något samband mellan kolinintag och risk för hjärt-kärlsjukdom (8, 9).
Studier kring kolinintag och att dö av hjärt-kärlsjukdomar visar motstridiga resultat. I en studie på 29 279 kvinnor och män i Japan var ett rapporterat högre intag av totalt kolin inte kopplat till att dö av hjärt-kärlsjukdomar. Samtidigt var intag av kolin från sfingomyelin kopplat till en ökad risk att dö av hjärt-kärlsjukdomar (10). Resultat från två stora kohorter från USA visade ökad risk att dö av hjärt-kärlsjukdomar med ett högre rapporterat intag av totalt kolin och fosfatidylkolin (11, 12). Yang och medarbetare inkluderade tre kohorter från USA och Kina, men inget samband mellan rapporterat intag av kolin och död relaterad till stroke rapporterades. Samtidigt rapporterades en högre risk för död från kranskärlssjukdom, men bara i två av tre kohorter (13). Således tyder några observationer på en möjlig ökad risk av förtida död från hjärt-kärlsjukdomar. Men – resultaten är motstridiga och bilden komplex beroende på vilken typ av kolin och vilka befolkningar som studerats. Det finns endast få studier med europeiska befolkningar.
Kognition hos vuxna
Kognitiv funktion hos friska vuxna har undersökts i ett par studier. Hos 1391 friska män och kvinnor (36–83 år) var verbal och visuell förmåga bättre vid högre kolinintag (14). Samtidigt fann man inget samband mellan kolinintag och andra kognitiva funktioner. I en studie från Finland med 2497 män mellan 42 och 60 år undersöktes risken för ett samband mellan demenssjukdom och rapporterat intag av totalt kolin samt intag av fosfatidylkolin (15). En uppföljande studie efter 22 år visade att högre intag av fosfatidylkolin var relaterat till lägre risk för demenssjukdom men man såg samtidigt inget samband mellan intag av totalt kolin och utveckling av demenssjukdom (15). Sammantaget tyder några observationsstudier på att kolin spelar en skyddande roll för kognitiv hälsa hos vuxna. Men underlaget är mycket begränsat och inga interventionsstudier är genomförda.
Livsmedelskällor, rekommendationer och intag
Livsmedelskällor
Kolin finns i en mängd olika livsmedel. Högst mängd per portion finns i animaliska livsmedel som ägg, kött, fågel, fisk och mejeriprodukter. Kolin finns också i många växtbaserade livsmedel som spannmål, vissa grönsaker, baljväxter, frön och nötter. Tabell 1 visar kolininnehållet i ett urval av livsmedel. Kolin finns också i förtjockningsmedlet lecitin, som används i livsmedelsindustrin, och som består av en stor andel fosfatidylkolin. I kosttillskott används vanligen kolinsalterna kolinbitartrat och kolinklorid samt fosfatidylkolin.
Idag finns enbart en amerikansk databas för kolininnehåll i mat tillgänglig (16). Detta försvårar studier på kolinintag eftersom innehåll av kolin i livsmedel kan skilja sig mellan samma livsmedel i olika geografiska områden. Dessutom finns inte livsmedel och maträtter specifika för ett geografiskt område med i den amerikanska databasen. Det finns alltså ett stort behov för en nationell databas för kolininnehåll i livsmedel.

Rekommendationer
Det finns idag inga rekommendationer för intag av kolin i Norden. Men det kommer att finnas ett kapitel om kolin i de kommande nordiska näringsrekommendationerna 2022. Få länder har nationella rekommendationer för kolinintag. Institute of Medicine, numera National Academy of Medicine (NAM) i USA var först med att publicera rekommendationer 1998 (17). Dessa rekommendationer baserades på en studie – den enda vid denna tidpunkt som undersökte tillräckligt intag för att undvika leverskador.
Det finns idag inget bra mått på kolinbrist eller någon markör för kolinintag. Kolin i blod är till exempel inte ett bra mått för vare sig kolinintag eller kolinbrist. NAM ansåg därför att det inte fanns tillräckligt underlag att sätta ett annat referensvärde än så kallat ”tillräckligt intag” vilket är ett referensvärde baserat på svagare underlag än ”rekommenderat intag” (17).
Tillräckligt intag av kolin sattes av NAM till 425 mg/dag för kvinnor och 550 mg/dag för män (tabell 2). Under 2016 etablerade EFSA riktlinjer för kolinintag men även då bedömdes att underlaget inte var tillräckligt för att fastställa ett genomsnittsbehov, alltså 97-98 procent av en grupps behov. Istället så rekommenderar EFSA ett tillräckligt intag av kolin på 400 mg/dag för vuxna (2). Både NAM och EFSA har tagit hänsyn till ett ökat behov av kolin under graviditet och amning. Baserat på olika sätt att värdera det ökade behovet satte NAM ett tillräckligt intag under graviditeten på 450 mg/dag och EFSA 480 mg/dag. Under amning går cirka 120 mg kolin per dag över till bröstmjölk och tillräckligt intag vid amning har satts till 520 mg/dag av NAM och 550 mg /dag av EFSA.
Det finns idag inte tillräcklig kunskap om tillskott av kolin generellt bör rekommenderas till någon enskild grupp.

Intag
Det saknas mycket kunskap om intag av kolin i Europa och Norden. Vennemann och medarbetare beräknade intag av kolin baserat på befolkningsbaserade kostundersökningar från ett antal europeiska länder (18). Det rapporterade medianintaget av kolin var 317-442 mg kolin/dag hos män och 282-374 mg/dag hos kvinnor. I denna studie ingick matvaneundersökningen Riksmaten vuxna 2010-11 för att beräkna kolinintag i Sverige. Rapporterat medianintag hos vuxna under 65 år i Sverige var 442 mg/dag hos män och 365 mg/dag hos kvinnor. De vanligaste livsmedelskällorna till kolin i den europeiska befolkningen rapporterades vara kött, fisk, ägg, spannmål och mejeriprodukter (18).
Generellt rapporterades ett kolinintag som är lägre än rekommendationer om tillräckligt intag, men svårigheter att mäta och beräkna intag av kolin bör beaktas. Men – dessa resultat tillsammans med undersökningar från andra delar av världen talar för att det generellt kan finnas grupper som har ett lågt intag av kolin. Då animaliska livsmedel innehåller mer kolin per portion skulle en vegetarisk eller vegansk kost kunna vara en risk för lågt intag av kolin. Det finns idag mycket begränsad kunskap om kolinintag hos vegetarianer och veganer och inga studier har undersökt intag av kolin i dessa grupper i Sverige. I en amerikansk studie på en grupp vegetarianer rapporterades ett medelintag på 192 mg kolin/dag (19). Därför kan det behövas extra hänsyn till intag av kolin vid planering av växtbaserade koster.
Författaren uppger inga jävsförhållanden.
Referenser
1.Ueland PM. Choline and betaine in health and disease. Journal of inherited metabolic disease. 2011;34(1):3-15. doi: 10.1007/s10545-010-9088-4.
2. EFSA Panel on dietetic products. Dietary references values for choline. EFSA Journal. 2016;14(8):4484. doi: 10.2903/j.efsa.2016.4484.
3. Zeisel SH. Choline: critical role during fetal development and dietary requirements in adults. Annual review of nutrition. 2006;26:229-50. doi: 10.1146/annurev.nutr.26.061505.111156.
4. Heianza Y, Ma W, Manson JE, Rexrode KM, Qi L. Gut Microbiota Metabolites and Risk of Major Adverse Cardiovascular Disease Events and Death: A Systematic Review and Meta-Analysis of Prospective Studies. Journal of the American Heart Association. 2017;6(7). doi: 10.1161/JAHA.116.004947.
5. Buchman AL, Dubin MD, Moukarzel AA, Jenden DJ, Roch M, Rice KM, et al. Choline deficiency: a cause of hepatic steatosis during parenteral nutrition that can be reversed with intravenous choline supplementation. Hepatology. 1995;22(5):1399-403.
6. Fischer LM, daCosta KA, Kwock L, Stewart PW, Lu TS, Stabler SP, et al. Sex and menopausal status influence human dietary requirements for the nutrient choline. Am J Clin Nutr. 2007;85(5):1275-85.
7. Obeid R, Derbyshire E, Schon C. Association between maternal choline, foetal brain development and child neurocognition; systematic review and meta-analysis of human studies. Advances in nutrition. 2022. doi: 10.1093/advances/nmac082.
8. Bertoia ML, Pai JK, Cooke JP, Joosten MM, Mittleman MA, Rimm EB, et al. Plasma homocysteine, dietary B vitamins, betaine, and choline and risk of peripheral artery disease. Atherosclerosis. 2014;235(1):94-101. doi: 10.1016/j.atherosclerosis.2014.04.010.
9. Millard HR, Musani SK, Dibaba DT, Talegawkar SA, Taylor HA, Tucker KL, et al. Dietary choline and betaine; associations with subclinical markers of cardiovascular disease risk and incidence of CVD, coronary heart disease and stroke: the Jackson Heart Study. Eur J Nutr. 2018;57(1):51-60. doi: 10.1007/s00394-016-1296-8.
10. Nagata C, Wada K, Tamura T, Konishi K, Kawachi T, Tsuji M, et al. Choline and Betaine Intakes Are Not Associated with Cardiovascular Disease Mortality Risk in Japanese Men and Women. J Nutr. 2015;145(8):1787-92. doi: 10.3945/jn.114.209296.
11. Mazidi M, Katsiki N, Mikhailidis DP, Banach M. Dietary choline is positively related to overall and cause-specific mortality: results from individuals of the National Health and Nutrition Examination Survey and pooling prospective data. Br J Nutr. 2019;122(11):1262-70. doi: 10.1017/S0007114519001065.
12. Zheng Y, Li Y, Rimm EB, Hu FB, Albert CM, Rexrode KM, et al. Dietary phosphatidylcholine and risk of all-cause and cardiovascular-specific mortality among US women and men. Am J Clin Nutr. 2016;104(1):173-80. doi: 10.3945/ajcn.116.131771.
13. Yang JJ, Lipworth LP, Shu XO, Blot WJ, Xiang YB, Steinwandel MD, et al. Associations of choline-related nutrients with cardiometabolic and all-cause mortality: results from 3 prospective cohort studies of blacks, whites, and Chinese. Am J Clin Nutr. 2020;111(3):644-56. doi: 10.1093/ajcn/nqz318.
14. Poly C, Massaro JM, Seshadri S, Wolf PA, Cho E, Krall E, et al. The relation of dietary choline to cognitive performance and white-matter hyperintensity in the Framingham Offspring Cohort. Am J Clin Nutr. 2011;94(6):1584-91. doi: 10.3945/ajcn.110.008938.
15. Ylilauri MPT, Voutilainen S, Lonnroos E, Virtanen HEK, Tuomainen TP, Salonen JT, et al. Associations of dietary choline intake with risk of incident dementia and with cognitive performance: the Kuopio Ischaemic Heart Disease Risk Factor Study. Am J Clin Nutr. 2019;110(6):1416-23. doi:10.1093/ajcn/nqz148.
16. Patterson KY, Bhagwat SA, Williams JR, Howe JC, Holden JM. USDA Database for the choline content of common foods, release two, January 2008. Available at: http://www.ars.usda.gov/services/docs.htm?docid=6232. Accessed 23 April 2014.
17. Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic acid, Bioton, and Choline (1998). Washington, DC: (IOM) Institute of Medicine.
18. Vennemann FB, Ioannidou S, Valsta LM, Dumas C, Ocke MC, Mensink GB, et al. Dietary intake and food sources of choline in European populations. Br J Nutr. 2015:1-10. doi: 10.1017/S0007114515003700.
19. Wallace TC, Blusztajn JK, Caudill MA, Klatt KC, Natker E, Zeisel SH, et al. Choline: The Underconsumed and Underappreciated Essential Nutrient. Nutr Today. 2018;53(6):240-53. doi: 10.1097/NT.0000000000000302.
Möjlighet att lämna synpunkter på flera NNR-kapitel och en bakgrundsartikel
Under augusti och september är flera kapitel och en bakgrundsartikel om miljömässig hållbarhet ute på remiss inför de kommande nordiska näringsrekommendationerna, NNR2022. Det finns möjlighet för forskare och andra intresserade att lämna synpunkter på kapitlen och artikeln.
Kapitel med näringsämnen och livsmedelsgrupper
Fram till den 29 augusti 2022 är kapitlet om jod ute på remiss med möjlighet att lämna synpunkter på kapitlet.
Fram till den 9 september 2022 är följande kapitel ute på remiss:
Folat med möjlighet att lämna synpunkter
Kalcium med möjlighet att lämna synpunkter
Kalium med möjlighet att lämna synpunkter
Fetter och oljor med möjlighet att lämna synpunkter
Fram till den 20 september 2022 är kapitlet om pantotensyra ute på remiss med möjlighet att lämna synpunkter på kapitlet.
En av tre bakgrundsartiklar om miljömässig hållbarhet
Fram till den 30 september 2022 är bakgrundsartikeln om miljömässig hållbarhet ”Assessing the environmental sustainability of diets – an overview of approaches and identification of 5 key considerations for comprehensive assessments” ute på remiss med möjlighet att lämna synpunkter på artikeln. Ytterligare två bakgrundsartiklar om miljömässig hållbarhet är planerade.
Jod – ett anspråkslöst spårämne som lyft folkhälsan och kan rädda framtida liv
Denna översiktsartikel handlar om jodets roll för människan, hur Sverige gjort över tid för att bekämpa jodbristen, var Sverige står idag och vilka framtidens utmaningar är. Sverige har varit framgångsrikt eftersom de allvarligaste konsekvenserna av jodbrist har bekämpats. Men vårt jodintag är långt ifrån garanterat och våra mest utsatta grupper löper fortfarande risk för mild jodbrist. Om vi förlorar kunskapen om jodets betydelse för befolkningen och om monitoreringen brister, riskerar vi att hamna där vi var för 100 år sedan.
Men låt oss börja från början – är människan beroende av jod i sin kost?
>>text: Sofia Manousou, PhD, överläkare Frölunda Specialistsjukhus, Västra Frölunda och Helena Filipsson Nyström, docent, universitetssjukhusöverläkare Sahlgrenska Universitetssjukhuset, Göteborg
Ett alldeles nödvändigt spårämne
När jod förångas omvandlas den till violett rök, och det är från ångans färg – ”ιώδες” (iodes) betyder ”violfärgad” på grekiska – som jod fått sitt namn (figur 1). Jodatomer behövs som byggstenar till sköldkörtelhormonerna T4 (tyroxin) och T3 (trijodotyronin), som innehåller fyra respektive tre jodatomer i molekylen.
Sköldkörtelhormonerna styr metabolismen och på ett förenklat sätt kan man säga att de är kroppens gaspedal. Vid jodbrist sätter kroppen i gång sina kompensatoriska mekanismer: sköldkörteln ökar i storlek – struma – med risk för utveckling av knölar i sköldkörteln. Allvarlig jodbrist är därför associerad med struma och låg sköldkörtelfunktion, eftersom det saknas byggstenar. Mild till moderat jodbrist kan i sin tur även ge hög ämnesomsättning (när aktiva knölar blir självständiga och inte lyssnar på kroppens förnuftiga styrning) (1, 2). Hög ämnesomsättning kan leda till hjärtklappning, trötthet och viktnedgång.
Det är därför viktigt att upprätthålla normal jodnivå i befolkningen både för att minska struma och förekomsten av sköldkörtelsjukdomar. Jod och sköldkörtelhormon är också extra viktiga under graviditet och amning.
För fostret och det nyfödda barnet är jod och sköldkörtelhormonerna avgörande för den fysiska och den kognitiva utvecklingen (2). Allvarlig jodbrist under graviditeten eller tidigt i livet kan leda till missfall, dödfödsel eller allvarliga utvecklingsavvikelser, så kallad kretinism. Kretinism innebär en allvarlig utvecklingsstörning med samtidiga avvikelser som kortvuxenhet, döv-stumhet och vissa utseendemässiga särdrag till följd av brist på sköldkörtelhormon i fosterlivet.
Det pågår en kamp i världen mot jodbrist. Allvarlig jodbrist förekommer idag inte i Sverige. Det är dock globalt vanligt med mild till moderat jodbrist under graviditeten – i Europa förekommer det i 2 av 3 länder (3). Några observationsstudier tyder på att mild till moderat jodbrist är associerad med något sämre kognitiv utveckling hos barnet men det saknas starka vetenskapliga bevis. Det gör att experterna är oeniga om gravida kvinnor i dessa länder borde rekommenderas dagligt jodtillskott (4). Ytterligare studier av hög vetenskaplig kvalitet behövs därför.
För högt intag av jod, till exempel vid intag av algprodukter med mycket högt jodinnehåll eller onödigt jodtillskott, är inte heller riskfritt. Jodöverskott kan leda till både hög och låg ämnesomsättning, genom olika mekanismer.
Det optimala fönstret för jodintaget, som ger lägst risk för sköldkörtelsjukdomar, är således relativt smal. Åtgärder för att säkerställa adekvat jodnutrition i en population behöver vara genomtänkta och jodläget kräver regelbunden monitorering. Detta är två av Livsmedelsverkets ansvarsområden.

Figur 1. När jod förångas bildas violett rök och jod har fått sitt namn från grekiskan – iodes betyder violfärgad.
I naturen och på matbordet
Jod i naturen finns huvudsakligen i de salta haven. Stora mängder jod urlakades ur marken av glaciärer, snö och regn och fördes med floder till haven. Tillgången på jod varierar stort, beroende på varierande jodnivåer i grundvattnet, olika tillgång på mat som innehåller jod (tabell 1) och varierande kostvanor. Mest utsatta är de områden som ligger långt från havet och där folk inte äter fisk och skaldjur. Människan får i sig jod via livsmedel med naturligt högt jodinnehåll – som just fisk och skaldjur – eller via livsmedel där jod har tillsatts, till exempel joderat salt eller mejeriprodukter när djurfodret är jodberikat (5).
Bergsalt innehåller inget eller nästan inget jod och icke-joderat havssalt innehåller mindre än hälften än det joderade saltet gör (6). Jodering av bordssalt är den mest använda och mest framgångsrika strategin mot jodbristen världen över även om jodbrist tyvärr inte är helt eliminerad ännu (3).
Tabell 1. Exempel på livsmedel och dess jodinnehåll och jämförelse med havssalt och joderat salt. Källa: Livsmedelstabell: mineralämnen och spårelement, Livsmedelsverket.

Jodintag – vad är lagom?
Världshälsoorganisationen (WHO) definierar en befolknings jodstatus efter mängden jod i en skvätt urin, så kallad UIC (median urinjodkoncentration) i en för landet representativ population av skolbarn (7, 8). Om medianen hos skolbarnen ligger inom rekommenderat intervall (tabell 2), anser WHO att landet har tillräckligt jodintag i den allmänna befolkningen. Att överföra dessa intervall till en population av vuxna är dock problematiskt, eftersom en vuxen person dricker mer än ett barn och urinen blir mer utspädd, vilket medför lägre jodkoncentration (5).
Ett annat problem med att bedöma jodstatus i en befolkning är att det finns en stor dag-till-dag variation av jodintag (9) och UIC avspeglar den mängd jod som individen har intagit det senaste dygnet. Dag-till-dag variationen av jodintag hos en individ jämnas ut när man bedömer jodstatus på befolkningsnivå – om man har en tillräckligt stor grupp att mäta på. För att bedöma jodnutritionen hos en individ, behövs det däremot urinprov från minst 10 till 14 olika tillfällen (10).
Mätning av UIC är den mest använda metoden för att bedöma jodstatus, eftersom den är billig, praktisk att utföra och relativt lätt att tolka. Men det finns också andra sätt (5). Jodintaget via maten kan skattas utifrån jodspecifika frågeformulär om kosten. Här är problemet att samma typ av livsmedel kan ha varierande jodinnehåll. Det är också svårt att skatta mängden joderat salt som används i matlagning och inom livsmedelsindustrin. Dessutom är jod svårt att analysera i livsmedel.
En annan markör för jodstatus är sköldkörtelstorlek. Tidigare värderades detta genom att känna på sköldkörteln eller genom ultraljud. Båda är sena tecken på jodbrist. Idag används tyreoglobulin, ett blodprov som samvarierar med sköldkörtelns storlek, som markör för jodstatus. Under amning anses jodkoncentrationen i bröstmjölken som den lämpligaste markören för jodstatus (11).
Tabell 2. Kriterier för bedömning av jodnutrition och jodstatus hos en population, baserat på urinjodkoncentration, enligt Världshälsoorganisationen (7, 8).

Jodets historia i Sverige
I mitten av 1800-talet hade 20 till 30 procent av barnen i Gästrikland och Dalarna struma. Efter 20 år hade förekomsten stigit till mellan 60 och 65 procent, med ökad förekomst av kretinism (12) (figur 2). En nationell kartläggning 1929 visade på det så kallade ”strumabältet” (figur 3).
Varför var just dessa områden mest drabbade av jodbrist? En senare undersökning visade att jodnivån i grundvattnet är lägre inom strumabältet från 1929 (13). Det medförde att det totala jodintaget var lägre för befolkningen inom dessa områden. På den tiden var sill den huvudsakliga jodkällan i Sverige. Sill transporterades från västkusten till de större städerna och de som bodde längs vägarna kunde köpa från de så kallade sillfororna. Under 1800-talet introducerandes potatisen, som visserligen räddade folk undan svältdöden, men som genom sitt lägre jodinnehåll bidrog till de ökande problemen med struma eftersom potatisens intåg samvarierade med att sillen försvann från västkusten under många år under 1800-talet.
Samtidigt ledde befolkningsökningen till att mindre bördiga områden började odlas – områden som inte hade varit havsbotten och där marken hade lägre jodinnehåll. Därför blev struman allt vanligare.
Jodbristen i Sverige åtgärdades 1936 med frivillig jodering av bordssalt, först med 10 mikrogram/gram salt, vilket innebar att struman minskade och kretinism hos barn försvann. Men struma försvann inte helt och 30 år senare ökades joderingen till dagens nivå på 50 mikrogram/gram salt (12).
De övriga länderna i Skandinavien har följt olika strategier för att säkerställa adekvat jodnutrition. I Danmark är det obligatoriskt med jodberikning av salt som används i bröd (20 mikrogram/gram salt) (14). I Norge är bordssaltet jodberikat med endast 5 mikrogram/gram salt, men det finns krav på jordberikning av djurfoder. Finland jodberikar både salt (25 mikrogram/gram salt) och djurfoder (12). En nationell kartläggning av jodstatus i Sverige genomfördes 2007, alltså 70 år efter det att jodberikningen av salt startade. Den visade att den svenska befolkningen hade adekvat jodnutrition och det tidigare strumabältet hade försvunnit (15, 16) (figur 2).
 Figur 2. Jodets historia i Sverige. Låga jodnivåer i marken ger förutsättningar för uttalad jodbrist. Sedan introduktion av joderat salt har effekterna minskat, men det finns utmaningar för framtiden.
Figur 2. Jodets historia i Sverige. Låga jodnivåer i marken ger förutsättningar för uttalad jodbrist. Sedan introduktion av joderat salt har effekterna minskat, men det finns utmaningar för framtiden.

Figur 3. Karta som visar förekomsten av struma i Sverige 1928-1929. Källa: Höjer, J., Kropfstudien Die Verbreitung des endemischen Kropfes in Schweden. Svenska Läkarsällskapets handlingar, 1931. 57: s.1-104.
Är jodfrågan då löst i Sverige?
Enligt WHO, behöver jodstatus kontinuerligt monitoreras och jodnutritionen i riskgrupperna kartläggas (7). Finland, som hade högst jodintag i Europa under 80-talet är nu klassat som jodotillräckligt, till följd av en lägre konsumtion av mjölk och joderat salt. Ett annat exempel är Island som är fortsatt jodsufficient (12). Detta trots att jodinnehållet i mjölken har sjunkit dramatiskt sedan 1962 eftersom fisk inte längre används i samma utsträckning i djurfoder. Som kompensation har man på Island jodberikat djurfodret.
Även i Sverige har vi rapporter om en sänkning av jodinnehållet i mjölken mellan 2001 och 2009 – av oklar anledning (17). Omkring 75 procent av konsumerat salt verkar vara icke-joderat (enligt personlig kommunikation med saltindustrin, 2017). Kosttrender mot icke-joderade salter och hälsorekommendation om att äta mindre salt kan också påverka den svenska befolkningens jodstatus i framtiden. Idag finns också trender om att rent allmänt undvika tillsatser. En allt större del av vårt matintag sker också utanför hemmet, vilket gör oss beroende av vilket salt som restauranger och livsmedelsindustrin använder. Risken för jodbrist är därför alltid aktuell.
Aktuell status i Sverige
Den nationella kartläggningen gjordes på en representativ population av skolbarn 2007 och visade adekvat jodstatus i Sverige (15). Livsmedelsverket utförde en undersökning 2016-2017, som visade att pojkar och flickor i årskurs 5, årskurs 8 och årskurs 2 på gymnasiet hade adekvat jodnutrition (18). Det finns därför i nuläget inte anledning att ifrågasätta att Sverige fortfarande är ett jodsufficient land i den allmänna befolkningen. Men situationen kan vara en annan i riskgrupperna, alltså de som behöver högre dagligt jodintag – gravida och ammande kvinnor (tabell 3) och de med en kost som utesluter viktiga jodkällor.
Gravida kvinnor i Sverige uppvisade mild jodbrist vid en nationell kartläggning 2015–16 (19). Våra data från Göteborgsområdet pekar också på mild jodbrist i en population av ammande kvinnor 2008–2011 (20). Om mild jodbrist under graviditet och amning har någon effekt på fostret/spädbarnet är fortfarande inte klarlagt. Det finns inte heller konsensus kring vilken effekt (positiv/negativ/neutral) som eventuellt jodtillskott under graviditet och amning skulle ha på barnet (4). I Sverige pågår forskning med mål att svara på denna viktiga fråga om jod och graviditet, den så kallade ”SWIDDICH-studien” (21).
En viktig aspekt är om kvinnor i barnafödande åldern har tillräckligt jodintag, eftersom jodstatus påverkar vilket utgångsläge kvinnorna har när de blir gravida. Behovet av jod ökar under graviditeten. En kartläggning av flickor i årskurs 2 på gymnasiet, som representerar kostintaget hos kvinnor i barnafödande ålder, och mindre studier av kvinnor i reproduktionsåldern visade nivåer nära gränsen för god jodstatus (18, 22, 23). Så länge det inte gjorts en nationell kartläggning av jodstatus i en representativ population av kvinnor i barnafödande ålder, kan man inte uttala sig med säkerhet om jodstatus i den gruppen. Men de begränsade data vi har indikerar inte jodbrist, men som sagt resultaten behöver säkerställas och följas över tid.
Utöver gravida och ammande kvinnor, så utgör även individer som utesluter jodkällor från sin kost riskgrupper för jodbrist. Invandrargrupper kan vara mer utsatta för jodbrist, eftersom det kan vara svårare att nå ut med information. Dessutom kan kosten av kulturella eller socioekonomiska skäl innebära mindre konsumtion av livsmedel med jod.
Veganer utesluter allt som kommer från djur från sin kost, bland annat mejeriprodukter, fisk och skaldjur. Veganer löper därmed större risk för jodbrist (24) och är i större behov av joderat salt (25) så vi rekommenderar dagligt jodtillskott. Stenåldersdieten är baserad på det som människan hade tillgång till innan de började bruka jorden, vilket exkluderar både mejeriprodukter och salt. För dem är fisk enda jodkällan. Den dieten är associerad med ökad risk för jodbrist och även för dem rekommenderar vi ett dagligt jodtillskott (26).
Tabell 3. Dagligt jodintag och median urinjodkoncentation enligt rekommendationer från Världshälsoorganisationen (7).

Det här kan du göra som konsument
- Välj klokt bland olika salt-alternativ. Många populära sorter, som flingsalt, gourmetsalt, bergsalt, havssalt, innehåller inget eller ringa mängd jod. Läs på förpackningen och välj det salt som har tillsatt jod. Det var joderingen av bordssalt som gjort att Sveriges befolkning sluppit jodbrist det senaste seklet.
- Skydda dig från jodöverskott – för mycket jod är också skadligt. Avstå från algkapslar, jod-droppar eller andra produkter med höga halter jod.
Inför framtiden
- Det är av stor vikt att bibehålla tillräckliga jodnivåer i befolkningen även i framtiden. Den övervakningen ligger inom Livsmedelsverkets ansvarsområde. Eftersom vi har en hög jodering av saltet i Sverige – 50 mikrogram/gram salt, jämfört med 15-30 mikrogram/gram salt som är vanligast i Europa (27) – borde det vara tillräckligt om livsmedelsindustrin använder mer joderat salt och att medvetenheten om att använda joderat salt i hushållen ökar.
- Några riskgrupper för jodbrist – gravida och veganer – är särskilt rekommenderade att använda joderat salt (28, 29). Fortsatt monitorering av gravida i Sverige genom nationella uppföljningsstudier behövs. Dessutom är det angeläget med en kartläggning av jodstatus under amning och vid speciella dieter. Målet är att nå jodsufficiens i riskgrupperna i Sverige.
- Det pågår forskning i Sverige för att svara på frågan om och vilken effekt ett jodtillskott under graviditet skulle ha på fostret (21). I väntan på resultat från den studien, finns det inte någon rekommendation från Livsmedelsverket kring jodtillskott på grund av bristande evidens på dess effektivitet och säkerhet (4).
För att Sverige ska förbli ett jodsufficient land krävs det ett samarbete inom hela samhällssektorn. Det gäller att även säkerställa adekvat jodnutrition i riskgrupperna med speciellt fokus på den särskilt sårbara gruppen av gravida och ammande kvinnor (figur 2).
Kunskapen om jod behöver öka inom livsmedelsindustrin och i samhället i stort. Mattidningar och TV-program om mat måste ta ett ansvar för att inte lansera icke-joderat salt. Det behövs kontinuerlig utbildning inom jodets betydelse, jodbristens historia i vårt land och pågående forskning. Vi hoppas denna översiktsartikel bidrar i den riktningen.
Författarna uppger inga jävsförhållanden.
Referenser
1. Farebrother J, Zimmermann MB, Andersson M. Excess iodine intake: sources, assessment, and effects on thyroid function. Ann N Y Acad Sci. 2019;1446(1):44-65.
2. Zimmermann MB, Jooste PL, Pandav CS. Iodine-deficiency disorders. Lancet. 2008;372(9645):1251-62.
3. Ittermann T, Albrecht D, Arohonka P, Bilek R, de Castro JJ, Dahl L, et al. Standardized Map of Iodine Status in Europe. Thyroid. 2020;30(9):1346-54.
4. Dineva M, Fishpool H, Rayman MP, Mendis J, Bath SC. Systematic review and meta-analysis of the effects of iodine supplementation on thyroid function and child neurodevelopment in mildly-to-moderately iodine-deficient pregnant women. Am J Clin Nutr. 2020;112(2):389-412.
5. Zimmermann MB, Andersson M. Assessment of iodine nutrition in populations: past, present, and future. Nutr Rev. 2012;70(10):553-70.
6. The Iodine Global Network. Iodized salt or sea salt: Which is better for you? 2019. Available from: https://www.ign.org/blog-salt-myths-2019.htm.
7. World Health Organization, UNICEF, International Council for the Control of Iodine Deficiency Disorders. Assessment of iodine deficiency disorders and monitoring their elimination. A guide for programme managers, 3rd edition, Geneva. 2007. Available from: http://apps.who.int/iris/bitstream/handle/10665/43781/9789241595827_eng.pdf?sequence=1.
8. The Iodine Global Network. Global scorecard of iodine nutrition in 2019 in the general population based on school-age children (SAC). IGN: Zurich, Switzerland; 2019.
9. Karmisholt J, Laurberg P, Andersen S. Recommended number of participants in iodine nutrition studies is similar before and after an iodine fortification programme. Eur J Nutr. 2014;53(2):487-92.
10. Konig F, Andersson M, Hotz K, Aeberli I, Zimmermann MB. Ten repeat collections for urinary iodine from spot samples or 24-hour samples are needed to reliably estimate individual iodine status in women. J Nutr. 2011;141(11):2049-54.
11. Dold S, Zimmermann MB, Aboussad A, Cherkaoui M, Jia Q, Jukic T, et al. Breast Milk Iodine Concentration Is a More Accurate Biomarker of Iodine Status Than Urinary Iodine Concentration in Exclusively Breastfeeding Women. J Nutr. 2017;147(4):528-37.
12. Nystrom HF, Brantsaeter AL, Erlund I, Gunnarsdottir I, Hulthen L, Laurberg P, et al. Iodine status in the Nordic countries – past and present. Food Nutr Res. 2016;60:31969.
13. Manousou S SM, Eggertsen R, Hoppe M, Hulthén L, Nyström Filipsson H. Correlations of water iodine concentration to earlier goitre frequency in Sweden– an iodine sufficient country with long-term iodination of table salt (in press). Environmental Health and Preventive Medicine 2019.
14. Miljø- og Fødevareministeriet. Bekendtgørelse om tilsætning af jod til husholdningssalt og salt i brød og almindeligt bagværk m.v. 2019. Available from: https://www.retsinformation.dk/eli/lta/2019/613.
15. Andersson M, Berg G, Eggertsen R, Filipsson H, Gramatkovski E, Hansson M, et al. Adequate iodine nutrition in Sweden: a cross-sectional national study of urinary iodine concentration in school-age children. Eur J Clin Nutr. 2009;63(7):828-34.
16. Filipsson Nyström H, Andersson M, Berg G, Eggertsen R, Gramatkowski E, Hansson M, et al. Thyroid volume in Swedish school children: a national, stratified, population-based survey. Eur J Clin Nutr. 2010;64(11):1289-95.
17. Lindmark Månsson H. Den svenska mejerimjölkens sammansättning 2009. Report no: 7094. The Swedish Dairy Association;2012.
18. Lemming E, Moraeus L, Sipinen J, AK L. Riksmaten ungdom 2016-17. Näringsintag och näringsstatus bland ungdomar i Sverige. Livsmedelsverket; 2018.
19. Manousou S, Andersson M, Eggertsen R, Hunziker S, Hulthén L, Nyström HF. Iodine deficiency in pregnant women in Sweden: a national cross-sectional study. Eur J Nutr. 2020;59(6):2535-45.
20. Manousou S, Augustin H, Eggertsen R, Hulthen L, Filipsson Nystrom H. Inadequate iodine intake in lactating women in Sweden: A pilot 1-year, prospective, observational study. Acta Obstet Gynecol Scand. 2021;100(1):48-57.
21. Manousou S, Johansson B, Chmielewska A, Eriksson J, Gutefeldt K, Tornhage CJ, et al. Role of iodine-containing multivitamins during pregnancy for children’s brain function: protocol of an ongoing randomised controlled trial: the SWIDDICH study. BMJ Open. 2018;8(4):e019945.
22. Becker W, Lindroos AK, Nälsén C, Warensjö Lemming E, Öhrvik V. Dietary habits, nutrient intake and biomarkers for folate, vitamin D, iodine and iron status among women of childbearing age in Sweden. Ups J Med Sci. 2016;121(4):271-5.
23. Manousou S, Eggertsen R, Hulthen L, Filipsson Nystrom H. A randomized, double-blind study of iodine supplementation during pregnancy in Sweden: pilot evaluation of maternal iodine status and thyroid function. Eur J Nutr. 2021.
24. Bakaloudi DR, Halloran A, Rippin HL, Oikonomidou AC, Dardavesis TI, Williams J, et al. Intake and adequacy of the vegan diet. A systematic review of the evidence. Clin Nutr. 2021;40(5):3503-21.
25. Livsmedelsverket. Available from: https://www.livsmedelsverket.se/matvanor-halsa–miljo/kostrad/vegansk-mat.
26. Manousou S, Stal M, Larsson C, Mellberg C, Lindahl B, Eggertsen R, et al. A Paleolithic-type diet results in iodine deficiency: a 2-year randomized trial in postmenopausal obese women. Eur J Clin Nutr. 2018;72(1):124-9.
27. EFSA NDA Panel (EFSA Panel on Dietetic Products Nutrition and Allergies). Scientific Opinion on Dietary Reference Values for iodine. EFSA Journal. 2014;12:3660.
28. Livsmedelsverket, Julin B. Jod under graviditet och amning. Livsmedelsverkets rapportserie. Uppsala. 2020.
29. Svensk Förening för Obstetrik och Gynekologi (Swedish Society of Obstetrics and Gynecology). Tyreoideasjukdom i samband med graviditet (thyroid disease during pregnancy). 2017.
30. Bath SC. The effect of iodine deficiency during pregnancy on child development. Proc Nutr Soc. 2019;78(2):150-60.
31. Institute of Medicine (Panel on Micronutrients). Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Copper, Iodine, Iron, Manganese, Molybdenum, Nickel, Silicon, Vanadium, and Zinc. Washington 2001. 258-89 p.
32. Nordic Council of Ministers. Nordic Nutrition Recommendations 2012: integrating nutrition and physical activity. Copenhagen: Nordic Council of Minsters; 2014.
Så kan nitrat i rödbetsjuice göra gott för hjärta-kärl, njurar och metabolism
Rödbetsjuice har under den senaste tiden lyfts fram i media som en magisk dryck med superkrafter som bland annat hjälper mot åldersrelaterade sjukdomar som hjärtkärlsjukdom och typ 2-diabetes. Rödbetan har också hyllats på flera träningssajter eftersom rödbetsjuice sägs förbättra fysisk uthållighet.
Men vad är det då i rödbetsjuicen som ger den dessa möjliga gynnsamma hälsoeffekter? Rödbetor och flera grönbladiga grönsaker innehåller nitrat som i kroppen kan omvandlas och bilda molekylen kväveoxid (NO•). I kroppen spelar kväveoxid en viktig roll för att upprätthålla normal funktion och reglering av bland annat hjärtkärlsystemet, njurarna, och ämnesomsättningen. Vanliga samhällssjukdomar som hjärtkärlsjukdomar, försämrad njurfunktion och metabol dysfunktion, alltså övervikt kombinerat med typ 2-diabetes, har i flera studier associerats med brist på kväveoxid.
Studier visar att ökat intag av nitrat via kosten kan återställa normala nivåer av kväveoxid i kroppen och på så vis minska utveckling eller försämring av ovan nämnda sjukdomar.
I denna artikel diskuteras de potentiellt gynnsamma effekterna på hjärta och kärl, njurar och metabolism av dietärt nitrattillskott, i första hand i form av rödbetsjuice.
>>text: Mattias Carlström, professor i kardiorenal fysiologi, Institutionen för fysiologi och farmakologi, Karolinska Institutet, Stockholm
Hälsoeffekter kopplade till frukt och grönsaker
Hjärtkärlsjukdom och typ 2-diabetes, är idag växande globala hälsoproblem, som ofta samexisterar med en försämrad njurfunktion hos äldre. Dessa välfärdssjukdomar, i synnerhet i den industrialiserade världen, kan i hög grad kopplas till ett alltmer stillasittande liv och en osund kost enligt Världshälsoorganisationen, WHO. Denna moderna livsstil bidrar ofta till övervikt och fetma som i sin tur är starkt kopplat till risken för att utveckla allvarliga sjukdomar.
Det råder idag ingen tvekan om att ökad fysisk aktivitet och bra matvanor med ett dagligt intag av mycket frukt och grönsaker är gynnsamt för hälsan. Ett sådant samband mellan kosten och hälsan har bevisats i flera kliniska koststudier (1, 2). Inte minst handlar det om den så kallade Medelhavskosten (3) eller ”DASH-dieten” (4) som är rik på grönsaker och innehåller lite salt.
Frågan är då, vad det är specifikt i dessa typer av ”hälsodieter” som bidrar till de önskvärda fysiologiska effekterna? Mest sannolikt handlar det inte om en enskild komponent, utan snarare samspelet mellan olika ämnen i kosten – eller bidraget från flera. Det kan vara vitaminer, mineraler, fibrer och antioxidanter.
Innehållet av elektrolyten nitrat är värt lite extra uppmärksamhet. Flera olika grönsaker, däribland grönbladig sallat – i synnerhet spenat och ruccola, och rödbetor – innehåller nämligen höga nivåer av nitrat. Rödbetan innehåller förutom nitrat även vitaminer och mineraler som C-vitamin, folat, kalium och zink. Den är även rik på fytokemikalier (bioaktiva skyddande ämnen som finns till exempel i frukt och bär) och växtpigmentet betalainer som ger betan dess rödlila färg, och som har visat sig vara hälsofrämjande.
Nitrat-nitrit-kväveoxid-systemet
I drygt ett par decennier har det varit känt att nitrat i kroppen, med hjälp av bakterier i munhålan, kan omvandlas till nitrit som i sin tur via olika icke-enzymatiska och enzymatiska processer kan reduceras och bilda reaktiva kväveoxidföreningar, inklusive den bioaktiva molekylen kväveoxid (Figur 1). Kväveoxid är en kortlivad radikal (molekyl som lätt reagerar med andra ämnen i kroppen) som vanligtvis bildas från aminosyran L-arginin i olika vävnader med hjälp av enzymet kväveoxidsyntas, förkortat NOS. I synnerhet sker det på insidan, endotelet, av blodkärlen. Kväveoxid spelar en betydande roll för att reglera en mängd olika fysiologiska processer i kroppen och då framför allt kardiovaskulära funktioner, exempelvis spänning och tryck i blodkärl, koagulering, och nybildning av blodkärl (5-7). Men kväveoxiden är också viktig för reglering av nervsignalering, immunsystemets funktion och för protein- och mitokondriefunktion.
I samband med naturligt åldrande och vid olika sjukdomar som förknippas med en osund livsstil, till exempel hjärtkärlsjukdomar, typ 2-diabetes och kronisk njursvikt – är funktionen av kväveoxidsyntas i blodkärlen ofta försämrad vilket leder till minskade nivåer av kväveoxid (6, 7). Minskad bildning och/eller signalering via kväveoxid har kopplats till bland annat högt blodtryck, försämrad blodkärlsfunktion, förhöjda blodfettsnivåer, ateroskleros, diabetes och störd njurfunktion (6-8). Studier visar att kost eller mediciner som ökar produktion och biotillgänglighet av kväveoxid kan förhindra utveckling eller försämring av ovan nämnda sjukdomar. Ett sätt kan vara att stimulera nitrat-nitrit-kväveoxid-systemet, oberoende av enzymet kväveoxidsyntas, med hjälp av ökat dietärt nitratintag (Figur 1).

Intag av nitrat sänker blodtrycket och skyddar kärlen
Mer än 1,5 miljarder människor världen över uppskattas ha högt blodtryck, och detta är kvantitativt den överlägset viktigaste riskfaktorn för hjärtkärlsjukdom (WHO). Högt blodtryck står för minst 50 procent av alla dödsfall på grund av ischemisk hjärtsjukdom (hjärtinfarkt) och stroke. Den första studien som visade att intag av nitrat kan sänka blodtrycket publicerades 2006 (9). I denna studie på unga friska individer gavs nitrat i dosen 0.1 mmol/kg kroppsvikt per dag under tre dagar, vilket signifikant ökade nitrat- och nitritnivåerna i blodplasman – och sänkte medelvärdet på artärtrycket med 3.2 mmHg. Den dagliga nitratdosen som användes i studien – cirka 400 mg för en person som väger 70 kilo – motsvarar den mängd som normalt finns i 200 gram av nitratrika grönsaker, som till exempel rödbetor eller grönbladig sallat.
I en efterföljande klinisk studie 2008, från en annan forskargrupp, på friska individer fick deltagarna en halvliter rödbetsjuice motsvarande en nitratdos på 23 mmol (10). Detta var cirka tre gånger högre daglig dos än i studien från 2006. Med den högre dosen noterades en större sänkning av blodtrycket tre timmar efter intaget (systoliskt tryck: -10.4 mmHg; diastoliskt tryck: -8 mmHg). Denna blodtryckssänkande effekt korrelerade med den maximala ökningen av nitrit i blodplasman. Samma forskargrupp har även visat att nitrat i form av rödbetsjuice (250-500 ml) eller som kapslar med kaliumnitrat (8-23 mmol), förhindrar akut dysfunktion i underarmens blodkärl orsakade av ett tillfälligt stopp av blodflödet (10, 11). Dessutom minskade signifikant blodplättarnas förmåga att klumpas ihop vilket kan minska risken för blodproppar.
De gynnsamma effekter som beskrivits ovan gäller friska individer. Den första kliniska studien där man undersökte de mer långsiktiga effekterna av ökat nitratintag hos patienter med högt blodtryck kom 2015. I denna studie, där patienterna under fyra veckor drack 250 ml nitratrik rödbetsjuice per dag (motsvarande 0.1 mmol/kg/dag = cirka 400 mg hos en 70 kg individ) sågs en signifikant och varaktig blodtryckssänkning (systoliskt tryck: -8 mmHg; diastoliskt tryck: -4 mmHg) jämfört med intag av en speciellt framtagen rödbetsjuice utan något innehåll av nitrat (så kallad placebo) (12).
Sedan dessa fynd publicerades så har åtskilliga efterföljande kliniska och experimentella studier gjorts för att vidare undersöka de bakomliggande mekanismerna för blodtryckssänkningen och de kärlskyddande effekterna (13). Dessutom har forskare också studerat potentiellt gynnsamma effekter vid andra typer av hjärtkärlsjukdomar och komplikationer associerade med njursvikt och metabola sjukdomar (8, 14). Detta diskuteras mer i senare delen av artikeln.
När det gäller de observerade effekterna på blodtrycket efter intag av nitrat är det viktigt att komma ihåg att kopplingen mellan högt blodtryck och risken för allvarliga kardiovaskulära komplikationer inklusive hjärtinfarkt och stroke inte är linjär utan snarare exponentiell. För en patient med högt blodtryck motsvarar en sänkning av blodtrycket med 10 mmHg en cirka 30 procent minskad risk för att drabbas av stroke (15). Med detta i åtanke så är de gynnsamma effekterna som observerats efter ökat intag av nitratrik kost – ofta i form av rödbetsjuice – att betrakta som påtagliga och högst relevanta att använda för att förebygga kardiovaskulära sjukdomar. Större kliniska studier är dock nödvändiga för att vidare studera och bevisa detta.
Intag av nitrat och effekter på njurfunktion
Njurarna spelar en central roll för att upprätthålla normal vatten- och elektrolytbalans i kroppen, och har i och med detta en stor betydelse för regleringen av blodtrycket (16). Njurfunktionen minskar successivt ju äldre vi blir. Samtidigt sker ofta en ökning av blodtrycket vilket ökar risken för kardiovaskulära sjukdomar och allvarliga komplikationer. I likhet med hjärtkärlsystemet så spelar kväveoxid en viktig roll för att reglera njurfunktionen. Minskad produktion och biotillgänglighet av kväveoxid har också kopplats till mild, måttlig eller allvarlig njursjukdom (7, 17).
I flera experimentella studier där olika modeller för akut och kronisk njursjukdom använts har man sett att tillskott av nitrat via kosten (supplementering med 0.1-1.0 mmol/kg kroppsvikt/dag), för att stimulera nitrat-nitrit-kväveoxid-systemet, leder till att njurfunktionen bättre bevaras och minskar risken för att utveckla olika varianter av njursvikt (7, 14). Som en följd av dessa experimentella studier har flera mekanismer föreslagits bidra till de observerade gynnsamma effekterna av nitrattillskott.
Bland dessa är följande mekanismer ofta återkommande och anses därför vara av speciellt viktig betydelse: minskad oxidativ stress och skadlig inverkan av så kallade reaktiva fria radikaler, ökad funktion av antioxidativa system, ökad biotillgänglighet för kväveoxid, minskad aktivitet av det blodtrycksreglerande hormonella systemet renin-angiotensin-aldosteron-systemet (RAAS), dämpad sympatisk nervaktivitet, modulerad funktion av immunsystemet och förbättrad mitokondriefunktion (7, 14).
En systematisk litteraturöversikt med metaanalys som undersökte olika modifierbara livsstilsfaktorer visade att högre grönsaksintag signifikant minskade risken för kronisk njursvikt (18). I vilken utsträckning denna effekt kan vara specifikt kopplad till det ökade intaget av nitrat är okänt. Hittills har ingen placebokontrollerad klinisk studie undersökt de långsiktiga effekterna av nitrattillskott hos patienter med njursjukdom.
En studie på patienter med kronisk njursvikt (stadie 2–4) visade dock en signifikant minskning av blodtrycket och resistensen i njurens blodkärl fyra timmar efter en engångsdos av nitrat (300 mg) (19). När det gäller de kortsiktiga effekterna av tillskott av nitrat (0.1 mmol/kg/dag) hos unga friska individer så såg man däremot inga signifikanta effekter på njurfunktionen efter en veckas tillskott jämfört med placebo (20). Slutsatsen från en epidemiologisk studie med en uppföljningsperiod på sex år var att ett högt intag av nitrat, och/eller nitrit från naturliga kostkällor, var associerat med en signifikant minskad risk för högt blodtryck och kronisk njursvikt (21).
Ett problem hos många patienter med avancerad njursjukdom är minskad fysisk kapacitet och träningsförmåga vilket påverkar livskvaliteten. I en nyligen publicerad studie visade man att intag av nitratrik rödbetsjuice (12.6 mmol = 781 mg nitrat) signifikant förbättrade träningskapacitet och uthållighet hos patienter med kronisk njursvikt (stadie 3-4) (22). Framtida längre kliniska placebo-kontrollerade studier behövs för att undersöka betydelsen av nitrattillskott för att motverka utveckling eller försämring av kronisk njursvikt samt associerade hjärt-kärl-komplikationer.
Förhöjda kaliumnivåer i serum (hyperkalemi) är vanligt förekommande hos individer med kronisk njursvikt och detta har associerats med ökad risk för kardiovaskulära komplikationer (23, 24). Det finns ett potentiellt problem att beakta vid upprepad användning av rödbetsjuice. Detta eftersom sambandet mellan förhöjda kaliumnivåer och risken för sjuklighet och dödlighet hos patienter med allvarlig njursjukdom och kronisk dialys ofta har diskuterats (25, 26) och ibland ifrågasatts (27). De nitratrika koncentrerade rödbetsjuicer som använts i många kliniska studier innehåller nämligen relativt höga halter av kalium (till exempel produkter som innehåller 850 mg kalium per 70 ml). Om detta skulle innebära att kroppens reglering av kalium riskerar att påverkas kan kombination med de nya kalium-bindarna sannolikt förhindra detta (27).
Metabola effekter av intag av nitrat
Förbättrad mitokondriefunktion och prestationsförmåga
Cellernas mitokondrier spelar en central roll i kroppens metabolism genom att med hjälp av syre och näringsämnen producera energi i form av adenosintrifosfat (ATP). En av de första studierna på människa som visade att nitrattillskott i kosten kan förbättra prestationsförmågan vid fysisk träning publicerades 2007 (28). I denna studie på friska unga män drogs slutsatsen att intag av nitrat (0.1 mmol/kg/dag), i en mängd motsvarande det som kan uppnås genom ökat intag av grönsaker, minskar syrebehovet vid submaximal fysisk kroppsansträngning. Mekanismen för denna gynnsamma effekt klarlagdes inte, även om man spekulerade att ökad bildning av bioaktiva kväveoxider inklusive nitrit och kväveoxid kan förbättra blodflödet till den arbetande muskeln och påverka mitokondriernas funktion.
Ett uppföljande arbete från samma forskargrupp visade att samma tillskott med nitrat under tre dagar påverkade basal mitokondriefunktion så att behovet av molekylärt syre för att producera ATP minskar (29). Dessa fynd ansågs ha potentiella gynnsamma konsekvenser för träningsfysiologi och livsstilsrelaterade störningar som involverar dysfunktionella mitokondrier.
Idag används nitratrik rödbetsjuice av såväl motionärer som elitidrottare för att förbättra prestationsförmågan. Även om effekten anses vara relativt liten, cirka 3 till 5 procent – och att alla inte svarar på nitrat – så kan ju detta få stor betydelse för prestationen vid tävling på hög belastningsnivå i elitsammanhang eller för äldre där mitokondriefunktionen ofta är nedsatt eller störd (30, 31).
Gynnsamma effekter vid metabol sjukdom
Under de senaste decennierna har förekomsten av övervikt och fetma i samhället ökat dramatiskt över i princip hela världen. Följaktligen har antalet personer som drabbats av och lider av metabolt syndrom nu nått epidemiska proportioner (WHO). Det metabola syndromet är ett kluster av riskfaktorer som ökar risken för bland annat hjärtkärlsjukdom och typ 2-diabetes (32). Det har gjorts försök att identifiera en gemensam underliggande molekylär mekanism som kan förklara olika aspekter av metabolt syndrom. En sådan potentiell mekanism som kopplar samman metabola och kardiovaskulära sjukdomar hos människor är minskad biotillgänglighet av kväveoxid i bland annat blodkärlens väggar.
I en studie från 2010 visade man för första gången att tillskott med nitrat kan ta bort i princip alla karakteristika för det metabola syndromet hos åldrande möss som saknar funktionellt kväveoxidsyntas i blodkärlen (33). I en senare uppföljande studie som även innefattade experimentella studier på celler från människa visade man att nitrattillskott via kosten, för att stimulera ökad bildning av kväveoxid, skyddade mot utveckling av högfettdiet-inducerad fettlever (34) vilket är ett stort och ännu olöst kliniskt problem vid kardiometabola sjukdomar (8). Dessa fynd med koppling till nitrat-nitrit-kväveoxid-systemet vid metabol reglering, har idag reproducerats och diskuterats av flera olika forskargrupper och kan ha kliniska implikationer för att med kost förebygga och eventuellt behandla metabol dysfunktion och associerade komplikationer (8). Kliniska studier planeras nu för att undersöka de potentiellt gynnsamma metabola och kardiovaskulära effekterna av nitratrik koncentrerad rödbetsjuice hos patienter med typ 2-diabetes och samtidigt jämföra med vanligt förekommande antidiabetiska läkemedel, till exempel metformin.
Risker med att få i sig för mycket nitrat?
Finns det då några kända hälsorisker med att äta mycket nitratrika grönsaker, dricka rödbetsjuice eller smoothies med spenat regelbundet? Grönsaker som diskuterats ovan är inte bara en källa för nitrat utan innehåller även kalium som är viktigt för flera funktioner i kroppen (bland annat nerv- och muskelfunktion samt hjärtkärlfunktion). Intag av koncentrerad rödbetsjuice har ibland associerats med magont vilket sannolikt kan förklaras av kalium-orsakad retning av magslemhinnan, men detta kan till stor del undvikas genom samtidigt matintag.
Som nämnts tidigare i artikeln så ska individer med kraftigt nedsatt njurfunktion vara försiktiga med alltför mycket kalium i kosten då detta kan öka dess plasmakoncentration och i sin tur påverka hjärta och kärl negativt. Det finns dock inga tydliga data från kliniska studier, där nitrat-supplementering i form av rödbetsjuice använts, faktiskt påverkat plasmanivåerna av kalium eller har haft negativ inverkan på hjärtkärlfunktionen.
En annan aspekt man bör ha i åtanke, om man regelbundet dricker rödbetsjuice, är att denna juice innehåller ganska mycket socker. Detta är i allmänhet inget problem om man har normal metabol funktion, men för individer med diabetes som ska vara försiktiga med sitt sockerintag så bör man vara uppmärksam på detta. Rekommendationen är i sådana fall att kontrollera sockerinnehållet på rödbetsjuicen man använder och att intag av denna sker i samband med annan måltid för att undvika onödiga svängningar i glukos-insulin-balansen. Detta är dock inte väl studerat, men kliniska studier på patienter med typ 2-diabetes planeras där bland annat metabola funktioner kommer att undersökas.
Slutligen bör nämnas att höga nivåer av nitrit (molekylen som bildas efter reduktion av nitrat) har associerats med methemoglobinemi (nedsatt syretransporterande förmåga till följd av oxidation av hemoglobinmolekylen). Detta gäller framför allt små barn och bebisar (yngre än 6 månader) som är mer känsliga. När det gäller risken för att drabbas av nitrit-inducerad methemoglobinemi hos en vuxen individ till följd av dietärt nitratintag (i form av grönsaker eller rödbetsjuice), så måste detta betraktas som högst osannolikt då nivåerna av nitrit i blodet efter intagen mängd nitrat endast är marginellt förhöjda. Methemoglobinemi är mycket ovanligt och mängderna nitrit som vi normalt får i oss är långt under de mängder som man har sett orsaka methemoglobinemi.
Hur mycket nitrat behöver man få i sig för att det ska ge effekt?
Grönsaker såsom grönbladig sallat och rödbeta innehåller alla ganska mycket nitrat, även om mängderna kan variera något beroende på producent och tidpunkt på året. Nitratmängden i de koncentrerade rödbetsjuicer som använts i många kliniska studier, och som intas en till två gånger dagligen, innehåller cirka 300-600 mg nitrat och motsvarar ungefär den mängd som finns i en tallrik med spenat och ruccola eller i en stor rödbeta. Som diskuterats ovan så anses nitratintag i dessa mängder inte vara associerat med några risker, utan snarare ha flera potentiellt gynnsamma effekter på en rad olika funktioner i kroppen. Det kan möjligen vara så att även mindre dagliga mängder nitrat har hälsofrämjande effekter, men detta har dock inte studerats väl i några större kliniska studier.
Klinisk betydelse och framtida perspektiv på intag av nitrat
Experimentella sjukdomsmodeller och kliniska studier på friska individer och patienter med hjärtkärlsjukdom har visat en rad gynnsamma kardiovaskulära effekter av nitrattillskott via kosten, inklusive blodtryckssänkning och förbättrad funktion av blodkärlen (13). Flera olika organsystem är involverade i aktiveringen av nitrat-nitrit-kväveoxid-systemet efter nitratintag. Men verkningsmekanismerna är i hög grad kopplade till minskad oxidativ stress och ökad produktion och biotillgänglighet av kväveoxid (13). Större placebo-kontrollerade kliniska studier är dock nödvändiga för att vidare studera och befästa dessa fynd.
Flera experimentella studier har gjorts med nitrattillskott i kosten som visat gynnsamma effekter på njurfunktion och kroppens metabolism (7, 8, 14). Det gäller också mindre kliniska studier som bland annat visar att stimulering av nitrat-nitrit-kväveoxid-systemet kan minska kärlresistansen och förbättra blodflödet i njurarna, förbättra mitokondriefunktionen, minska syrebehovet och därmed öka prestationsförmågan vid fysiskt arbete (19, 20, 28, 29).
I dagsläget saknas fortfarande större och mer långsiktiga kliniska studier vid kronisk njursjukdom och diabetes. Dessutom kommer större epidemiologiska koststudier med fokus på nitratintag i sig vara av intresse för att belysa de näringsmässiga aspekterna, men också påverkan på hjärt-kärl, njurar och de metabola funktionerna.
Sådana studier skulle kunna bidra till mer specifika kostråd för nitratrika grönsaker, som ett sätt att förebygga och förhindra utveckling av hjärtkärlsjukdom, njursvikt och metabola sjukdomar inklusive övervikt/fetma och typ 2-diabetes (Figur 1). Framtida studier på olika hälsoaspekter efter nitrattillskott bör dessutom beakta olika former av nitratkällor i kosten (till exempel fast eller flytande form, koncentrerad liten volym eller utspädd större volym), eftersom de har rapporterats kunna påverka bioaktiveringen av nitrat och därmed dess gynnsamma effekter (35). I denna kliniska studie på 10 friska försökspersoner jämfördes intaget av 5.76 mmol nitrat i form av en koncentrerad rödbetsjuicedryck (55 ml), en icke-koncentrerad rödbetsjuicedryck (456 ml) och en fast variant av rödbetsjuice (60 g). Fler och större studier är nödvändiga, men från denna studie drog man slutsatsen att konsumtion av en liten, koncentrerad nitratrik juice var det mest effektiva sättet att sänka blodtrycket.
Författaren uppger inga jävsförhållanden.
Referenser
1. K. Arnotti, M. D. Bamber, V. Brewer, Dietary interventions and blood pressure in overweight or obese individuals: A systematic review and meta-analysis. Clin Nutr 41, 1001-1012, 2022.
2. H. Mozaffari, S. Ajabshir, S. Alizadeh, Dietary Approaches to Stop Hypertension and risk of chronic kidney disease: A systematic review and meta-analysis of observational studies. Clin Nutr 39, 2035-2044, 2020.
3. M. A. Martinez-Gonzalez, A. Gea, M. Ruiz-Canela, The Mediterranean Diet and Cardiovascular Health. Circ Res 124, 779-798, 2019.
4. M. Siervo et al., Effects of the Dietary Approach to Stop Hypertension (DA SH) diet on cardiovascular risk factors: a systematic review and meta-analysis. Br J Nutr 113, 1-15, 2015.
5. U. Forstermann, W. C. Sessa, Nitric oxide synthases: regulation and function. Eur Heart J 33, 829-837, 837a-837d, 2012.
6. J. O. Lundberg, M. T. Gladwin, E. Weitzberg, Strategies to increase nitric oxide signalling in cardiovascular disease. Nat Rev Drug Discov 14, 623-641, 2015.
7. M. Carlstrom, Nitric oxide signalling in kidney regulation and cardiometabolic health. Nat Rev Nephrol 17, 575-590, 2021.
8. J. O. Lundberg, M. Carlstrom, E. Weitzberg, Metabolic Effects of Dietary Nitrate in Health and Disease. Cell Metab 28, 9-22, 2018.
9. F. J. Larsen, B. Ekblom, K. Sahlin, J. O. Lundberg, E. Weitzberg, Effects of dietary nitrate on blood pressure in healthy volunteers. N Engl J Med 355, 2792-2793, 2006.
10. A. J. Webb et al., Acute blood pressure lowering, vasoprotective, and antiplatelet properties of dietary nitrate via bioconversion to nitrite. Hypertension 51, 784-790, 2008.
11. S. Velmurugan et al., Antiplatelet effects of dietary nitrate in healthy volunteers: involvement of cGMP and influence of sex. Free Radic Biol Med 65, 1521-1532, 2013.
12. V. Kapil, R. S. Khambata, A. Robertson, M. J. Caulfield, A. Ahluwalia, Dietary nitrate provides sustained blood pressure lowering in hypertensive patients: a randomized, phase 2, double-blind, placebo-controlled study. Hypertension 65, 320-327, 2015.
13. M. Carlstrom, J. O. Lundberg, E. Weitzberg, Mechanisms underlying blood pressure reduction by dietary inorganic nitrate. Acta Physiol (Oxf) 224, e13080, 2018.
14. M. Carlstrom, M. F. Montenegro, Therapeutic value of stimulating the nitrate-nitrite-nitric oxide pathway to attenuate oxidative stress and restore nitric oxide bioavailability in cardiorenal disease. Journal of internal medicine 285, 2-18, 2019.
15. D. Ettehad et al., Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet 387, 957-967, 2016.
16. M. Carlstrom, C. S. Wilcox, W. J. Arendshorst, Renal autoregulation in health and disease. Physiol Rev 95, 405-511, 2015.
17. C. Baylis, Arginine, arginine analogs and nitric oxide production in chronic kidney disease. Nat Clin Pract Nephrol 2, 209-220, 2006.
18. J. T. Kelly et al., Modifiable Lifestyle Factors for Primary Prevention of CKD: A Systematic Review and Meta-Analysis. J Am Soc Nephrol 32, 239-253, 2021.
19. S. Kemmner et al., Dietary nitrate load lowers blood pressure and renal resistive index in patients with chronic kidney disease: A pilot study. Nitric Oxide 64, 7-15, 2017.
20. A. Carpentier, S. Stragier, C. Brejeon, J. R. Poortmans, Nitrate Supplementation, Exercise, and Kidney Function: Are There Detrimental Effects? Med Sci Sports Exerc 47, 1519-1522, 2015.
21. Z. Bahadoran et al., Association between Dietary Intakes of Nitrate and Nitrite and the Risk of Hypertension and Chronic Kidney Disease: Tehran Lipid and Glucose Study. Nutrients 8, 2016.
22. M. G. Ramick et al., The effect of dietary nitrate on exercise capacity in chronic kidney disease: a randomized controlled pilot study. Nitric Oxide 106, 17-23, 2021.
23. S. Kohsaka, S. Okami, E. Kanda, N. Kashihara, T. Yajima, Cardiovascular and Renal Outcomes Associated With Hyperkalemia in Chronic Kidney Disease: A Hospital-Based Cohort Study. Mayo Clin Proc Innov Qual Outcomes 5, 274-285, 2021.
24. G. James et al., Serum potassium variability as a predictor of clinical outcomes in patients with cardiorenal disease or diabetes: a retrospective UK database study. Clin Kidney J 15, 758-770, 2022.
25. E. N. M. de Rooij et al., Serum Potassium and Mortality Risk in Hemodialysis Patients: A Cohort Study. Kidney Med 4, 100379, 2022.
26. K. T. Chen et al., Efficacy and Safety of Mineralocorticoid Receptor Antagonists in Kidney Failure Patients Treated with Dialysis: A Systematic Review and Meta-Analysis. Clin J Am Soc Nephrol 16, 916-925, 2021.
27. B. F. Palmer, G. Colbert, D. J. Clegg, Potassium Homeostasis, Chronic Kidney Disease, and the Plant-Enriched Diets. Kidney360 1, 65-71, 2020.
28. F. J. Larsen, E. Weitzberg, J. O. Lundberg, B. Ekblom, Effects of dietary nitrate on oxygen cost during exercise. Acta Physiol (Oxf) 191, 59-66, 2007.
29. F. J. Larsen et al., Dietary inorganic nitrate improves mitochondrial efficiency in humans. Cell Metab 13, 149-159, 2011.
30. R. Dominguez et al., Effects of Beetroot Juice Supplementation on Cardiorespiratory Endurance in Athletes. A Systematic Review. Nutrients 9, 2017.
31. L. Stanaway, K. Rutherfurd-Markwick, R. Page, A. Ali, Performance and Health Benefits of Dietary Nitrate Supplementation in Older Adults: A Systematic Review. Nutrients 9, 2017.
32. P. W. Wilson, R. B. D’Agostino, H. Parise, L. Sullivan, J. B. Meigs, Metabolic syndrome as a precursor of cardiovascular disease and type 2 diabetes mellitus. Circulation 112, 3066-3072, 2005.
33. M. Carlstrom et al., Dietary inorganic nitrate reverses features of metabolic syndrome in endothelial nitric oxide synthase-deficient mice. Proc Natl Acad Sci U S A 107, 17716-17720, 2010.
34. I. Cordero-Herrera et al., AMP-activated protein kinase activation and NADPH oxidase inhibition by inorganic nitrate and nitrite prevent liver steatosis. Proc Natl Acad Sci U S A 116, 217-226, 2019.
35. S. T. J. McDonagh, L. J. Wylie, J. M. A. Webster, A. Vanhatalo, A. M. Jones, Influence of dietary nitrate food forms on nitrate metabolism and blood pressure in healthy normotensive adults. Nitric Oxide 72, 66-74, 2018.
Evidensbaserat arbete för dietister
Referat
Dietisternas Riksförbunds kongress 2022 arrangerades digitalt den 23-24 mars. Programmet tog avstamp i evidensbaserat arbete och hållbar nutrition. Föreläsningarna handlade bland annat om hållbara matsystem, kost vid njursvikt, äldre och nutrition och mat och träning. Här följer korta rapporter från delar av det intressanta innehållet.
>>text: Kajsa Asp Jonson, leg dietist, journalist, Kajsa Asp kommunikation, Göteborg
Hållbarhet kopplat till mat
Inledningstalare var Amanda Wood, forskare vid Stockholm Resilience Centre. Hon konstaterade att hållbarhet är en komplex fråga och när det gäller mat innefattas såväl miljö- och klimatmässig hållbarhet som ekonomiska och sociala frågor, inklusive hälsoaspekter.
Ett hälsosamt matmönster är ofta även skonsamt för miljö och klimat, men det finns undantag och många perspektiv att ta hänsyn till. Några exempel:
- En ekologiskt odlad sockerbeta – råvaran är klimatsmart, men produkterna som görs av den är oftast inte hälsosamma
- En lunchtallrik med grönsaker och fisk – hållbart för hälsan, men avtrycket på klimat och miljö varierar beroende på var och hur ingredienserna odlas och produceras
- En skål med nötter – nötter och frön är bra för hälsan, men miljöpåverkan avgörs av hur de har odlats
Matvanor som är mer hälsosamma än befolkningens genomsnitt är som regel även mer miljömässigt hållbara. Grönsaker, baljväxter och fullkorn påverkar hälsan positivt och har generellt sett låg miljöpåverkan. Socker och raffinerade kolhydratskällor är ett av undantagen, med låg miljöpåverkan och negativ påverkan på hälsan.
Processat kött har negativa effekter på såväl hälsa som klimat och miljö, och animaliska produkter står för två tredjedelar av växthusgaserna. Men kött bidrar även med viktig näring. Dessutom kan djuren beta på icke odlingsbar mark och bidra till biologisk mångfald. Ultraprocessad mat har ofta stor negativ påverkan på både hälsan och miljön och forskning pågår för att kartlägga klimatavtrycket från vegetarisk färdigmat och nya proteinkällor.
En produkts miljöpåverkan kommer till största del från produktionen och kan mätas på många olika sätt, till exempel koldioxidekvivalenter per 100 gram av produkten, per 100 gram protein, eller per 100 kcal. Andra viktiga aspekter är markanvändning, färskvattenåtgång och biodiversitet.
Hur ser då en hälsosam och miljömässigt hållbar kost ut i Sverige? I stora drag är den växtbaserad med en hög andel spannmål, grönsaker, rotfrukter, frukt, bär, baljväxter, nötter, vegetabiliska oljor och sjömat (tidigt i näringskedjan), och mindre andel sötsaker, alkohol och ultraprocessad mat.
”Det är viktigt att se till både människans och planetens bästa”, avslutade Amanda Wood som rekommenderar Matkalkylatorn.se, WWF matguiden, Livsmedelsverkets ”Hitta ditt sätt” och kommande nordiska näringsrekommendationer för vidare fördjupning.
Evidensbaserad kostbehandling vid njursvikt
Karin Windahl, dietist med specialistkompetens i njurmedicin på Danderyds sjukhus och doktorand vid Karolinska institutet, presenterade aktuell forskning och riktlinjer. Evidens finns för att proteinreducerad kost bidrar till symtomlindring vid försämrad njurfunktion.
ESPEN guidelines vid njursvikt inkluderar forskning fram till 2020. KDOQI (Kidney Disease Outcomes Quality Initiative) har bedömt 15 000 studier utifrån GRADE-systemet. Randomiserade kontrollerade studier (RCT) har högst bevisvärde och i den här patientgruppen har även observationsstudier högt bevisvärde. GRADE är ett internationellt system för att gradera styrkan av det samlade vetenskapliga underlaget i en viss fråga. Med hjälp av GRADE görs en övergripande värdering som visar hur vetenskapligt underbyggd en slutsats är.
Nationellt programområde (NPO) inom njurmedicin inriktas på primärvårdens förebyggande åtgärder, inklusive enklare kostråd kring hälsosamma matvanor. Njursjukdom som kräver proteinreducerad kost bör vara specialistsjukvårdens ansvar enligt Karin Windahl.
Växtbaserat förebygger komplikationer vid njursjukdom
Juan-Jesus Carrero, professor i epidemiologi vid Karolinska Institutet, konstaterade att det är hälsosamt att äta mer av växtbaserade livsmedel, även för personer med nedsatt njurfunktion. ”Men det behöver inte vara vegetariskt, och växtbaserad kost är ingen garanti för hälsosamma matvanor – näringsinnehåll och tillagningsmetoder är mer avgörande”, berättade han.
Grönsaker och frukt bidrar till lägre sjukdomsrisk totalt sett. Synergieffekterna är många, bland annat av kostfibrer. Fibrer har stor betydelse som prebiotika, vilket är positivt för tarmbakterierna och tarmbarriären, och glykemisk kontroll samt bidrar till mindre inflammation och minskad produktion av kvävehaltiga nedbrytningsprodukter som kan ansamlas i blodet (uremiska ämnen).
”Hälsosamma matvanor lägger en viktig grund för all behandling och kan bromsa njursjukdomens utveckling, samt minska risken för andra sjukdomar och förtida död”, sa Juan-Jesus Carrero.
Äldre och nutrition
Olivia Wigzell, generaldirektör på Socialstyrelsen och regeringens särskilda utredare inom nutrition, betonade att arbetet kring äldres hälsa bör vara teambaserat, framåtlutat och förebyggande.
Äldres levnadsvanor är ett högprioriterat område hos Socialstyrelsen. Arbete med åtgärdsförslag och utbildningar pågår för att stärka såväl psykisk som fysisk hälsa, vilket även inkluderar nutrition. Vårdtagarna i äldreomsorgen har ofta komplexa vårdbehov, och medicinsk kompetens behöver stärkas inom alla kompetensområden. På uppdrag av regeringen inrättas Kompetenscentrum för vård och omsorg för äldre i augusti.
Trycksår, undernäring, fallskador och munhälsa följs via kvalitetsregistret Senior alert som även är ett verktyg för att stödja vårdprevention. Riktlinjer för tandvård har nyligen uppdaterats och kompletterats med en webbutbildning om munhälsa. Lägesrapporten ”Vård och omsorg hos äldre” presenterades i mars 2022. På Kunskapsguiden.se finns kunskapsstöd för olika områden, bland annat Mat och näring för äldre personer.
I Äldreomsorgslagen som kommer att föreslås under våren skärps kraven på äldreomsorgens förebyggande och hälsofrämjande perspektiv. Vården ska bli mer likvärdig och stödja individens funktionsförmåga. Arbetet knyter an till omställningen till god och nära vård där fokus ligger på personcentrering, hälsofrämjande, förebyggande och rehabiliterande arbete samt vård efter behov och på lika villkor. Förslagen stärker styrningen av primärvården, både på ledningsnivå och verksamhetsnära. Kommunens hälso- och sjukvårdsansvar ska tydliggöras och utformning och gemensam plan görs i samverkan mellan kommun och primärvård. Lagen behöver kompletteras med kartläggningar av kommunernas resursbehov.
Enligt Olivia Wigzell behövs dietister både i klinisk verksamhet och på högre övergripande nivå för att skapa rutiner och arbetssätt och bidra till att nutritionsfrågor prioriteras högre. Både det patientnära perspektivet och det förebyggande arbetet med äldre som målgrupp behöver få högre prioritet.
Kroppssammansättning visar nutritionsstatus
Isabell Stahlén, dietist vid Mälarsjukhuset och doktorand vid Uppsala universitet, gav en grundlig genomgång av hur kroppssammansättning kan användas vid bedömning och uppföljning av nutritionsstatus.
Antropometriska mått såsom Body Mass Index (BMI) och midjeomfång är enkla att använda men påvisar till exempel inte vätskeansamlingar eller förändringar i muskelmassa. För att veta hur fettmassa respektive fettfri massa fördelas och förändras behöver kroppssammansättningen mätas, till exempel med datortomografi, magnetröntgen, DEXA (Dual-energy X-ray absorptiometry) eller bioelektrisk impedans.
Information om kroppssammansättningen är betydelsefull för hela teamet och bidrar ofta till ökad motivation hos patienten. Nutritionsstatus kan följas vid till exempel cancerbehandling, risk för sarkopeni (nedsatt muskelstyrka och minskad muskelmassa) eller långvarig kortisonbehandling när man vill undersöka om övervätskning maskerar en faktisk viktnedgång enligt Isabell Stahlén.
Börja med barnen!
Peter Almgren, barnläkare och regeringens särskilda utredare, presenterade Sammanhållen god och nära vård för barn och unga vars uppdrag varit att kartlägga förutsättningar och föreslå satsningar för en mer likvärdig vård och hälsofrämjande insatser för barn och unga.
Det är en utmaning att följa ett barn från graviditet och småbarnsåren, genom uppväxten fram till vuxen ålder – det finns en mängd aktörer och huvudmän, olika vårdnivåer, kommunalt självstyre samt fritt vårdval och fritt skolval, konstaterade Peter Almgren. Nationell styrning av hälsofrämjande förebyggande arbete för barn och unga lägger grunden för all förebyggande vård, och behöver förtydligas.
Utredningens förslag är bland annat att hälsofrämjande arbete för barn och unga ska lyftas fram i hälso- och sjukvårdslagen. Ett nationellt hälsovårdsprogram ska tydliggöra vilket stöd barn och unga och deras föräldrar erbjuds i form av hälsobesök under uppväxten. Insatserna ska göras tillgängliga för alla (universell nivå) och riktade insatser ska ges till de som behöver. Barnperspektivet ska lyftas fram och det ska bli enklare att få en fast vårdkontakt. Skolhälsovården ska fortsatt vara ansvarig för elevhälsan, och samverkar med regionen som är huvudman för samlad hälsouppföljning. Samverkan mellan vård, skola, tandvård och socialtjänst behöver stärkas, liksom övergången från vård för barn till vård för vuxna.
Ett stort fokus ligger på att stärka den psykiska hälsan, bland annat genom tidiga insatser och ett bredare förhållningssätt. Primärvården är första instans. Specialiserad vård, skola och socialtjänst ska samordnas kring barn med långsiktiga behov och ett viktigt mål är att BUP (barn- och ungdomspsykiatri) ska vara köfri.
Det behövs en nationell heltäckande uppföljning av barns och ungas hälsa samt möjligheter att utvärdera insatser, bland annat avseende kvalitet och jämlikhet. Staten bör ha ansvar för strukturen, och journaler och övrig dokumentation bör kunna delas mellan olika vårdinstanser.
Peter Almgrens förhoppning är att utredningen ska leda till insatser och lagförslag som främjar hälsan för barn och unga.
Mat vid IBS
Stine Störsrud, överdietist och medicine doktor vid Sahlgrenska universitetssjukhuset, presenterade senaste forskningen kring kost vid IBS (irritable bowel syndrome, känslig tarm). Studier pågår runt om i världen för att kartlägga samband, symtom och mekanismer.
Kolhydrater som absorberas ofullständigt, så kallade FODMAP (Fermenterbara Oligosackarider, Disackarider, Monosackarider och Polyoler), tas om hand av bakterierna i tjocktarmen och kan orsaka symtom, ofta i form av gaser, smärta och ibland även diarré. Kostbehandling med låg mängd FODMAP kan lindra symtomen men innebär att många viktiga livsmedel utesluts. Det är därför viktigt att återintroducera dem utifrån vad varje individ tolererar.
I forskning som presenteras under våren 2022 har effekterna av låg FODMAP kombinerat med kostråd enligt NICE-guidelines jämförts med lågkolhydratkost respektive medicinsk behandling.
”Kostbehandlingen syftar till att minska symtom och näringsbrister, men minst lika viktigt är att främja matglädje och valmöjligheter för personer med IBS”, poängterade Stine Störsrud.
Mål med nutritionsbehandling
Lina Al-Aldili, dietist och doktorand vid Institutionen för Kostvetenskap, Uppsala universitet, presenterade sin forskning baserad på fokusgruppsintervjuer med dietister.
Många patienter med komplexa tillstånd har ökad risk för undernäring. Hälso- och sjukvården uppmanas till ett personcentrerat förhållningssätt och det är en utmaning för dietisten att identifiera evidensbaserade åtgärder, bjuda in till delaktighet och tillsammans med patienten sätta hållbara och realistiska mål.
Det finns ofta en diskrepans mellan kliniska mål och patientens personliga mål. Det är vanligt att viktnedgång tolkas som positivt. Förståelse och kunskap om livsmedel med högre energitäthet är en viktig del av kostbehandlingen, summerade Lina Al-Aldili.
Aktivt och hälsosamt åldrande i Norden
Äldre personer utgör en allt större andel av befolkningen i Norden. Beslutsfattare behöver tillförsäkra en god vård och omsorg, och god livskvalitet för äldre. Även WHO lyfter äldres hälsa under 2021-2030 med initiativet The decade of healthy ageing.
”Åldersvänliga städer, välfärdsteknik och arbete för en god och jämlik hälsa bidrar till ett aktivt och hälsosamt åldrande. Det främjar individens kognitiva, psykiska, sociala och fysiska förmågor”, konstaterade Pia Nevala Westman, dietist och projektledare i folkhälsofrågor vid Nordens välfärdscenter i Helsingfors, samt koordinator för Nordiskt demensnätverk.
Äldre personer är en resurs att ta vara på i samhället och det salutogena perspektivet, det vill säga med fokus på faktorer som bidrar till och vidmakthåller hälsa, behöver lyftas in. Indikatorer, det vill säga mätbara företeelser som tydliggör tillståndet i ett större system, utgör ett grundläggande ramverk för kunskapsbaserade policys, vilka anger en riktning för sakfrågorna. Dessa bäddas in i strategi, handlingsplan och riktlinjer. Gemensamma nordiska indikatorer om aktivt och hälsosamt åldrande kan bidra till en hälsofrämjande och kunskapsbaserad samhällsutveckling samt god hälsa och funktionsförmåga, social hållbarhet i framtidens vård och omsorg, och bidrar även till möjligheter för seniorer att vara aktiva och delaktiga. I Livsmedelsverkets dokument ”Indikatorer kopplade till mat” finns möjlighet till fördjupning.
Måltiden är en del av träningen
Linda Bakkman, näringsfysiolog, doktor i medicinsk vetenskap och rådgivare vid Sveriges olympiska kommitté, föreläste om idrottarens energi- och näringsmässiga utmaningar.
Parallellt med samhällets övervikts- och fetmaproblematik finns en växande grupp som är väldigt hälsomedvetna och tränar mycket. Det allmänna kostbudskapet, där låg energitäthet är en grund, är inte anpassat för idrottaren.
Träning och kost går hand i hand och tillgång till energi är en förutsättning för prestation och optimerad återhämtning. För lite mat i förhållande till behovet innebär en relativ energibrist som påverkar hela kroppen med symtom som sämre återhämtning, ”överträning”, ökad skaderisk, infektionskänslighet, hormonrubbningar, magproblem, sömnstörningar, lägre bentäthet samt ökad risk för depression berättade Linda Bakkman. Exempel på orsaker till relativ energibrist är högt energibehov, aptitlöshet, brist på tid att laga och äta mat, låg energitäthet i maten samt strävan efter viktreglering inom vissa idrotter.
Intresset för kost och idrottsnutrition är stort och det krävs god kunskap hos tränare och aktiva för att förstå individens energiförbrukning och proteinbehov. Det krävs också praktisk kunskap om hur man gör till exempel vid resor och långa tävlingsdagar konstaterade Linda Bakkman.
Framtidens mat, människor och planet
Kongressen avslutades av Andrew Merrie, forskare och kommunikatör vid Stockholm Resilience Centre, som genom storytelling åskådliggjorde tänkbara framtidsscenarion under rubriken Future earth, future human, future food – an imagination led apporoach for system transformation”.
Vår omvärld förändras ständigt och människan har makt och ansvar att påverka utvecklingen. Andrew Merrie poängterade att jordens framtid 10 000 år framåt avgörs under de närmaste femtio åren. Miljö- och klimatfaktorer som tidigare varit stabila förändras i allt snabbare takt. Kritiska brytpunkter för naturens jämvikt och oåterkalleliga klimatförändringar leder till ändrade temperaturer, omfattande torka och bränder, smältande isar och översvämning. Djurarter dör ut och vi kommer att kunna bo och leva på en allt mindre andel av jordens yta.
Ett hållbart matsystem lägger grunden för en hållbar utveckling. Mat finns med i alla FN:s globala mål och våra mat- och levnadsvanor spelar stor roll för såväl människans som planetens hälsa och framtid avslutade Andrew Merrie.
Många av föreläsningarna från kongressen kommer att publiceras på DRF:s YouTube-kanal.
Författaren uppger inga jävsförhållanden.
Kan matdonationer minska matfattigdom och ge bra näring?
Enligt FN:s förklaring om de mänskliga rättigheterna har alla rätt till en levnadsstandard som är tillräcklig för hälsa och välbefinnande, vilket inkluderar tillgång till mat. Även i ett land som Sverige, som länge varit en välfärdsstat, drabbar matfattigdom delar av befolkningen. Vi undersöker i ett forskningsprojekt matdonationer ur ett hållbarhetsperspektiv. Studien innefattar näringsmässiga och andra sociala fördelar med matdonationer till socialt och ekonomiskt utsatta. Preliminära resultat visar att matdonationer kan bidra till en säkrare tillgång till mat. Samtidigt får mottagarna pengar över att lägga på andra nödvändigheter, till exempel ytterligare matinköp, sjukvård, läkemedel, kläder, skor och andra konsumtionsvaror. Matdonationer har därför potential att bidra till en social hållbar utveckling för personer som lever i matfattigdom.
>>text: Niina Sundin, doktorand, Institutionen för energi och teknik, SLU, Uppsala; Christine Persson Osowski, docent, Avdelningen för folkhälsovetenskap, Akademin för hälsa, vård och välfärd, Mälardalens universitet, Västerås; Mattias Eriksson, docent, Institutionen för energi och teknik, SLU, Uppsala; Ingrid Strid, forskare, Institutionen för energi och teknik, SLU, Uppsala
Matfattigdom – definition och utbredning
Enligt FN:s globala mål för hållbar utveckling ska all hunger elimineras fram till 2030. I verkligheten lider idag fortfarande en av nio i världen av undernäring (1). Asien är värst drabbat av hunger.
Sverige ligger på sjunde plats på Human Development Index (HDI) och klassas därmed som ett land med mycket hög grad av utveckling och välfärd (2). Undernäring förekommer i Sverige, men det är framför allt något som drabbar äldre och i samband med sjukdom (3). Däremot är det fortfarande delar av befolkningen som upplever en brist på tillgång till mat, så kallad food insecurity.
I en studie av Borch & Kjaernes (4) var det 1,9 procent av alla deltagande svenskar som rapporterade att de ofta eller ibland upplever att man inte har tillräckligt med mat att äta. Författarna poängterar att fler studier behövs för att kunna säkerställa resultaten.
Matfattigdom kan definieras som att inte ha ekonomi som räcker till en kost av tillräcklig mängd och kvalitet för att upprätthålla en näringsriktigt tillfredsställande, socialt acceptabel diet (5, 6). Bristande ekonomiska resurser är således en bidragande orsak till matfattigdom och idag är det 6 procent av den svenska befolkningen som har så låg inkomst att det inte räcker till att bekosta levnadsomkostnader som mat, något som definieras som låg inkomststandard enligt SCB (7). Särskilt utsatta grupper för matfattigdom är EU-migranter, personer som lever av försörjningsstöd, papperslösa flyktingar och så kallade icke-mottagare. Den sista gruppen har egentligen rätt till ersättning från välfärdssystemet, men har av olika skäl inte tagit del av dem (6).
När välfärdssystemets insatser inte räcker till bidrar organisationer inom civilsamhället med insatser mot matfattigdomen (6). Stadsmissionerna är en av dessa ideella organisationer och arbetar med tre olika typer av insatser: subventionerad matförsäljning, matkassar och lagade måltider. Vid Uppsala stadsmission, där vår studie har utförts, genomförs insatser vid Matcentralen, i form av matkassar, och vid Mikaelsgården i form av färdiga måltider.
Livsmedlen som används är till stor del skänkta. Av fem ton mat som kommer från livsmedelsbutiker till Uppsala stadsmission varje vecka blir det fyra ton mat som mättar behövande människor. Verksamheten bidrar också till sociala insatser genom att bryta ensamhet och isolering. Flera personer får dessutom möjlighet att arbetsträna (8).
Matfattigdom och nutrition
Höga utgifter för mat är associerat med en mer hälsosam kost (9). Grupper med låg inkomst tenderar i sin tur att ha en sämre tillgång till livsmedel (4). Hur mycket pengar människor har möjlighet att spendera på mat får alltså betydelse för matvanorna. De med lägst inkomst tenderar att äta mer näringsfattiga och energitäta livsmedel (10), vilket sannolikt påverkar näringsstatus i negativ riktning.
Studier av hemlösas kost har visat på malnutrition, både relaterat till under- och övernutrition. Särskilt utmärkande är ett högt intag av salt, mättat fett och ett lågt intag av fibrer och vitamin C (11, 12).
De som hämtar matkassar vid Uppsala stadsmission har en disponibel inkomst under 9 300 kronor i månaden. Det är dock inte enbart disponibel inkomst i sig som avgör om kosten blir hälsosam eller inte. Faktorer som kunskap om mat och näring, lokal tillgänglighet, social situation – och att ohälsosamma livsmedel ofta är relativt billiga spelar också in (5, 13).
Studieresultat i relation till näringsintag
I vår studie gjordes en hållbarhetsbedömning utifrån alla tre dimensioner av hållbar utveckling – miljömässig, ekonomisk och social hållbarhet. Uppsala stadsmissions verksamhet Matcentralen och Mikaelsgården var fallstudie.
Här lyfter vi fram de preliminära resultaten om de näringsmässiga konsekvenserna av donerade matkassar inom ramen för social hållbar utveckling. De indikatorer vi har studerat är food security (säker tillgång till mat), dietary diversity (variation i kosten avseende livsmedelsgrupper) samt näringstätheten i matkassarna.
De preliminära resultaten visar att studiedeltagarna hade en låg grad av ”food security” vid studiens början, men att matkassarna medförde en förbättring. Men kassarna var inte tillräckligt för att ensamt säkra tillgången till mat. Statusen för ”food security” förblev låg, trots förbättringarna och vi kunde inte se någon ökad variation i kosten. Detta kan bero på att matkassarnas innehåll delades av flera familjemedlemmar. En annan orsak kan vara att matkassarna till stor del bestod av livsmedelsgrupper som deltagarna redan konsumerade, till exempel bröd, mejeriprodukter samt frukt- och grönsaker, men mindre av de livsmedelsgrupper som deltagarna åt mer sällan, såsom kött, fisk, nötter och frön. Mer forskning behövs dock för att bekräfta detta.
Förbättrad ”food security” är i linje med tidigare studier på liknande målgrupper. Skillnaden är att forskarna då även funnit en förbättrad kvalitet i kosten (14, 15). Orsaken är den näringsmässiga kvaliteten på den donerade maten, som kan variera beroende på färskvaror: frukt, grönsaker och mejeriprodukter (16, 17). Våra analyser visade att matkassarna från Uppsala stadsmission till hälften bestod av frukt och grönsaker. Övriga livsmedelsgrupper var bland annat cerealier, mejeriprodukter och drycker, till exempel kaffe. En preliminär analys av näringsinnehållet visade att matkassarna har en god näringstäthet som i stort motsvarar de nordiska näringsrekommendationerna (18).
Matkassarna innehöll makronutrienter som protein, kolhydrater och fett i proportioner inom referensvärdena. Dessutom innehöll kassarna lite socker, mycket fibrer och hade en tämligen god fettkvalitet. Matkassarna hade också en näringstäthet som huvudsakligen motsvarade referensvärdena för de flesta vitaminer och mineraler, med ett extra högt innehåll av vitamin C och E. Saltinnehåll understeg referensvärdena. Energiinnehållet motsvarade behovet i ungefär fyra dagar för en vuxen person i åldern 31-60 år, med en genomsnittlig grad av fysisk aktivitet. I praktiken är det oftast flera i ett hushåll som delar på matkassen och många av prenumeranterna är barnfamiljer. Vi bedömer ändå att matkassen har potential att bidra till ett förbättrat näringsintag. En enkätundersökning visade att 74 procent av prenumeranterna upplevde att matkassen ger en ökad livskvalitet, och 51 procent att den bidrar till en bättre hälsa (19).
Övriga sociala fördelar
Slutligen så visade vår studie att de sociala värdena av matdonationer inte är begränsade till en förbättrad tillgång till mat eller näringsmässiga fördelar. Matkassarna gjorde att prenumeranterna även kunde spara pengar som kunde läggas på andra nödvändigheter som ytterligare matinköp, sjukvård, läkemedel, kläder, skor och andra konsumtionsvaror (20).
Även om denna ökade konsumtion till viss del minskar de miljömässiga fördelarna med matdonationer så är de sociala värdena obestridliga.
Författarna uppger inga jävsförhållanden.
Referenser
1. Svenska FN-förbundet. Frågor och svar om hunger. Hämtad 2022-02-03 från https://fn.se/skolmat/hunger-faq/
2. UNDP. The next frontier. Human development and the Anthropocene. Human Development Report 2020. New York: United Nations. Hämtad 2022-02-03 från https://hdr.undp.org/sites/default/files/hdr2020.pdf
3. Socialstyrelsen. Att förebygga och behandla undernäring. Kunskapsstöd i hälso- och sjukvård och socialtjänst, 2020. Hämtad 2022-02-03 från www.socialstyrelsen.se/globalassets/sharepoint-dokument/artikelkatalog/kunskapsstod/2020-4-6716.pdf
4. Borch A, et al. The prevalence and risk of food insecurity in the Nordic Region: Preliminary Results. Journal of Consumer Policy 2016; 39: 261–274.
5. O’Connor N, et al. What is food poverty? A conceptual framework. British Food Journal 2016; 118: 429-449.
6. Karlsson M. Matfattigdom i välfärdsstaten. Socialmedicinsk tidskrift 2019; 1: 106-115.
7. SCB. Att mäta fattigdom. Hämtad 2022-02-03 från www.scb.se/hitta-statistik/artiklar/2017/Att-mata-fattigdom/
8. Sundbeck J, et al. De delar ut mat från butikernas svinn: ”Matfattigdom kan drabba oss alla”. Dagens Nyheter 2021-11-08.
9. Mackenbach JD, et al. Socioeconomic and ethnic differences in the relation between dietary costs and dietary quality: the HELIUS study. Nutrition Journal 2019; 18: 21.
10. Mattisson I. Socioekonomiska skillnader i matvanor i Sverige. Rapport 9. Uppsala: Livsmedelsverket, 2016.
11. Fallaize R, et al. Dietary intake, nutritional status and mental wellbeing of homeless adults in Reading, UK. British Journal of Nutrition 2017; 118: 707-714.
12. Seale JV, et al. Nutrition and the homeless: the underestimated challenge. Nutrition Research Reviews 2016; 29: 143-151.
13. NHS Health Scotland. Food Poverty. Hämtad 22-03-22 från http://www.healthscotland.scot/media/2222/food-poverty.pdf
14. Mousa TY, et al. Impact of food pantry donations on diet of a low-income population. International Journal of Food Sciences and Nutrition 2019; 70: 78-87.
15. Mousa TY, et al. Food security of food recipients of a food pantry and soup kitchen. Public Health Nutrition 2019; 22: 1451-1460.
16. Simmet A, et al. The nutritional quality of food provided from pantries: A systematic review of existing literature. Journal of the Academy of Nutrition and Dietetics 2017; 117: 577-588.
17. Tse C, et al. Nutritional assessment of charitable meal programmes serving homeless people in Toronto. Public Health Nutrition 2008; 11: 1296-1305.
18. Nordiska ministerrådet. Nordic Nutrition Recommendations 2012. Integrating Nutrition and Physical Activity. Hämtad 2022-03-22 från https://norden.diva-portal.org/smash/get/diva2:704251/FULLTEXT01.pdf
19. Topor A, et al. Vardag, värdighet och det lilla extra i en utsatt situation. Om Stadsmissionens matkasseverksamhet. Hämtad 22-03-22 från https://uppsalastadsmission.se/wp-content/uploads/2021/09/Utvardering_Matkassen.pdf
20. Sundin N, et al. Surplus food donation: Effectiveness, carbon footprint, and rebound effect. Resources, Conservation and Recycling 2022; 181: 106271.
Nu finns möjlighet att lämna synpunkter på NNR-kapitlet om kolin
Fram till den 9 juni 2022 är kapitlet om kolin ute på remiss med möjlighet för forskare och andra intresserade att lämna synpunkter på kapitlet.
Alla kapitel i de nordiska näringsrekommendationerna 2022, NNR2022, kommer att vara tillgängliga för offentliga samråd. Både kapitel om näringsämnen och livsmedelsgrupper kommer att ingå i NNR2022-rapporten.
Även kapitlet om niacin finns det möjlighet att lämna synpunkter på fram till den 9 juni 2022. Tidigare under våren var kapitlet om riboflavin ute på offentligt samråd.
Nu finns möjlighet att lämna synpunkter på NNR-kapitlet om niacin
Fram till den 9 juni 2022 är kapitlet om niacin ute på remiss med möjlighet för forskare och andra intresserade att lämna synpunkter på kapitlet.
Alla kapitel i de nordiska näringsrekommendationerna 2022, NNR2022, kommer att vara tillgängliga för offentliga samråd. Både kapitel om näringsämnen och livsmedelsgrupper kommer att ingå i NNR2022-rapporten.
Även kapitlet om kolin finns det möjlighet att lämna synpunkter på fram till den 9 juni 2022. Tidigare under våren var kapitlet om riboflavin ute på offentligt samråd.
Munhälsa efter överviktskirurgi
Överviktskirurgi har blivit en allt vanligare metod för behandling av sjuklig fetma, obesitas. Trots många fördelar för patienten finns det en risk för komplikationer som påverkar både den generella hälsan och munhälsan. Generella komplikationer som kan uppstå efter kirurgi har varit föremål för mycket forskning de senaste åren, medan det endast finns ett begränsat antal studier som undersöker hur munhälsan påverkas. Det knappa vetenskapliga underlaget gör det svårt att dra definitiva slutsatser men vissa studier tyder på att det kan finnas risk för både tandlossning och karies. Vaksamhet hos både vårdgivare och individer som funderar på eller har genomgått kirurgi är viktigt för att minimera risken för oral sjukdom.
>>text: Negin Taghat, leg tandläkare, doktorand, Avdelningen för odontologisk psykologi och folkhälsa, Institutionen för odontologi, Sahlgrenska Akademin, Göteborgs universitet
Denna artikels huvudfokus är den orala hälsan, det vill säga munhälsan, efter överviktskirurgi; en introduktion till ämnet tillhandahålls i syfte att ge läsaren en överblick över området.
Obesitas
Obesitas, eller fetma, definierat som ett Body Mass Index, BMI, över 30 kg/m2 har under de senaste årtiondena stadigt ökat i världen. Idag klassificeras 13 procent av den vuxna befolkningen i världen som obesa (1). I Sverige är motsvarande andel 16 procent enligt en nationell enkät (2). Obesitas har identifierats som en riskfaktor för att utveckla hjärt-kärlsjukdomar, typ 2-diabetes och flera cancerformer (3, 4). Studier som undersökt hur obesitas påverkar den orala hälsan har funnit associationer till tandlossningssjukdomar och tandförluster (5, 6).
Behandlingar för obesitas
Det finns olika behandlingsmetoder vid obesitas, till exempel kost, fysisk aktivitet, läkemedel och kirurgi (7). Obesitaskirurgi anses vara en effektiv behandlingsmetod mot sjuklig obesitas – BMI över 40 – och leder förutom till viktminskning också till minskad sjuklighet och förtida död (7, 8). I Sverige är de vanligaste operationsmetoderna ”gastric bypass” och ”sleeve gastrectomy”. Vid gastric bypass omvandlas övre delen av magsäcken till en liten ficka medan större delen av magsäcken och tunntarmen kopplas bort. Den lilla kvarvarande delen av magsäcken kopplas direkt till tunntarmens nedre del. Vid sleeve gastrectomy avlägsnas ungefär 3/4 av magsäcken och kvarvarande del ombildas till ett rör (9). Båda operationerna utförs vanligen genom titthålskirurgi (10). För att berättigas till obesitaskirurgi inom ramen för hälso- och sjukvårdsförsäkringen i Sverige finns rekommendationer från regionerna att BMI ska antingen vara över 40, alternativt ett BMI över 35 med samsjuklighet, exempelvis diabetes eller hjärt-kärlsjukdomar. År 2020 genomfördes omkring 3400 överviktsoperationer i Sverige, varav 30 procent finansierades av patienten själv. Sleeve gastrectomy var en något vanligare operationsmetod än gastric bypass (10).
Generella komplikationer efter obesitaskirurgi
Obesitaskirurgi kan leda till en rad komplikationer. Kortsiktiga komplikationer är oftast orsakade av själva det operativa ingreppet, exempelvis blödning och sårbildning (9). Långsiktiga komplikationer beror på omstrukturering av magtarm-kanalen och kan medföra exempelvis svårigheter med matintag, anemi, malnutrition, och minskad bentäthet (9, 11).
Malnutrition till följd av överviktskirurgi kan resultera i brist på vitaminer och mineraler som A, tiamin, B6, B12, D, E, folsyra, kalcium, järn, koppar och zink (12). Patienter som genomgått kirurgisk behandling får därför rådet att utöver allsidig kost, även äta tillskott för att minska risken för näringsbrist. För sjukvården är rekommendationen att regelbundet följa upp nutritionsstatus hos dem som opererats (13).
Orala komplikationer efter obesitaskirurgi
Studier har visat att kosten kan vara en bidragande orsak till utvecklingen av orala sjukdomar, och att näringsbrist eventuellt kan öka risken för uppkomsten av både tandlossning och karies (14). Den omstrukturering av magtarm-kanalen som obesitaskirurgi medför, i kombination med förändringar i ätmönster och måltidsfrekvens, kan teoretiskt sett kunna påverka den orala hälsan efter operationen.
Hur obesitaskirurgi påverkar den orala hälsan är däremot otillräckligt studerat. Forskningen inom området är begränsad och resultaten är i många fall motsägelsefulla. Vissa studier tyder på att det finns ökad förekomst av karies (15, 16). I en studie observerades höga nivåer av kariesframkallande bakterier i munhålan, som ökar risken för att initiala kariesangrepp – ”små hål” – förvärras och ökar risken för att utveckla nya kariesangrepp (16). Det har även observerats associationer till tandlossningssjukdomar och tandisningar (17-20). Samtidigt har andra studier inte visat några sådana samband (21-23).
Gemensamt för studierna är dock att de har korta uppföljningstider. Det saknas helt studier om hur den orala hälsan påverkas över längre tid av olika operationsmetoder.
Positiva förändringar efter obesitaskirurgi har också påvisats, främst i form av ökad salivsekretion, troligen till följd av minskad medicinering (21). Det finns flera läkemedel som kan orsaka biverkningar i form av minskad salivsekretion. Tidigare forskning visar att ökad salivmängd minskar risken för karies. En fallserie visade dock att ”vilosaliven”, det vill säga saliven som smörjer och renar munnen mellan måltider var låg hos många opererade individer. Nedsatt salivflöde kan bidra till ökad kariesrisk (16, 24).
Egen upplevelse av oral hälsa
Vårdpersonal som möter obesitasopererade patienter uppger att dessa ofta uttrycker att de fått försämrad oral hälsa. Flera studier har visat samma resultat och även påverkan på den orala hälsorelaterade livskvaliteten (16, 25, 26). I en studie uppgav nästan hälften av deltagarna att deras orala hälsa var dålig. Kvinnor uppgav mer besvär med tandisningar än män, medan män rapporterade färre kvarvarande tänder (26). Män gick dessutom mer sällan till tandläkaren än kvinnor.
Kliniska implikationer
Trots det begränsade vetenskapliga underlaget är slutsatsen idag att det finns en risk för påverkan på den orala hälsan efter obesitaskirurgi. Det är därför viktigt att göra vårdgivare och individer medvetna om dessa möjliga komplikationer. En god dialog mellan tandläkare och patienter som ska eller har genomgått obesitaskirurgi är viktig. Detta skapar rätt förutsättningar för att tandvården ska kunna erbjuda goda förebyggande och hälsofrämjande insatser.
Pågående forskning
Det pågår mycket forskning i Sverige och internationellt om obesitaskirurgi och dess komplikationer (27-29). Forskning kring hur den orala hälsan påverkas är inte lika vanligt förekommande. Ett projekt som inkluderar denna aspekt är BAriatric Surgery SUbstitutional and Nutritional Study (BASUN) (www.basunstudien.se) (28). Det är ett samverkansprojekt mellan forskare inom flera medicinska specialiteter vid Sahlgrenska Akademin, Göteborgs universitet, med syfte att jämföra och studera långsiktiga utfall av kirurgisk och medicinsk obesitasbehandling. Information om oral hälsa och tandstatus samlas in på en subgrupp inom den befintliga studiepopulationen i BASUN och relateras till medicinska och nutritionella data. Uppföljningar planeras under en 10-årsperiod. För närvarande pågår analys av tvåårsdata och parallellt sker datainsamling vid 5-årsuppföljning (26).
Författaren uppger inga jävsförhållanden.
Referenser
1. World Health Organization. Obesity and overweight. Senast uppdaterad 2020. http://www.who.int/mediacentre/factsheets/fs311/en/ [Hämtad 2022-01-21].
2. Folkhälsomyndigheten. Övervikt och fetma. Senast uppdaterad 2021-05-07. https://www.folkhalsomyndigheten.se/livsvillkor-levnadsvanor/fysisk-aktivitet-och-matvanor/overvikt-och-fetma/ [Hämtad 2022-01-21].
3. G. B. D. Obesity Collaborators. Health effects of overweight and obesity in 195 countries over 25 years. N Engl J Med. 2017; 377:13-27.
4. Guh DP et al. The incidence of co-morbidities related to obesity and overweight: a systematic review and meta-analysis. BMC Public Health. 2009; 9:88.
5. Keller AJ et al. Association between periodontal disease and overweight and obesity: a systematic review. J Periodontol. 2015; 86:766-76.
6. Östberg AL et al. Tooth loss and obesity in a defined Swedish population. Scand J Public Health. 2009; 37:427-33.
7. Bray GA et al. Management of obesity. Lancet. 2016; 387:1947–56.
8. O’Brien PE et al. Long-term outcomes after bariatric surgery: a systematic review and meta-analysis of weight loss at 10 or more years for all bariatric procedures and a single centre review of 20-year outcomes after adjustable gastric banding. Obes Surg. 2019; 29: 3–14.
9. Colquitt JL et al. Surgery for weight loss in adults. Cochrane Database Syst Rev. 2014; 8:Cd003641.
10. Årsrapport SOReg 2020. Publicerad maj 2021. https://www.ucr.uu.se/soreg/component/edocman/arsrapport-soreg-2020-del-1/viewdocument/1700?Itemid=.
11. Fujioka K. 2005. Follow-up of nutritional and metabolic problems after bariatric surgery. Diabetes Care. 2005; 28:481–84.
12. Via MA et al. Nutritional and micronutrient care of bariatric surgery patients: current evidence update. Curr Obes Rep. 2017; 6:286–96.
13. Laurenius A et al. Nordiska riktlinjer för kosttillskott och uppföljning efter obesitaskirurgi – Monitorering och supplementering med vitaminer och mineraler. Läkartidningen. 2018 Jan 9; 115:ETD7.
14. Chapple IL et al. Interaction of lifestyle, behaviour or systemic diseases with dental caries and periodontal diseases: consensus report of group 2 of the joint EFP/ORCA workshop on the boundaries between caries and periodontal diseases. J Clin Periodontol. 2017; 44 Suppl 18:S39-S51.
15. Marsicano JA et al. Interfaces between bariatric surgery and oral health: a longitudinal survey. Acta Cir Bras. 2011; 26 (Suppl2):79-83.
16. Taghat N et al. Oral health profile of postbariatric surgery individuals: A case series. Clin Exp Dent Res. 2021; 7(5):811-18.
17. de Moura-Grec PG et al. Impact of bariatric surgery on oral health conditions: 6-months cohort study. Int Dent J. 2014; 64:144-49.
18. Sales-Peres SH et al. Periodontal status and pathogenic bacteria after gastric bypass: a cohort study. J Clin Periodontol. 2015; 42:530-36.
19. Marsicano JA et al. Evaluation of oral health status and salivary flow rate in obese patients after bariatric surgery. Eur J Dent. 2012; 6:191–97.
20. Netto BD et al. Influence of Roux-En-Y gastric bypass surgery on vitamin C, myeloperoxidase, and oral clinical manifestations: a 2-year follow-up study. Nutr Clin Pract. 2012; 27:114-21.
21. Cardozo DD et al. Impact of bariatric surgery on the oral health of patients with morbid obesity. Obes Surg. 2014; 24:1812-16.
22. Knas M et al. Impact of morbid obesity and bariatric surgery on antioxidant/oxidant balance of the unstimulated and stimulated human saliva. J Oral Pathol Med. 2016; 45:455-64.
23. Jaiswal GR et al. Impact of bariatric surgery and diet modification on periodontal status: a six-month cohort study. J Clin Diagn Res. 2015; 9:43-45.
24. Leone CW et al. Physical and chemical aspects of saliva as indicators of risk for dental caries in humans. J Dent Educ. 2001; 65(10):1054-62.
25. Berg A. Untold stories of living with a bariatric body: long-term experiences of weight-loss surgery. Sociol Health Illn. 2020; 42(2):217-231.
26. Taghat N et al. Oral health-related quality of life after gastric bypass surgery. Obes Surg. 2020; 30(1):224–32.
27. National Institute of Diabetes and Digestive and Kidney diseases. Clinical trials for weight-loss surgery. Senast uppdaterad september 2020. https://www.niddk.nih.gov/health-information/weight-management/bariatric-surgery/clinical-trials. [Hämtad 2022-03-29].
28. SOReg. Ny kunskap som baseras på data från SOReg – Leder forskningen till bättre resultat? Publicerad oktober 2021. https://www.ucr.uu.se/soreg/component/edocman/ny-kunskap-som-baseras-pa-data-fran-soreg-leder-forskningen-till-battre-resultat-2/viewdocument/1824?Itemid=
29. Höskuldsdottir G et al. Design and baseline data in the Bariatic Surgery Substitution and Nutrition Study (BASUN): a 10-year prospective cohort study. BMC Endocr Disord. 2020; 20:23.
Viljan att förstå – avgörande för att möta människor med icke vedertagna diagnoser
Det första människor gör när de mår dåligt är sällan att gå till doktorn, psykologen, eller någon annan professionell person. I stället försöker de flesta tolka sitt hälsotillstånd med hjälp av sina egna teorier, släkt och vänner och den omgivande kulturen. När personer gör egna hypoteser om vad symtomen kan handla om, är det vanligt att ta till varianter av icke vedertagna diagnoser. Det kan vara viktiga steg på vägen till att få professionell, evidensbaserad vård. Men det finns också en risk att icke vedertagna diagnoser håller personer borta från den vård de kan behöva.
>>text: Gustaf Waxegård, specialist i klinisk psykologi och PhD i psykologi, affilierad forskare vid psykologiska institutionen, Linnéuniversitetet, Växjö, och arbetar på barn- och ungdomskliniken i Region Kronoberg
Först: vad som utgör en ”diagnos” är ingen enkel fråga. Svenska akademins ordlista definierar ordet som: fastställande av sjukdoms art.1 Socialstyrelsen slår fast att ”all hälso- och sjukvårdspersonal som har tillräcklig kunskap om en sjukdom, en funktionsnedsättning eller en skada kan ställa diagnos inom ramen för sin yrkeskompetens.” Det är också en skillnad mellan processen att ställa en diagnos, och processen att koda eller klassificera den i formella system som ICD 10/11 eller DSM 5 som används i vården. Det gör att den lockande enkla utvägen att likställa ”vedertagen” med ”finns i ett klassificeringssystem” inte håller.2
Vad som kan anses vara icke vedertagna diagnoser är också långt ifrån självklart. Det går att tänka sig minst fem olika kategorier:
1. En diagnos som har spridning i samhället och som över lag anses pseudovetenskaplig av professionella och forskare. Möjliga exempel kan vara sockerberoende (1) även om sockerberoende inte avfärdas av alla forskare (2), olika typer av överkänsligheter för stimuli i miljön som saknar vetenskapligt stöd (3) som elallergi, eller vaccinationsutlöst autism (4, 5).
2. En pseudovetenskaplig diagnos som även används av professionella och forskare. Ett exempel kan vara diagnosen homosexualitet, som ströks ur den psykiatriska diagnosmanualen DSM år 1974 (6).
3. En diagnos som har vetenskaplig grund men som inte längre används officiellt, som Aspergers syndrom: syndromet ingår nu i diagnosen autism (7).
4. En diagnos som är på väg att bli vetenskapligt legitim men där forskningsbasen är under uppbyggnad och som därför ännu inte har ”slagit igenom”. Ett tänkbart exempel här är PANS/PANDAS (8), som innebär en akut och dramatisk debut av samtidigt tvångssyndrom och neuropsykiatriska symtom. En orsakshypotes har varit att debuten delvis förklaras av streptokockinfektion. PANS är accepterat av många forskare men det finns också betydande kunskapsluckor.
5. Väl validerade begrepp som används i professionella sammanhang men som inte är egentliga diagnoser. Exempel återfinns bland annat inom ramen för psykoterapi, såsom inlärd hjälplöshet (9) vid depression.
Fortsättningsvis kommer den här texten att rikta in sig på kategori 1: Icke vedertagna diagnoser som har spridning i samhället och som över lag anses pseudovetenskapliga av professionella och forskare.
En dimensionell modell som pedagogiskt stöd
I bästa fall kan sådana icke vedertagna diagnoser bana väg för en ny förklaringsmodell som accepteras både av den professionella och av personen som har problemet. Ett värre scenario är när icke vedertagna diagnoser förekommer i sammanhang som präglas av faktaresistens och/eller konspirationsteorier.
När en professionell person stöter på idéer som inte stämmer med vedertagen kunskap kan hen, själv eller tillsammans med andra, försöka placera in utsagan längs en tänkt dimension. I den ena änden av dimensionen – som är en pedagogisk hjälp och inte gör anspråk på att vara en vetenskaplig modell – återfinns avsiktligt manipulativ desinformation från särintressen. Det kan vara ”systemkonkurrerande” icke-demokratiska stater, religiösa extremister, politiska extremister och kriminella. Ibland också en kombination av dessa.
I andra änden av vår tänkta dimension går det att placera in personer som, oavsett omständigheter i övrigt, redan har en tolkning av sina symtom som är näraliggande en vedertagen förståelse, och aktivt söker professionell bedömning för att bekräfta eller korrigera sin egen tolkning av symtomen. Icke vedertagna diagnoser kan då bidra till normalisering och göra det möjligt att sätta ord på något som tidigare varit svårt att förmedla till andra.
När begreppet ”introvert” trendade i media, bland annat definierat av att ha ett rikt inre liv och att lätt bli uttröttad av sociala situationer, var det många som ”kom ut” som introverta på grund av igenkänningsfaktorn. Introvert fick i media en klart diagnosliknande kvalitet som dessutom ofta förmodades definiera en persons hela psykiska värld. I själva verket är introversion motpolen till personlighetsdraget ”extraversion” i den vetenskapligt välförankrade femfaktor-modellen, och förekommer alltså som ett personlighetsdrag bland (minst) fyra andra som är lika viktiga. När (kombinationer av) personlighetsdrag blir extrema och får dysfunktionella konsekvenser, pratar vi om personlighetsstörningar.
Vilken funktion fyller en icke vedertagen diagnos?
Beroende på vilken funktion en icke vedertagen diagnos bedöms fylla, kan olika professionella strategier fungera olika väl för att hjälpa patienter att få bästa möjliga vård.
Avsiktlig desinformation
Den ena extrema änden av dimensionen – avsiktlig desinformation – innebär att patienter påverkas av sådant som att någon utomstående tagit över en etablerad hemsida, statligt regisserad vaccinpropaganda, läckage och manipulation av sekretesskyddade uppgifter, automatiska dataprogram, så kallade botar, som gör att desinformation trendar, med mera.
Forskarna Neylan, Patel och Erickson (10) ger 10 konkreta råd till professionella verksamheter:
1. Var försiktig med vad du lägger ut på internet – allt kan ändras, manipuleras, eller missbrukas.
2. Informera sociala medie-plattformar när du ser felaktig information i deras tjänster.
3. Var beredd att bemöta och konfrontera andra professionella som sprider konspirationsteorier.
4. Titta noga på URL-adresser för att undersöka deras legitimitet.
5. Jämför information från flera källor för att bättre kunna urskilja om den är riktig.
6. Ha uppdaterad hård- och mjukvara. Äldre datorer och program hackas lättare.
7. Kontakta snabbt myndigheter och lokala IT-tekniker när ett online-angrepp sker.
8. Säkerhetskopiera dokument så att det alltid finns ett pålitligt original när känslig information läcker ut, sprids och förvanskas på nätet.
9. Utbilda vårdpersonal om risker och hot från virus, sabotageprogram (malware), försök att lura till sig lösenord och bankuppgifter (phishing), och hackare.
10. Kom ihåg att konspirationsteorier ofta bekämpas bättre med empati och medkänsla än med fakta och debatt.
Konspirationsteorier och faktaresistens
Till höger om ren desinformation från särintressen, kan vi på vår dimensionella modell placera in icke vedertagna diagnoser som hänger samman med problematisk faktaresistens och konspirationsteorier. Detta kan också kallas missinformation (11). Här återfinns ”diagnoser” som vaccinationsorsakad autism, eller andningsbesvär som en effekt av ”chemtrails”. Personer som anser att en del kondensationsstrimmor efter flygplan är medvetna utsläpp av farliga ämnen avsedda för att påverka oss kallar strimmorna för chemtrails. Det finns inga vetenskapliga belägg att chemtrails finns.
Faktaresistens och konspirationsteorier är vitt spridda i olika tider, kulturer och sammanhang. De har konsekvenser i form av konkret påverkan på människors hälsa. Vidare är de emotionella på så vis att de snarare orsakas av negativa känslor än av rationella överväganden. De är även sociala, genom att hänga tätt ihop med psykologisk motivation som har att göra med någon typ av mellangruppskonflikt. Det kan handla om elit kontra folk, land mot stad, eller arier mot judarIndivider kan dras in i faktaresistens via samverkande faktorer som en förhöjd benägenhet att känna ångest, ideologisk övertygelse, att vara påverkad av särintressen, stark lojalitet till sin sociala identitet – och en vilja att hävda sin personliga identitet (13).
Personer som fastnat i faktaresistent tänkande har precis som alla andra ett behov av upplevd kontroll och trygghet, tillhörighet och av att förstå livet (14). Problemet är att de ”köper” sig dessa värden med hjälp av verklighetsfrånvända idéer, vilket riskerar att göra dem ännu mera isolerade på sikt. Problemen tilltar väsentligt i miljöer där verklighetsförnekelse i vissa avseenden är norm, och där det snarare är förknippat med utanförskap att inte anamma konspirationsteoretiskt tänkande.
Konspirationsteoretiskt tänkande är ofta monologiskt, vilket betyder att det finns en övergripande tendens att se tillvaron som styrd av konspirationer. Det kan leda till något paradoxala resultat: ju mer deltagare i en forskningsstudie höll för troligt att prinsessan Diana fejkade sin egen död, desto mer sannolikt ansåg samma deltagare det var att hon blev mördad. Konspirationsteorier behöver alltså inte vara logiskt kompatibla för att kunna samexistera och få spridning (15).
Ett konstruktivt professionellt synsätt i relation till faktaresistens kan vara att människor i normalfallet inte avstår frivilligt från möjlighet till god medicinsk hjälp. Faktaresistens kan då liknas vid ett livsstilsproblem i stil med rökning: en potentiellt hälsoskadlig (14) vana som individer kan vara olika motiverade att göra sig av med. Det är en rättighetsfråga att få ta del av vetenskapligt vederhäftig kunskap, och effekterna av den, även om man haft oturen att hamna i ett förnekande av den.
Det bör inte ses som en nedlåtande inställning att aktivt hjälpa människor till en förståelse som bättre gynnar deras egen och/eller anhörigas hälsa. Däremot är det centralt att inte bete sig nedlåtande i ansträngningarna att lyckas med detta mål. Effektiva sätt att bistå patienter i deras vandring mot mer vedertagen förståelse – och sammanhängande effektiv vård – kan vara:
- Du och patienten ska göra ett jobb tillsammans. Lyssna och argumentera nyfiket, för att lära, inte för att vinna. En öppenhet för att det finns fler viktiga sanningar än en enda kan mjuka upp oflexibla förhållningssätt (16).
- Skapa ett möte där patienten känner att du bidrar till lugn, trygghet och värdighet.
- Låt ditt lyssnande präglas av nyfikenhet, intresse, iver och glädje. Det öppnar upp för gemensamt utforskande. Känslor som ilska, irritation, rädsla och stress leder till ett smalt, mentalt fokus inriktat på hot hos både behandlare och patient (17, 18).
- Utbilda dig i motiverande samtalsmetod (MI) (19, 20).
- Fokusera gärna på fakta, siffror, forskning – på en nivå som den du möter kan förstå. Individer som förstår att stödet för en åsikt de har går att mäta blir ofta mindre benägna att inta extrema ståndpunkter. När siffror och fakta utelämnas från en diskussion blir åsikter gärna mer extrema (21).
- Ha i åtanke att det inte alltid är problemet/diagnosen som inte kan accepteras av patienten, utan snarare lösningen på problemet (22). En patient kan ha svårt att överge en felaktig självdiagnos på grund av konsekvenserna som det för med sig. Det kan handla om ett behov av att förstå sig själv på ett nytt sätt, eller att behöva genomgå svåra behandlingar.
- Utmana inte patientens grundläggande identitet eller självbild i onödan (13). Fokusera på det patienten söker vård för.
- Upprätthåll en god kultur baserad på fakta på din arbetsplats och i ditt team. Skaffa vid behov handledning som bidrar till reflektion.
- Bibehåll ditt professionella omdöme och agera på det sätt du behöver. Om faktaresistens hos en förälder exempelvis leder till oro för att ett barn far illa ska anmälan till socialtjänsten göras.
Olika benämningar av distress
Ytterligare en bit åt höger på vår tänkta dimension finns personer som av andra skäl tagit till sig icke vedertagna diagnoser för att sätta ord på sina egna eller andras symtom eller stressande upplevelser (eng. distress).
Ett sådant skäl att föredra vissa diagnoser framför andra kan vara social önskvärdhet. Att vara en psykologiskt ”högkänslig person” kan ses som mer ok, intressant och begripligt än att ha en personlighet som präglas av en kombination av de mer vedertagna personlighetsdragen hög neuroticism, hög introversion och hög öppenhet för upplevelser (23). En överkänslighet av något slag – el, olika födoämnen, ansträngning, stress med mera – kan av olika anledningar kännas mer ok än att ha vedertagna diagnoser som depression, IBS, hälsoångest, eller autism.
Ett annan förklaring till varför patienter på svaga grunder ibland hävdar överkänslighet för olika typer av stimuli kan vara att en person har utvecklat en nocebo-respons, alltså förväntansstyrt illabefinnande (24). Nocebo är motsatsen till placebo-effekten, där positiva förväntningar skapar välbefinnande. Det har gjorts ett antal studier där självupplevt överkänsliga personer i dubbelblinda provokationstester inte kan skilja upplevt farliga från harmlösa stimuli. Medan överkänslighet för olika födoämnen är överrapporterat – men självklart förekommer och ofta är legitima diagnoser – kan andra typer av upplevd överkänslighet vara svåra att påvisa överhuvudtaget (25-28). Naturligtvis finns upplevelsen av illabefinnande hos personen, men den är svår att trovärdigt koppla till den upplevda orsaken.
Sättet som människor får medicinsk information på kan ge negativa förväntningar på egna symtom (29). Därför är maximering av placebo-responser och minimering av nocebo-responser bland de viktigaste utmaningarna för vissa typer av medicinska problem. Placebo och nocebo-responser kan påverka både immunsystem (30, 31) och hormoner (32).
Kulturell mismatch
Ytterligare en omständighet som kan förklara medicinska missuppfattningar och misstro är kulturell mismatch. Här kan en grupp människor tidigare i historien ha utsatts för en förnedrande behandling, som påtvingade medicinska experiment, vilket lett till kvarstående misstänksamhet hos den utsatta gruppen. Trots att det oetiska beteendet upphört finns skepsis kvar, vilket orsakar dubbel skada hos den ursprungligen utsatta gruppen.
Det finns många exempel (33-35), men ett av de mest ökända är Tuskegee-studien, som ville studera naturalförloppet av syfilis hos svarta personer i USA (36-40). Svarta personer som ingick i studien fick ingen vård, inte ens efter det att verksamma mediciner hade tagits fram. Tuskegee-studien har bidragit till en kvarstående skepsis hos många svarta i USA till att delta i biomedicinsk forskning.
Fenomenet kulturell mismatch kan vara upplysande men också tolkas fel. Framför allt är det lätt att glömma att a) bristande tillit mellan grupper i samhället kan ha existerat tidigare och b) de kan vara en skönmålning av det nuvarande samhället att hävda att de socialt ojämlika strukturer som ledde till att en grupp utsattes har upphört, även om vissa saker förändrats till det bättre. Oavsett orsaker kvarstår ett faktum: social ojämlikhet föder bristande tillit mellan samhällsgrupper.
Kulturbundna idiom
Det finns också en växande forskningstradition kring ”idioms of distress” (41), att lokal kulturell tillhörighet påverkar hur människor formulerar sig kring sina symtom. Ett exempel på ett idiomatiskt uttryck som används i många delar av världen i samband med problem som generaliserad oro, ältande (ruminering), depression och trauma är ”thinking too much”, att ”tänka för mycket” (42). Ett mer specifikt exempel är uttrycket ”ataque de nervios”, ungefär nervsammanbrott, efter trauma, som används i flera spansktalande kulturer (43). Somatisering, att uttrycka psykisk ohälsa med kroppsliga symtom, är ett annat typiskt exempel. Somatisering i olika former är vanligt i de flesta kulturer (44, 45).
Idioms of distress är både mindre precisa och mer mångfacetterade än vedertagna diagnoser. De ska inte reduceras till, eller ses som synonyma med dessa. Däremot kan det vara bra att inkludera dem i screening och bedömning, då de fungerar väl som indikatorer på problematik. De kan också användas för att begripliggöra, förtydliga och normalisera behandlingsmetoder för patienter. För att minska stigma, nå ut bättre och få fler att söka vård är det rätt att ta hänsyn till kulturbundna sätt att uttrycka symtom på. Om man i det enskilda fallet har en god förståelse för vad ett visst uttryck står för, kan det också i samråd med patienten sättas upp som ett behandlingsmål att påverka. När kulturella faktorer behöver vägas in för att ge bra vård, kan det vara värt att använda en så kallad kulturformuleringsintervju (46, 47), som den i klassificeringen DSM 5. Intervjun ger en vägledning till att bättre förstå patientens syn på sina egna besvär, skapar förståelse för patientens identitet och sjukdomssyn i allmänhet, och för vilket stöd och vilka åtgärder patienten önskar och/eller förväntar sig. Svenska versioner kan laddas ned utan kostnad från Pilgrim Press förlag.3
Harmlös informationspåverkan
En patient kan också vara påverkad av icke vedertagen information utan att ha en stark psykologisk motivation att hålla fast i den. Det finns idag tusentals appar med medicinsk inriktning, varav ett antal riktar in sig på att bidra till ”själv-diagnos”. Även om kvalitetssäkrad professionell information på betrodda hemsidor kan vara av stort värde (48) behöver hälso-appar och deras affärsmodeller utvärderas med ett kritiskt öga (49).
Längst till höger på vår tänkta dimension går det som sagt att placera in personer som redan har en tolkning av sina symtom som är näraliggande en vedertagen förståelse. De söker aktivt en professionell bedömning för att bekräfta – eller korrigera – sin egen tolkning symtomen. I det här fallet handlar det om att vården är tillgänglig, och om att utveckla fungerande former av egenvård. Forum som ger överblickbar och professionellt kvalitetssäkrad information, som 1177.se, är viktiga.
Bör påståenden om den egna hälsan påverka vilken vård en person får?
Bör det på något vis, och av några skäl, få konsekvenser för personers vård att de väljer att sätta tilltro till ovetenskapliga begrepp, eller beter sig på ett sätt som kan försämra den egna hälsan? En sådan inställning kan kallas för hälso-responsibilism. I en nyligen godkänd doktorsavhandling i medicinsk etik (50) argumenterar specialistläkaren Joar Björk emot en sådan ståndpunkt. Argumenten för hälso-responsibilism har flera svaga punkter och håller enligt honom inte för närmare medicinsk-etisk granskning. Ett övergripande motargument är att synsättet att människor som gjort dåliga val bör lämnas åt sitt öde helt enkelt är så strängt att det inte uppfyller kraven för en rimlig teori om rättvisa. Andra svårigheter med hälso-responsibilism är att begreppen fri vilja och fritt val måste kunna definieras och tillämpas både teoretiskt och praktiskt: När gjorde till exempel en individ valet som ledde till att hen fastnade i en beroendeproblematik, och var det valet fritt? När skedde valet för en gängmedlem att glida in i en kriminell livsstil som ledde till akutkrävande vård efter en skottskada? Fanns det ett fritt val någon gång tidigare i livet, och efter det att individen fastnat i beroende och/eller kriminella strukturer ska valen inte anses fria och därför inte heller påverka vården? Om inte den här typen av frågor går att reda ut – och mycket lite, baserat på vad vi vet om exempelvis utvecklingspsykologi och kognitiv psykologi tyder på att det går – faller en stor del av meningsfullheten med ett hälso-responsibilistiskt förhållningssätt.
Ett relaterat psykologiskt synsätt är att beteenden som inte är hälsofrämjande ofta väljs i relation till en helt annan funktion än hälsa. Det kan vara social gångbarhet, kulturella referensramar, eller individuell sårbarhet för snabba belöningar – rökning för att bli accepterad i ett ungdomsgäng, spänning vid bergsklättring, att gå till puben efter jobbet, aktivt belöningscentrum i hjärnan för energirik mat och/eller alkohol, ökad vakenhetsgrad hos hjärnan vid ADHD i samband med ”störande” beteende, och så vidare. Dessa beteenden kan vara kopplade till negativa långsiktiga hälsokonsekvenser, men det blir klåfingrigt av vården att ta sig rätten att kräva att olika livsval hos individen alltid ska göras med hälso- och sjukvårdsapparatens prioriteringar i åtanke. Att ge förebyggande beteendestöd och information som underlättar hälsofrämjande livsval är naturligtvis en helt annan, och mindre problematisk, approach.
Det finns inte heller ett uttryckt stöd för hälso-responsibilism i hälso- och sjukvårdslagens4 prioriteringsgrundande huvudprinciper (människovärdesprincipen, behovs- och solidaritetsprincipen, och kostnadseffektivitetsprincipen).
Slutsats: anpassa och öka mängden strategier för att ge fortsatt god, personcentrerad vård
Sammanfattningsvis: om icke vedertagna diagnoser ur professionell synvinkel inledningsvis kan ses som något icke-önskvärt och rent av irriterande, så leder fördjupad reflektion till ett mer nyanserat synsätt. Språkbruk och förklaringsmodeller kan ha sin upprinnelse i allt från aktiv desinformation till ett ärligt sökande efter den mest välförankrade kunskapen. Oavsett vilket, så är den professionelles uppgift att hjälpa människor att få tillgång till en så god vård som möjligt, från systemnivå till individnivå. Metoderna för att lyckas med detta behöver emellertid variera, baserat på vilken funktion den icke vedertagna diagnosen fyller i det enskilda fallet.
1 https://svenska.se/tre/?sok=diagnos&pz=1
3 https://www.pilgrimpress.se/produkt/dsm-5-i-kulturformuleringsintervju-kfi/
Referenser
1. Westwater ML, Fletcher PC, Ziauddeen H. Sugar addiction: the state of the science. European Journal of Nutrition. 2016;55:55-69.
2. DiNicolantonio JJ, O’Keefe JH, Wilson WL. Sugar addiction: Is it real? A narrative review. British Journal of Sports Medicine. 2018;52(14):910-3.
3. Van den Bergh O, Brown RJ, Petersen S, Witthöft M. Idiopathic Environmental Intolerance: A Comprehensive Model. Clinical Psychological Science. 2017;5(3):551-67.
4. DeStefano F, Shimabukuro TT. The MMR Vaccine and Autism. Annual Review of Virology. 2019;6:585-600.
5. Hviid A, Hansen JV, Frisch M, Melbye M. Measles, mumps, rubella vaccination and autism a nationwide cohort study. Annals of Internal Medicine. 2019;170(8):513-20.
6. De Block A, Adriaens PR. Pathologizing sexual deviance: A history. Journal of Sex Research. 2013;50(3-4):276-98.
7. Rosen NE, Lord C, Volkmar FR. The Diagnosis of Autism: From Kanner to DSM-III to DSM-5 and Beyond. Journal of Autism and Developmental Disorders. 2021;51(12):4253-70.
8. Chiarello F, Spitoni S, Hollander E, Matucci Cerinic M, Pallanti S. An expert opinion on PANDAS/PANS: highlights and controversies. International Journal of Psychiatry in Clinical Practice. 2017;21(2):91-8.
9. Vollmayr B, Gass P. Learned helplessness: Unique features and translational value of a cognitive depression model. Cell and Tissue Research. 2013;354(1):171-8.
10. Neylan JH, Patel SS, Erickson TB. Strategies to counter disinformation for healthcare practitioners and policymakers. World Medical and Health Policy. 2021.
11. Swire-Thompson B, Lazer D. Public health and online misinformation: Challenges and recommendations. Annual Review of Public Health 2019. p. 433-51.
12. van Prooijen JW, Douglas KM. Belief in conspiracy theories: Basic principles of an emerging research domain. European Journal of Social Psychology. 2018;48(7):897-908.
13. Hornsey MJ. Why Facts Are Not Enough: Understanding and Managing the Motivated Rejection of Science. Current Directions in Psychological Science. 2020;29(6):583-91.
14. Douglas KM, Sutton RM. Why conspiracy theories matter: A social psychological analysis. European Review of Social Psychology. 2018;29(1):256-98.
15. Wood MJ, Douglas KM, Sutton RM. Dead and alive: Beliefs in contradictory conspiracy theories. Social Psychological and Personality Science. 2012;3(6):767-73.
16. Fisher M, Knobe J, Strickland B, Keil FC. The Influence of Social Interaction on Intuitions of Objectivity and Subjectivity. Cognitive Science. 2017;41(4):1119-34.
17. Isgett SF, Fredrickson BL. Broaden-and-Build Theory of Positive Emotions. International Encyclopedia of the Social & Behavioral Sciences: Second Edition 2015. p. 864-9.
18. Fredrickson BL. The role of positive emotions in positive psychology: The broaden-and-build theory of positive emotions. American Psychologist. 2001;56(3):218-26.
19. Rollnick S, Butler CC, Kinnersley P, Gregory J, Mash B. Motivational interviewing. BMJ (Online). 2010;340(7758):1242-4.
20. Miller WR, Rollnick S. Ten things that motivational interviewing is not. Behavioural and Cognitive Psychotherapy. 2009;37(2):129-40.
21. Friesen JP, Campbell TH, Kay AC. The psychological advantage of unfalsifiability: The appeal of untestable religious and political ideologies. Journal of Personality and Social Psychology. 2015;108(3):515-29.
22. Campbell TH, Kay AC. Solution aversion: On the relation between ideology and motivated disbelief. Journal of Personality and Social Psychology. 2014;107(5):809-24.
23. Hellwig S, Roth M. Conceptual ambiguities and measurement issues in sensory processing sensitivity. Journal of Research in Personality. 2021;93.
24. Petrie KJ, Rief W. Psychobiological Mechanisms of Placebo and Nocebo Effects: Pathways to Improve Treatments and Reduce Side Effects. Annual Review of Psychology 2019. p. 599-625.
25. Rubin GJ, Hillert L, Nieto-Hernandez R, van Rongen E, Oftedal G. Do people with idiopathic environmental intolerance attributed to electromagnetic fields display physiological effects when exposed to electromagnetic fields? A systematic review of provocation studies. Bioelectromagnetics. 2011;32(8):593-609.
26. Rubin GJ, Nieto-Hernandez R, Wessely S. Idiopathic environmental intolerance attributed to electromagnetic fields (formerly ’electromagnetic hypersensitivity’): An updated systematic review of provocation studies. Bioelectromagnetics. 2010;31(1):1-11.
27. Bräscher AK, Schulz SM, Van den Bergh O, Witthöft M. Prospective study of nocebo effects related to symptoms of idiopathic environmental intolerance attributed to electromagnetic fields (IEI-EMF). Environmental Research. 2020;190.
28. Turnbull JL, Adams HN, Gorard DA. Review article: The diagnosis and management of food allergy and food intolerances. Alimentary Pharmacology and Therapeutics. 2015;41(1):3-25.
29. Winters W, Devriese S, Van Diest I, Nemery B, Veulemans H, Eelen P, et al. Media warnings about environmental pollution facilitate the acquisition of symptoms in response to chemical substances. Psychosomatic Medicine. 2003;65(3):332-8.
30. Goebel MU, Meykadeh N, Kou W, Schedlowski M, Hengge UR. Behavioral conditioning of antihistamine effects in patients with allergic rhinitis. Psychotherapy and Psychosomatics. 2008;77(4):227-34.
31. Wirth T, Ober K, Prager G, Vogelsang M, Benson S, Witzke O, et al. Repeated recall of learned immunosuppression: Evidence from rats and men. Brain, Behavior, and Immunity. 2011;25(7):1444-51.
32. Skvortsova A, Veldhuijzen DS, Kloosterman IEM, Meijer OC, van Middendorp H, Pacheco-Lopez G, et al. Conditioned hormonal responses: A systematic review in animals and humans. Frontiers in Neuroendocrinology. 2019;52:206-18.
33. Lowes S, Montero E. The legacy of colonial medicine in central africa. American Economic Review. 2021;11(4):1284-314.
34. Nunn N, Wantchekon L. The slave trade and the origins of Mistrust in Africa. American Economic Review. 2011;101(7):3221-52.
35. Nunn N. Historical legacies: A model linking Africa’s past to its current underdevelopment. Journal of Development Economics. 2007;83(1):157-75.
36. Freimuth VS, Quinn SC, Thomas SB, Cole G, Zook E, Duncan T. African Americans’ views on research and the Tuskegee Syphilis study. Social Science and Medicine. 2001;52(5):797-808.
37. Gamble VN. Under the Shadow of Tuskegee: African Americans and Health Care. American Journal of Public Health. 1997;87(11):1773-8.
38. Jaiswal J, Halkitis PN. Towards a More Inclusive and Dynamic Understanding of Medical Mistrust Informed by Science. Behavioral Medicine. 2019;45(2):79-85.
39. Scharf DP, Mathews KJ, Jackson P, Hofsuemmer J, Martin E, Edwards D. More than Tuskegee: Understanding mistrust about research participation. Journal of Health Care for the Poor and Underserved. 2010;21(3):879-97.
40. Shavers VL, Lynch CF, Burmeister LF. Knowledge of the Tuskegee Study and its impact on the willingness to participate in medical research studies. Journal of the National Medical Association. 2000;92(12):563-72.
41. Desai G, Chaturvedi S. Idioms of distress. Journal of Neurosciences in Rural Practice. 2017;8(5):94-7.
42. Kaiser BN, Haroz EE, Kohrt BA, Bolton PA, Bass JK, Hinton DE. ”Thinking too much”: A systematic review of a common idiom of distress. Social Science and Medicine. 2015;147:170-83.
43. Hinton DE, Lewis-Fernández R. Idioms of distress among trauma survivors: Subtypes and clinical utility. Culture, Medicine and Psychiatry. 2010;34(2):209-18.
44. Bäärnhielm S, Ekblad S. Introducing a psychological agenda for understanding somatic symptoms – An area of conflict for clinicians in relation to patients in a multicultural community. Culture, Medicine and Psychiatry. 2008;32(3):386-405.
45. Kirmayer LJ, Nutt, Lecrubier, Lepine, Davidson. Cultural variations in the clinical presentation of depression and anxiety: Implications for diagnosis and treatment. Journal of Clinical Psychiatry. 2001;62(SUPPL. 13):22-30.
46. Lewis-Fernández R, Aggarwal NK, Lam PC, Galfalvy H, Weiss MG, Kirmayer LJ, et al. Feasibility, acceptability and clinical utility of the Cultural Formulation Interview: Mixed-methods results from the DSM-5 international field trial. British Journal of Psychiatry. 2017;210(4):290-7.
47. Lewis-Fernandez R, Krishan Aggarwal N, Baarnhielm S, Rohlof H, Kirmayer LJ, Weiss MG, et al. Culture and psychiatric evaluation: Operationalizing cultural formulation for DSM-5. Psychiatry (New York). 2014;77(2):130-54.
48. Hughes T, Meredith F, Monteregge S, Bennett SD, Shafran R. Medically unexplained symptoms in children: An experimental investigation of the impact of internet searching on parental responses. Behavioural and Cognitive Psychotherapy. 2021;49(1):91-103.
49. Lupton D, Jutel A. ’It’s like having a physician in your pocket!’ A critical analysis of self-diagnosis smartphone apps. Social Science and Medicine. 2015;133:128-35.
50. Björk J. Just responsibilities? On responsibility for health in Swedish healthcare priority setting [Doctoral dissertation]. Stockholm, Sweden: Karolinska Institutet; 2021.
Nu finns möjlighet att lämna synpunkter på NNR-kapitlet om riboflavin
Alla kapitel i de nordiska näringsrekommendationerna 2022, NNR2022, kommer att vara tillgängliga för offentliga samråd. Först ut är kapitlet om riboflavin med möjlighet för forskare och andra intresserade att lämna synpunkter fram till den 21 april 2022.
Både kapitel om näringsämnen och livsmedelsgrupper kommer att ingå i NNR2022-rapporten. Kapitlen om livsmedelsgrupperna täcker in de flesta huvudgrupper av livsmedel inklusive drycker och ultraprocessade livsmedel.
Nordiska bär och rotfrukter till spädbarn – en grund för hälsosamma och hållbara matvanor som vuxen
Kosten under spädbarnstiden är viktig när barnet utvecklas och växer mycket snabbt och kan ge långsiktiga effekter på hälsan senare i livet. Under första levnadsåret utvecklas smakpreferenser och ätbeteenden genom inlärning och upprepade smakprover av till exempel bittra och sura smaker som finns i frukt, bär och grönsaker, vilket kan ge goda förutsättningar för hälsosamma och hållbara matvanor längre fram.
I Ulrica Johanssons avhandling ingår studien OTIS (Optimerad Tilläggskost i Sverige) som är den första studien som visar på hur nordisk kost (New Nordic Diet) kan introduceras redan under spädbarnstiden. OTIS är en randomiserad kontrollerad studie bland 250 friska svenska spädbarn mellan 4 och 18 månader gamla.
Barnen i den nordiska gruppen åt 42 till 45 procent mer av frukt och grönsaker per dag från 9 till 18 månaders ålder – i jämförelse med kontrollgruppen som följde de nationella råden. Det ökade intaget av växtbaserad mat och det lägre proteinintaget i den nordiska gruppen hade inga negativa effekter på barnens tillväxt, järn- eller nutritionsstatus.
>>text: Ulrica Johansson, med dr, legitimerad dietist och fil kand i Gastronomi, Institutionen för klinisk vetenskap, Enheten för pediatrik, Umeå universitet
Tidig programmering och framtida hälsa
Spädbarnstiden är en kritisk period med snabb tillväxt och utveckling, vilket ställer höga krav på optimal nutrition (1). Kostfaktorer som högt intag av protein, snabba kolhydrater och mättat fett ökar risken för fetma, blodfettsrubbningar, typ 2 diabetes och högt blodtryck, vilket kan ge långsiktiga effekter på hälsan (2). Välfärdssjukdomar som övervikt, fetma, typ 2 diabetes och hjärt- och kärlsjukdom kan spåras tillbaka till kostfaktorer under spädbarnstiden, den så kallade tidiga metabola programmeringseffekten (3).
Frukt, grönsaker och fullkorn har skyddande effekt mot välfärdssjukdomar och vissa cancerformer (4). Däremot är intaget av dessa livsmedel lågt bland barn och vuxna världen över trots skyddande effekt mot flertal sjukdomar och att dö i förtid. Det är viktig att tidigt i livet optimera nutritionen med tilläggskosten och samtidigt etablera smakpreferenser för hälsosam mat som frukt och grönsaker som kan påverka barnens kostmönster i framtiden (5). Det behövs också mer evidensbaserad forskning inom området.
Sensitiv period och smakinlärning
Spädbarnet lär sig tidigt i livet att äta och tycka om mat utifrån konsistenser och smaker som barnet erbjuds från olika livsmedel och maträtter. Spädbarn är mer mottagliga för olika smaker, även bittra och sura, under den sensitiva perioden när hjärnan är extra formbar och sinnena är mer mottagliga (6). Smakinlärning och upprepad exponering för bittra och sura smaker från frukt, bär och grönsaker vid introduktionen av tilläggskosten kan ge goda förutsättningar för hälsosamma och hållbara matvanor senare i livet (5). Däremot är det en begränsad tid i livet för ett ”smakfönster” och mottaglighet för att acceptera även sura och bittra smaker som kan bidra till en bredare smakinlärning (5, 6). Det är därför extra viktigt att ta tillvara på denna korta tid i livet när spädbarnet är mottagligt för alla sorters smaker (7, 8).
Mot slutet av första levnadsåret börjar barn normalt bli allt mer misstänksamma mot grönsaker och frukter. Problemet är att dessa är en viktig del av det som är hälsosamt att äta. Genom att systematiskt införa frukt och grönt i små barns kost kan man öka intaget av dessa livsmedel även när barnet blir äldre. När och hur man bäst gör detta är oklart. De nationella råden för introduktion av smakportioner baseras på tradition och kultur, därför är OTIS-studien viktig för att bidra med evidensbaserad forskning om tilläggskost för just svenska barn.
Tilläggskost – timing och sammansättning
De positiva hälsoeffekterna från amning och bröstmjölk är välstuderat. Men det saknas forskning kring den optimala tilläggskostens sammansättning och när och hur den introduceras. När spädbarnet från 4 till 6 månader för första gången får smakportioner, och senare efter 6 månader får mer fast föda, ställer det höga krav på att tillgodose energi, näring, järn och etablering av framtida matpreferenser (9). Tillvänjning under tilläggskosten innebär att barnet stegvis introduceras till smaker och konsistenser. Allt sker i samspel med föräldrar för att etablera ätbeteenden, acceptans för mat och för att barnet gradvis ska kunna övergå till familjens mat. Detta sker under en kort tid i livet som är väldigt viktig för framtida hälsa (10).
Det finns flera viktiga komponenter i tilläggskosten i form av typ av kolhydrater, fettkvalitet och proteinkällor, och mängder (11). I de nordiska länderna är proteinintaget under tilläggskosten 2 till 3 gånger högre än rekommendationerna och i huvudsak från animaliska proteinkällor (12). Studier har visat att för högt proteinintag under spädbarnstiden är relaterat till snabb tillväxt, högt BMI och ökad risk för övervikt och fetma senare under barndomen (12). Speciellt animaliskt protein från framför allt mejeriprodukter är relaterad till snabb tillväxt i jämförelse med vegetabiliskt protein (13). Däremot är forskningen bristfällig om hur vegetabiliskt protein påverkar barns tillväxt i olika åldrar (9). Animaliskt protein är en viktig källa för järn och järnbehovet är mycket stort under spädbarnstiden då tillväxt och utveckling sker mycket fort (9).
New Nordic Diet – en hållbar väg framåt
Ny nordisk mat, är ett initiativ från Nordiska ministerrådet som bygger på tre principer; hälsa, hållbarhet och gastronomi. Syfte är att främja regional mat som är säsongsbaserad med fokus på mer växtbaserad mat (14). Den nya nordiska kosten består av stor andel frukt, bär, grönsaker, rotfrukter, örter, svamp, fullkornsprodukter, fisk och fleromättat fett som rapsolja. Syftet är också att minska intaget av kött, processat kött, feta mejeriprodukter, socker och salt.
Studier på nordisk mat (New Nordic Diet) bland vuxna i Sverige (15) och andra nordiska länder har visat flera positiva resultat. Resultaten visade förbättringar i vikt och blodvärden som är kopplade till insulinresistens och hjärt- och kärlsjukdom. En stor randomiserad studie bland danska skolbarn (16-18), som fick nordisk mat under skolmåltiderna visade förbättrade kostfaktorer som ökat intag av rotfrukter, kål, bär, linser och fisk, och bättre kognitiva funktioner som skolprestationer och läsförståelse. De visade också förbättrad insulinresistens, minskat blodtryck och lägre blodfetter, och minskad risk för framtida välfärdssjukdomar. Bland gravida kvinnor i Norge (19) som följde den nordiska kosten fanns positiva associationer till optimal viktuppgång under graviditeten och gynnsam fostertillväxt.
OTIS studien (20) är den första att studera nordiska kosten New Nordic Diet som tilläggskost under spädbarnstiden under den kritiska metabola programmeringsfasen då smakpreferenser och ätbeteenden grundas. Den nordiska kosten har en stor variation av både bittra och sura smaker från bär och rotfrukter som kommer väl till pass i matintroduktion och smakinlärning hos spädbarn. Eftersom smakpreferenser grundläggs tidigt är det logiskt att introducera en nordisk kost redan när barnet börjar sin tillvänjning till fast föda, också för att bidra till hälsosamma och hållbara matvanor för barnet och hela familjen.
Hälsosamma och hållbara matvanor
Vi står inför stora utmaningar i framtiden att både äta hälsosamt och hållbart för planeten (21). Oftast går hälsosamt ätande hand i hand med planetens hälsa. Det innebär att vi behöver ställa om våra matvanor (22). Huvudråvaran vid lunch och middagar behöver i huvudsak komma från växtbaserad mat och mindre från animaliskt protein som kött och processade köttprodukter. Detta för att uppnå målen inom Agenda 2030 och EAT-Lancet kommitténs föreslagna klimatmål för hälsosam mathållning för människor och planeten (21, 22). De kommande nordiska näringsrekommendationerna 2022 innehåller riktlinjer om hur vi kan implementera hälsosam mat som är hållbar och klimatsmart på populationsnivå. Den nordiska kosten är både hälsosam och hållbar för oss nordbor och ett sätt att uppnå klimatmål och hälsomål (23). Det som behövs är verktyg och underlag för att omsätta denna kost i praktiken, en kost som ska vara gastronomisk, inspirerande, hälsosam och hållbar.
Om avhandlingen
Målsättning
Avhandlingens huvudsyfte var att undersöka spädbarnskost baserad på nordisk mat med minskad proteinmängd hos friska fullgångna svenska spädbarn fram till 18 månaders ålder och jämföra med de nationella rekommendationerna från Livsmedelsverket för spädbarn (24).
Metoder
Avhandlingen bygger på en randomiserad, kontrollerad studie (OTIS) bland 250 friska spädbarn från 4 till 6 månaders ålder som följdes till 18 månaders ålder i en multikomponent interventionsstudie (20, 24). En multikomponent interventionsstudie innehåller flera interventioner i syfte att försöka uppnå hållbara och hälsosamma ätbeteenden över tid som kan ha större effekt än en singelkomponent studie.
Interventionsgruppen i OTIS studien, det vill säga den nordiska gruppen (n=125), fick en tilläggskost baserad på nordisk mat med reducerad mängd protein (cirka 30 procent mindre per dag). Barnen i den nordiska gruppen fick systematiskt en variation av olika smaker från nordiska frukter, bär och grönsaker via ett smakschema under 24 dagar när de var mellan 4 och 6 månader. Från 6 till 18 månaders ålder fick barnen i den nordiska gruppen flera olika sorters interventioner, som att föräldrarna fick recept på hemlagad nordisk barnmat, familjerecept på nordisk mat, föräldrastöd på sociala medier och proteinreducerade nordiska barnmatsprodukter. Studien var interaktiv i barnets hemmamiljö och innehöll utbildningsmoment för föräldrarna.
Föräldrarna i kontrollgruppen (n=125) uppmanades följa rekommendationerna och råden för introduktion av smakportioner och tilläggskost från Livsmedelverket och barnhälsovården. De fick dessutom kommersiella barnmatsprodukter med vanligt innehåll av protein.
Vid studiestart (ca 4,5 månader) och vid 9, 12 och 18 månaders ålder samlades data in om barnens tillväxt, blodprover som folat, urea, järnparametrar, blodfetter etc., urinprover för kroppssammansättning, uppgifter om matintag från matdagböcker, videofilmade testmåltider i hemmet och enkäter om ätbeteenden. Båda grupperna hade tillgång till forskningskliniken på pediatrik för att ställa frågor och likaså inom barnhälsovården.
Resultat
Från studiens start vid 4 till 6 månader och fram till 18 månaders ålder fullföljde 206 barn (82 procent) studien (24). Fler barn lämnade den nordiska gruppen (n=30) än kontrollgruppen (n=14). Både grupperna startade studien vid 4,5 månaders ålder med sina första smakportioner vid sidan om amning eller flaskmatning. Det ingick fler pojkar än flickor i studien. Nästintill alla barnen i studien ammades. Amningsfrekvensen skiljde inte mellan grupperna under studien och var likvärdig med amningsdata från SCB i Västerbotten under samma tid. Majoriteten av föräldrarna var högutbildade, framför allt mammorna. Cirka hälften av deltagarna från båda grupperna hade syskon. Nästan alla mammor i studien oavsett grupp, var födda i Sverige och bland pappor/partner var 83 till 88 procent födda i Sverige.
Barnen i nordiska gruppen följde ett smakschema för upprepad smakinlärning av nordiska hemlagade puréer av frukter, bär och grönsaker under 24 dagar i rad när de var mellan 4 och 6 månader (25). De påbörjade smakschemat när det var 4,8 månader och avslutade vid 5,7 månaders ålder och genomförde smakschemat under 27 dagar, då de behövde 3 dagar extra på sig. Under dessa 27 dagar genomfördes 64 (87 procent) exponeringar/smakportioner varav 3 av dessa (5 procent) var vägringar av totala antalet exponeringar/smakportioner. Det visade att acceptansen hos barnen för alla smaker såsom söta, sura, beska och bittra är hög under denna tid och att vägringarna var få (26).
Av de åtta olika puréerna (smakportionerna) som serverades barnet fungerade alla smaker lika bra, det vill säga det åt lika mycket från varje smakportion/puré och vägrade inte mer av någon smakportion/puré (25). Puréerna som ingick var; äpple, gröna ärtor, hallon, blomkål, lingon/havtorn, majrova, tranbär, vit rättika. Eftersom havtorn är svår att få tag på kunde föräldrarna välja lingon. Bland föräldrarna i den nordiska gruppen anslöt 75 procent av familjerna till vår frivilliga Facebookgrupp för tips, möjligheten att chatta och ställa frågor till oss i forskningsteamet. Där fanns även filmer hur man tillagade alla smakportionerna/puréerna till smakschemat.
I den nordiska gruppen observerades positiva effekter på ätbeteendet genom ett ökat intag av frukt, bär, rotfrukter och grönsaker i jämförelse med kontrollgruppen. Barnen i den nordiska gruppen åt 42 till 45 procent mer av frukt och grönsaker per dag från 9 till 18 månaders ålder (24). Skillnaderna bekräftades även med högre nivå av plasma-folat, som ökar vid ökat frukt- och grönsaksintag. Det ökade intaget av växtbaserad mat och det lägre proteinintaget per dag i den nordiska gruppen påverkade inte barnens tillväxt, järnstatus eller nutritionsstatus negativt.
Proteinintaget var lägre i nordiska gruppen, 27 till 29 procent, vid 9 och 12 månader, och 17 procent vid 18 månader (24). Blodproverna på plasma-urea, som är en markör för proteinintag, visade också att proteinintaget varit lägre i den nordiska gruppen än i kontrollgruppen mellan 9 och 18 månaders ålder. Barnen i nordiska gruppen åt ändå tillräckligt med protein och låg över rekommenderad nivå från WHO. Olika typer av proteinkällor hos grupperna har inte ännu analyserats utifrån OTIS studien, och inte heller kroppssammansättningsdata.
Det specifika med the New Nordic Diet är att bland annat äta mer av nordiska bär och rotfrukter, och mindre av importerad mat. Den nordiska gruppen åt mer rotfrukter genom hela studien från 9 till 18 månaders ålder (24, 26). Likaså åt de mer bär genom hela studien i jämförelse med kontrollgruppen (24, 26). Kontrollgruppen åt mycket importerad exotisk frukt som banan, apelsin, ananas, mango och clementin. Barnen i den nordiska gruppen åt i princip inget (noll gram per dag på gruppnivå) av exotiska frukter som banan och mango.
Slutsatser
En tilläggskost baserad på nordiska råvaror och med reducerad mängd protein är genomförbart och säkert. Det lägre intaget av protein i nordiska gruppen gav inga negativa effekter på barnens tillväxt, järnstatus, amningsfrekvens eller andra biomarkörer i jämförelse med kontrollgruppen. I den nordiska gruppen observerades positiva effekter på ätbeteendet genom ett ökat intag av frukt, bär, rotfrukter och grönsaker. Dessa anses hälsosamma även om studien inte kan påvisa tydliga hälsoeffekter.
Föräldrastödet och tidig systematisk smakinlärning av olika sorters smaker har troligtvis bidragit till de ökade intaget av hälsosam mat hos spädbarnen i den nordiska gruppen. Nordiska bär och vissa rotfrukter är särskilt lämpade att ingå i matintroduktion och tilläggskost – för att främja smakinlärning och förhoppningsvis etablera framtida hälsosamma och miljömässigt hållbara matvanor.
Avslutande ord
I de nationella riktlinjerna för tilläggskost hos spädbarn ingår inte systematisk smakinlärning eller hur den första kosten i livet även kan vara miljömässigt hållbar. Det är ett område som vi tror behöver implementeras och utvecklas i framtiden. Det behövs också mer föräldrastöd under tilläggskosten för att stegvis integrera hela familjens matvanor. De nordiska råvarorna som bär och rotfrukter är något vi behöver ta tillvara på mer. Fler studier behövs inom området och de långsiktiga effekterna från OTIS-studien kommer följas upp när barnen är i skolåldern.
Vi äter det vi tycker om. Vi måste träna för att lära oss att tycka om det vi äter.
Inga jävsförhållanden. Delar av forskningen finansierades av Semper, men Semper var inte involverade i studiedesign, datainsamling, analyser, bearbetning av manuskript eller publiceringsprocessen.

Referenser
1. Gluckman PD, Hanson MA. Developmental and epigenetic pathways to obesity: an evolutionary-developmental perspective. International Journal of Obesity. 2008;32(7):62–71.
2. Craigie AM, Lake AA, Kelly SA, Adamson AJ, Mathers JC. Tracking of obesity-related behaviours from childhood to adulthood: A systematic review. Maturitas. 2011;70:266–84.
3. Koletzko B, Brands B, Chourdakis M, Cramer S, Grote V, Hellmuth C, et al. The Power of Programming and the Early Nutrition Project: Opportunities for Health Promotion by Nutrition during the First Thousand Days of Life and Beyond. ANM. 2014;64(3–4):187–96.
4. World Health Organization. Global Status Report on Non Communicable Diseases 2010. World Health Organization: Geneva, Switzerland, 2011.
5. Birch L, Savage JS, Ventura A. Influences on the Development of Children’s Eating Behaviours: From Infancy to Adolescence. Can J Diet Pract Res. 2007;68:1–56.
6. Harris G, Mason S. Are There Sensitive Periods for Food Acceptance in Infancy? Curr Nutr Rep. 2017;6:190–6.
7. Mennella JA, Trabulsi JC. Complementary Foods and Flavor Experiences: Setting the Foundation. Ann Nutr Metab. 2012;60:40–50.
8. Birch LL. Development of food preferences. Annu Rev Nutr. 1999;19:41–62.
9. Fewtrell M, Bronsky J, Campoy C, Domellöf M, Embleton N, Fidler Mis N, et al. Complementary Feeding: A Position Paper by the European Society for Paediatric Gastroenterology, Hepatology, and Nutrition (ESPGHAN) Committee on Nutrition. Journal of Pediatric Gastroenterology and Nutrition. 2017;64(1):119–32.
10. Coulthard H, Harris G, Emmett P. Delayed introduction of lumpy foods to children during the complementary feeding period affects child’s food acceptance and feeding at 7 years of age. Maternal & Child Nutrition. 2009;5:75–85.
11. Rolland-Cachera MF, Deheeger M, Akrout M, Bellisle F. Influence of macronutrients on adiposity development: a follow up study of nutrition and growth from 10 mo to 8 y of age. Int J Obes. 1995;19:573–8.
12. Hörnell A, Lagström H, Lande B, Thorsdottir I. Protein intake from 0 to 18 years of age and its relation to health: a systematic literature review for the 5th Nordic Nutrition Recommendations. Food Nutr Res. 2013:57:21083.
13. Hoppe C, Rovenna Udam T, Lauritzen L, Mølgaard C, Juul A, Fleischer Michaelsen K. Animal protein intake, serum insulin-like growth factor I, and growth in healthy 2.5-y-old Danish children. Am J Clin Nutr. 2004;80(2):447–52.
14. Mithril C, Dragsted LO, Meyer C, Blauert E, Holt MK, Astrup A. Guidelines for the new nordic diet. Public Health Nutr. 2012;15:1941–7.
15. Adamsson V, Reumark A, Fredriksson IB, Hammarstrom E, Vessby B, Johansson G, et al. Effects of a healthy Nordic diet on cardiovascular risk factors in hypercholesterolaemic subjects: a randomized controlled trial (NORDIET). J Intern Med. 2011;269:150–9.
16. Andersen R, Biltoft-Jensen A, Christensen T, Andersen EW, Ege M, Thorsen AV, et al. Dietary effects of introducing school meals based on the New Nordic Diet – a randomised controlled trial in Danish children. The OPUS School Meal Study. Br J Nutr. 2014;111:1967–76.
17. Andersen R, Biltoft-Jensen A, Andersen EW, Ege M, Christensen T, Ygil KH, et al. Effects of school meals based on the New Nordic Diet on intake of signature foods: a randomised controlled trial. The OPUS School Meal Study. British Journal of Nutrition. 2015;114(5):772–9.
18. Sørensen LB, Damsgaard CT, Dalskov S-M, Petersen RA, Egelund N, Dyssegaard CB, et al. Diet-induced changes in iron and n-3 fatty acid status and associations with cognitive performance in 8-11-year-old Danish children: secondary analyses of the Optimal Well-Being, Development and Health for Danish Children through a Healthy New Nordic Diet School Meal Study. Br J Nutr. 2015;1–15.
19. Skreden M, Hillesund ER, Wills AK, Brantsæter AL, Bere E, Øverby NC. Adherence to the New Nordic Diet during pregnancy and subsequent maternal weight development: a study conducted in the Norwegian Mother and Child Cohort Study (MoBa). British Journal of Nutrition. 2018;119(11):1286–94.
20. Lind T, Johansson U, Öhlund I, Lindberg L, Lönnerdal B, Tennefors C, Hernell O. Study protocol: optimized complementary feeding study (OTIS): a randomized controlled trial of the impact of a protein-reduced complementary diet based on Nordic foods. BMC Public Health. 2019;19:134. DOI:10.1186/S12889-019-6466-1.
21. Willett W, Rockström J, Loken B, Springmann M, Lang T et al. Food in the Anthropocene: the EAT–Lancet Commission on healthy diets from sustainable food systems. Lancet. 2019;393:447–92.
22. Food and Agriculture Organization of the United Nations and World Health Organization. Sustainable healthy diets: guiding principles. 2019. Internet: http://www.fao.org/3/ca6640en/ca6640en.pdf
23. Meltzer HM, Brantsæter AL, Trolle E, Eneroth H, Fogelholm M, Ydersbond TA, et al. Environmental Sustainability Perspectives of the Nordic Diet. Nutrients. 2019;11(9).
24. Johansson U. Complementary feeding based on Nordic foods: effects on nutrient intake, growth, biomarkers and eating behavior. Umeå University medical dissertations, 2021. Internet: http://umu.diva-portal.org/smash/get/diva2:1609343/FULLTEXT01.pdf
25. Johansson U, Öhlund I, Hernell O, Lönnerdal B, Lindberg L, Lind T. Protein-reduced complementary foods based on Nordic ingredients combined with systematic introduction of taste portion increase intake of fruits and vegetables in 9-month-old infants: A randomized controlled trial. Nutrients. 2019; 11:1255. DOI:10.3390/nu11061255.
26. Johansson U, Lindberg L, Öhlund I, Hernell O, Lönnerdal B, Lundén S, Sandell M, Lind T. Acceptance of a Nordic protein-reduced diet for young children during complementary feeding: A randomized controlled trial. Foods. 2021; 10:2
Bra mat vid diabetes – SBU:s utvärdering är klar
Statens beredning för medicinsk och social utvärdering (SBU) har utvärderat det vetenskapliga stödet för hälsoeffekter av mat vid diabetes. Nu är utvärderingen ”Mat vid diabetes” publicerad.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
I utvärderingen ingår studier med typ 1-, typ 2- och graviditetsdiabetes. Även hälsoekonomiska och etiska faktorer ingår. Projektet har utvärderat positiva och negativa hälsoeffekter för människor med diabetes relaterat till olika typer av kost, kostbehandlingar, vissa livsmedel, näringsämnen och drycker. Studierna undersökte en rad hälsoeffekter. Där ingick nivåer av blodglukos och blodfetter, diabeteskomplikationer, som till exempel hjärt- och kärlsjukdomar, nervskador och för tidig död. Deltagarna som ingick i studierna var 18 år och äldre.
Utvärderingen visar att det finns ett samband mellan medelhavskost och lägre risk att dö i förtid vid diabetes typ 1 och typ 2. Medelhavskosten liknar de nordiska kostråden som grundar sig på de nordiska näringsrekommendationerna.
Utvärderingen visar att det finns ett samband mellan lägre risk att dö i förtid vid diabetes typ 1 och typ 2 och att äta mer fibrer, till exempel grovt bröd, grönsaker och frukt, baljväxter och dricka kaffe. Det kan även finnas ett samband mellan att äta mer nötter och lägre risk att dö i förtid, men bevisstyrkan är något lägre för nötter.
Utvärderingen visade även att två behandlingsmetoder inom vården för att minska i vikt hos personer med diabetes typ 2 medför flera hälsoförbättringar. Det handlar till exempel om högre livskvalitet, lägre blodsocker och större viktminskning än vanlig kostbehandling:
- Kraftigt minskat energiintag under en period med hjälp av så kallat lågenergipulver (VLED) och därefter övergång till mat för att hålla den nya vikten.
- Intensiv livsstilsbehandling där lågfettkost kombineras med fysisk aktivitet och minskat energiintag.
För graviditetsdiabetes saknas studier om kost med tillräcklig tillförlitlighet för att kunna dra slutsatser.
SBU använder en omfattande process för att säkerställa att resultaten i utvärderingar är vetenskapligt väl underbyggda. I processen ingår en strukturerad litteratursökning, granskning av studierna som ingår i utvärderingen och bedömning av hur tillförlitliga det sammanvägda resultatet från alla studier är. I denna utvärdering ingick 81 artiklar.
SBU:s rapport utgör underlag till ett nytt kunskapsstöd från Socialstyrelsen om mat vid diabetes.
Länk till sammanfattning inklusive beskrivning av de 81 artiklar som ingår i utvärderingen.
Protein och tillväxt hos barn – först ut bland de systematiska litteraturöversikterna för NNR2022
Systematiska litteraturöversikter är en del av uppdateringen av de nordiska näringsrekommendationerna, NNR2022. Den första översikten handlar om sambandet mellan intag av protein hos barn och tillväxt samt risk för övervikt och fetma upp till 18 års ålder.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
Översikterna är omfattande och ger en samlad bedömning av den vetenskapliga litteraturen inom varje område man valt att undersöka. Den första publicerade översikten är en av nio planerade systematiska litteraturöversikter, som görs enligt en arbetsprocess i flera steg som är systematisk och transparent och tidigare publicerad i Food Nutrition Research.
För att hitta de mest relevanta artiklarna i flera olika databaser, som till exempel MEDLINE och Embase, tar forskarna tillsammans med forskningsbibliotekarier fram en sökstrategi. Därefter bedömer forskarna om artiklarna följer de riktlinjer som utformats, och alla studier som inkluderas i översikten bedöms för att utesluta snedvridning av resultaten, alltså risk för bias. Vid bedömningarna granskar forskarna bland annat om studierna som ingår har svarat på forskningsfrågan, är av bra kvalitet och att resultaten är tillförlitliga.
Samband mellan totalt proteinintag och BMI, men inte övervikt och fetma
Totalt inkluderades 21 studier i den systematiska litteraturaturöversikten: fem randomiserade kliniska studier och 16 kohortstudier. De randomiserade kliniska studierna visade ingen effekt av högt proteinintag på viktuppgång och inte heller lågt proteinintag visade någon effekt på vikten. Forskarna bedömde emellertid att de randomiserade kliniska studierna har risk för bias och att studierna är små.
I elva av de 12 kohortstudierna fanns ett samband mellan totalt intag av protein och högre BMI. En metaanalys, där flera av kohortstudiernas resultat vägdes samman, genomfördes av forskarna och stärkte resultatet.
Resultatet från den systematiska litteraturgenomgången visade sedan ett samband mellan högre totalt intag av protein hos spädbarn – upp till 1,5 års ålder – och högre BMI senare under barndomen. Samma samband fanns för intag av animaliskt protein, till exempel från kött och mejeriprodukter. I evidensgraderingen benämns styrkan på sambandet som sannolik evidens, vilket räknas som ett ganska starkt bevis. Det starkaste beviset – den högsta evidensgraderingen är övertygande – fanns inte här.
För det totala proteinintaget och risk för övervikt och/eller fetma var sambandet begränsat och tvetydigt, det vill säga låg bevisstyrka. Inga slutsatser kunde dras beroende på om proteinkällan var växtbaserad eller animalisk.
Se också tidigare publicerat om NNR2022 på Nutritionsfakta
 Tabellen kommer ursprungligen från artikeln Systematiska litteraturöversikter för NNR2022 – så arbetar det nya centret
Tabellen kommer ursprungligen från artikeln Systematiska litteraturöversikter för NNR2022 – så arbetar det nya centret
Länk till World Cancer Research Fund
EAT-Lancetkosten undersökt i svensk studie
EAT-Lancetkommissionen lanserade 2019 sin ”the great food transformation”, en modell för hälsosamma matvanor för en växande global befolkning som skulle hålla livsmedelssystemet inom planetens gränser.
En uppföljande svensk studie har tagit fram ett eget index för att mäta följsamheten till EAT-Lancetkosten, med en poängsättning som gör det möjligt att se hur väl en person följer EAT-Lancetkosten för olika livsmedel.
Studien baserade sig på data från den omfattande befolkningskohorten Malmö Kost Cancer. Resultatet visar bland annat att de med högst följsamhet till EAT-Lancetkosten enligt indexet hade en 25 procent lägre risk att dö i förtid, 24 procent lägre risk att dö i cancer och 32 procent lägre risk att dö i hjärt-kärlsjukdom. Studien visar att flera livsmedel verkade bidra till detta resultat, vilket understryker vikten av en allmänt hälsosam kost, skriver Anna Stubbendorff.
>>text: Anna Stubbendorff, nutritionist och doktorand, Institutionen för kliniska vetenskaper, Lunds universitet, Malmö
Bakgrund
En omställning till hållbara kostvanor är nödvändigt för att uppnå FN:s mål för hållbar utveckling för att vi ska hålla oss inom de planetära gränserna (1-3). Jordbruket står för 25 till 30 procent av världens utsläpp av växthusgaser och har stor inverkan på flera andra miljöfaktorer (4, 5). Dessutom är våra matvanor en viktig bidragande orsak till sjukdom och död i förtid globalt (6). Icke smittsamma sjukdomar står för 71 procent av alla dödsfall globalt, och studier visar att hälsosamma kostmönster avsevärt skulle minska risken för sjuklighet och dödlighet från dessa sjukdomar (6-8).
I ”EAT-Lancet-kommissionen” samlades 37 internationellt erkända forskare i ett samarbete mellan tidskriften The Lancet och stiftelsen EAT. I sin rapport från 2019 lanserade kommissionen ”the great food transformation”, en modell för hur livsmedelssystemet skulle hålla sig inom planetens gränser. Omvandlingen baserade sig på hållbarhet och hälsosamma kostvanor för en växande global befolkning (9).
Kommissionen presenterade en hälsosam referensdiet – EAT-Lancetkosten – med syfte att vara både miljömässigt hållbar och förhindra kostrelaterade kroniska sjukdomar och död i förtid (9). EAT-Lancetkosten är huvudsakligen växtbaserad, med ett begränsat innehåll av animaliska livsmedel, socker och mättat fett. Dessutom ingår ett högt innehåll av fullkorn, grönsaker, frukt, baljväxter och nötter.
Forskarna bakom kosten uppskattade, baserat på simuleringar, att kosten skulle förhindra cirka 11 miljoner dödsfall per år, motsvarande 19–24 procent av de totala dödsfallen globalt. Eftersom det var en simulering har forskargrupper sedan studerat effekten på människor som ätit mer eller mindre som EAT-Lancetkosten. Studierna har baserats på kostindex för att kunna mäta efterlevnaden (10-12), men det finns ännu ingen konsensus om vilket som är det bästa måttet.
Knuppel och medarbetare (10) föreslog 2019 det hittills mest använda kostindexet för att mäta följsamhet till EAT-Lancetkosten. Forskningen har visat att höga indexpoäng i detta index, alltså god efterlevnad, är associerat med minskad risk för hjärt-kärlsjukdom och diabetes – men däremot fanns ingen koppling till stroke och dödlighet totalt. I indexet enligt Knuppel och medarbetare är antalet möjliga poäng snävt, vilket gör att det har begränsad möjlighet att fånga intagsvariationer utanför föreslagna referensnivåer för EAT-Lancetkosten. Indexet definierar baljväxter, fisk och fullkorn som livsmedel som bör begränsas, något som vi ställde oss frågande till.
I vår studie var syftet att ta fram ett nytt index för att mäta följsamheten till EAT-Lancetkosten. Det nya indexet är baserat på en ny poängsättning som gör att vi kan mäta hur väl en person följer EAT-Lancetkosten för olika livsmedel. Dessutom har vi till skillnad från Knuppel och medarbetare definierat baljväxter, fisk och fullkorn som livsmedelsgrupper vi bör öka vår konsumtion av. Syftet var också att utvärdera följsamheten till EAT-Lancetkosten och dess samband med död i förtid i en stor befolkningsbaserad svensk kohort – Malmö Kost Cancer. Vi undersökte också enskilda livsmedel som ingår i indexet och deras individuella samband med död i förtid.
Malmö Kost Cancer studien
Malmö Kost Cancer är en befolkningsbaserad kohortstudie som genomfördes i Malmö, där den första omgången data samlades in mellan 1991 och 1996. Män i åldern 46–73 år och kvinnor i åldrarna 45–73 år ingick i studien. Information om livsstil och socioekonomiska faktorer samlades in och blodprover och blodtryck mättes. Kartläggningen av kosten var omfattande och bestod av en 7-dagars matdagbok, ett frekvensformulär (FFQ) och en kostintervju. Totalt ingick 22 421 individer, 8 568 män och 13 853 kvinnor.
EAT-Lancetindex
I vår studie utvecklade vi ett index för att undersöka sambandet mellan EAT-Lancetkosten och död i förtid (13). EAT-Lancetkosten består av livsmedel med för vilka definierade målintagsnivåer och referensintervall föreslås. Målintagsnivåerna är framtagna för hälsa och miljömässig hållbarhet och är baserade på ett intag på 2500 kcal per person och dag. Referensintervallen är intervall som anses vara förenliga med optimal hälsa i olika populationer och möjliggör intag vid olika energinivåer (9).
I vår studie klassificerades livsmedel som antingen ”livsmedel att öka” eller ”begränsade livsmedel”, baserat på tidigare beskrivningar av EAT-Lancetkosten (9, 14). Livsmedel att öka var grönsaker, frukt, omättade oljor, baljväxter, fullkorn, nötter och fisk. Livsmedel att begränsa var nötkött och lamm, fläsk, fågel, ägg, mejeriprodukter, potatis och tillsatt socker.
Vårt index består av dessa 14 livsmedel, med ett möjligt intervall på 0 till 3 poäng för varje livsmedel; 0 poäng anger låg följsamhet till målet för livsmedelskomponenten i EAT-Lancetkosten, och 3 poäng anger hög följsamhet. Det totala möjliga poängintervallet för detta utvecklade index är 0 (icke-följsamhet) till 42 poäng (perfekt efterlevnad, alltså 14×3 poäng).
I analyserna delades deltagarna in i fem grupper efter total indexpoäng – ≤ 13, 14–16, 17–19, 20–22 och ≥ 23 poäng. Den lägst rankade gruppen, ≤ 13, hade lägst följsamhet och den högst rankade gruppen, ≥ 23, räknas som hög följsamhet. Så kallad Cox-regression användes för att undersöka sambanden mellan EAT-Lancetpoängen och riskkvoterna för total dödlighet, cancerdödlighet och kardiovaskulär dödlighet. Vi tog också hänsyn till andra livsstilsfaktorer.
Tabell 1. Poängsättning för intag av olika livsmedel i EAT-Lancetindexet (13).

EAT-Lancetindex, efterlevnad och bakgrund
Resultaten visade stora variationer i efterlevnaden och deltagare i studien fick mellan 5 och 35 poäng på EAT-Lancetindexet. Kvinnor hade högre följsamhet till EAT-Lancetkosten. Mindre än 1 procent av studiepopulationen nådde målintaget för baljväxter och nötter i EAT-Lancetkosten. Dessutom nådde mindre än 5 procent målintaget för fullkorn, nöt- och lammkött samt fläsk. Följsamheten var högst för fågel, 77 procent, och fisk, 66 procent. Kvinnor hade högre indexpoäng, alltså bättre efterlevnad, för alla livsmedelskomponenter – förutom för fullkorn, fisk och omättade oljor.
De med hög efterlevnad av EAT-Lancetkosten – högre poäng – hade lägre totalt energiintag och en kost som innehöll mindre fett och kolhydrater, och mer kostfiber jämfört med dem med låg följsamhet. Deltagarna med hög följsamhet till EAT-Lancetkosten var något äldre, rökte oftast mindre och färre bland dem hade hög alkoholkonsumtion. Dessutom hade de högre utbildning och var mer fysiskt aktiva. Förekomsten av övervikt var ungefär densamma i grupperna.
EAT-Lancetindex och risk att dö i förtid
Våra huvudsakliga fynd visade att de med högst följsamhet till EAT-Lancetkosten – mer än 23 poäng – hade en 25 procent lägre risk att dö i förtid. Hög följsamhet till EAT-Lancetkosten visade också en 24 procent lägre risk att dö i cancer och 32 procent lägre risk att dö i hjärt-kärlsjukdom. Studien visar att flera livsmedel verkade bidra till detta resultat, vilket understryker vikten av en allmänt hälsosam kost.
Följsamhet till var och en av de 14 grupper av livsmedel som ingår i EAT-Lancetindexet och dödlighet testades också separat. Högt intag av fullkorn, grönsaker och frukt, jämfört med lågt intag, var associerat med en lägre risk för dödlighet av alla orsaker. Ett högt intag av ägg var däremot förknippat med en högre risk. Dessutom tenderade högt intag av potatis att vara associerat med en högre risk för dödlighet än ett lågt intag. Det genomsnittliga intaget av baljväxter i vår studie var endast 6 gram om dagen, vilket är långt ifrån målet på 75 gram i EAT-Lancetkosten. Detta tyder på att studiepopulationen är olämplig för undersökning av hälsoresultat i relation till baljväxtintag. Konsumtionen av nötter var också långt ifrån målen i EAT-Lancetkosten.
Styrkor och svagheter i studien
Styrkan med denna studie är den omfattande uppföljningsperioden på i genomsnitt 20 år. Den kostundersökningsmetod som används i Malmö Kost Cancer studien indikerar att kostdatan som samlas in är tillförlitlig. En begränsning kan vara att väldigt få deltagare i vår studie följde de övergripande rekommendationerna i EAT-Lancetkosten. Inga deltagare var nära att få 42 poäng i indexet, och en potentiell ytterligare minskning av dödligheten skulle kunna vara möjlig för högre poäng. Alla kostundersökningsmetoder innebär också en viss grad av felaktig rapportering. Dessutom kan individer endast rangordnas på olika intagsnivåer när de jämförs med andra deltagare i studien. Följaktligen kan vi inte relatera hälsoutfall till exakta intagsnivåer.
Grönsaker delades in i kategorier baserade på färg i EAT-Lancetkosten. Detta var inte möjligt i vår studie på grund av brist på data om undergrupper av grönsaker. Vidare föreslog Willett och medarbetare (9) utbytbarhet mellan olika livsmedelsgrupper, till exempel att kyckling och annat fjäderfä skulle vara utbytbart med ägg, fisk eller växtproteiner i EAT-Lancetkosten, en dimension vi inte kunde inkludera i vårt index.
Användning av indexet
I framtida studier skulle vårt index kunna användas i relation till förekomsten av kroniska sjukdomar såsom diabetes, cancer och hjärtkärlsjukdom. Vidare tror vi att det vore intressant att studera intag av näringsämnen i relation till behov i olika åldersgrupper, även om modelleringsstudier visar ett tillräckligt intag av de flesta näringsämnen med EAT-Lancetkosten (9, 15).
Att tillämpa indexet på dagens matvanor skulle också vara ett intressant område för framtida forskning, eftersom dagens konsumtionsmönster skiljer sig från matvanorna på 1990-talet som undersöktes i denna kohortstudie. Även en utvärdering av vårt index i andra populationer, inklusive de i låg- eller medelinkomstländer, skulle vara relevant för att testa och utveckla indexet för global användning. På samma sätt skulle det vara värdefullt att jämföra olika typer av EAT-Lancetindex med avseende på olika sjukdomar.
Vi är bekanta med debatten om EAT-Lancetkosten. Kritik finns av de metodologiska övervägandena, bristande anpassning till lokala sammanhang och olika populationer. Dessutom pekar kritiker på att kostnaden är ett hinder för att genomföra en ändring av matvanorna enligt EAT-Lancetkosten och saknade miljöperspektiv (11, 16-20). Trots dessa förbehåll ger ändå de avsevärda minskningarna av risk att dö i förtid som visas i denna studie starka argument för att prioritera hälsosamma kostvanor som liknar EAT-Lancetkosten. Våra resultat visar värdet av kostmönstret som helhet vilket kan vara användbart vid utveckling av hållbara kostriktlinjer och policyer.
Författaren uppger inga jävsförhållanden
Länk till studien: https://doi.org/10.1093/ajcn/nqab369
Referenser
1. Springmann M, et al. Options for keeping the food system within environmental limits. Nature 2018; 562(7728): 519-525.
2. Fanzo J. Healthy and Sustainable Diets and Food Systems: the Key to Achieving Sustainable Development Goal 2? Food Ethics 2019; 4(2): 159-174.
3. FAO och WHO. Sustainable healthy diets – guiding priciples. F.a. WHO, 2019: Rome.
4. IPCC (The Intergovernmental Panel on Climate Change). Climate Change 2014: Mitigation of Climate Change: Working Group III Contribution to the IPCC Fifth Assessment Report. 2015, Cambridge: Cambridge University Press.
5. IPCC (The Intergovernmental Panel on Climate Change). Climate Change and Land, an IPCC special report on climate change, desertification, land degradation, sustainable land management, food security, and greenhouse gas fluxes in terrestrial ecosystem. 2019.
6. Murray CJL, et al. Global burden of 87 risk factors in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. The Lancet 2020; 396(10258): 1223-1249.
7. Willett WC och Stampfer MJ. Current evidence on healthy eating. Annu Rev Public Health 2013; 34: 77-95.
8. World Health Organization (WHO) (2021). Global Health Observatory (GHO). [Hämtad 2021 04-06]. Från: www.who.int/data/gho.
9. Willett W, et al. Food in the Anthropocene: the EAT-Lancet Commission on healthy diets from sustainable food systems. Lancet 2019.
10. Knuppel A, et al. EAT-Lancet score and major health outcomes: the EPIC-Oxford study. The Lancet 2019; 394(10194): 213-214.
11. Hanley-Cook GT, et al. EAT–Lancet diet score requires minimum intake values to predict higher micronutrient adequacy of diets in rural women of reproductive age from five low- and middle-income countries. British Journal of Nutrition 2020; 1-9.
12. Cacau LT, et al. Development and Validation of an Index Based on EAT-Lancet Recommendations: The Planetary Health Diet Index. Nutrients 2021; 13(5): 1698.
13. Stubbendorff A, et al. Development of an EAT-Lancet index and its relation to mortality in a Swedish population. The American Journal of Clinical Nutrition 2021.
14. Loken B och DeClerk F. Diets for a better future – Rebooting and reimagining healthy and sustainable food systems in the g20. 2020.
15. Lassen AD, et al. Development of a Danish Adapted Healthy Plant-Based Diet Based on the EAT-Lancet Reference Diet. Nutrients 2020; 12(3).
16. Zagmutt FJ, et al. The EAT-Lancet Commission: a flawed approach? The Lancet 2019; 394(10204): 1140-1141.
17. Hirvonen K, et al. Affordability of the EAT-Lancet reference diet: a global analysis. The Lancet Global Health 2020; 8(1): e59-e66.
18. Semba RD, et al. Adoption of the ‘planetary health diet’ has different impacts on countries’ greenhouse gas emissions. Nature Food 2020; 1(8): 481-484.
19. Steenson S och Buttriss JL. The challenges of defining a healthy and ‘sustainable’ diet. Nutrition Bulletin 2020; 45(2): 206-222.
20. Zagmutt FJ, et al. The EAT-Lancet Commission’s Dietary Composition May Not Prevent Noncommunicable Disease Mortality. The Journal of Nutrition 2020.
Systematiska litteraturöversikter för NNR2022 – så arbetar det nya centret
Arbetet med de nordiska näringsrekommendationerna 2022 (NNR2022) är i full gång. I skrivande stund ligger fokus på de systematiska översiktsartiklarna. Artiklarna är viktiga, eftersom de är grunden till de referensvärden som ska ingå i näringsrekommendationerna och de svenska kostråden. Arbetet sker systematiskt och transparent i tydliga steg, en process som sedan tidigare finns publicerade i en vetenskaplig tidskrift.
>>text: Fredrik Söderlund, MSc och Agneta Åkesson, professor, enheten för kardiovaskulär- och nutritionsepidemiologi, Institutet för miljömedicin (IMM), Karolinska Institutet, Stockholm
Experter inom NNR-SR Centre
Den sektion inom NNR2022 som står för de nya systematiska översiktsartiklarna kallas för NNR Systematic Review Centre (NNR-SR Centre) och består av experter inom nutrition och metodologi från Sverige, Norge, Finland och Island:
- Agneta Åkesson, Karolinska Institutet, Sverige (arbetsledare)
- Christel Lamberg-Allardt, Helsingfors universitet, Finland
- Erik Arnesen, Universitetet i Oslo, Norge
- Linnea Bärebring, Göteborgs universitet, Sverige
- Bright Nwaru, Göteborgs universitet, Sverige
- Jutta Dierkes, Universitetet i Bergen, Norge
- Birna Thorisdottir, University of Iceland, Island
- Alfons Ramel, University of Iceland, Island
- Fredrik Söderlund, Karolinska Institutet, Sverige
Inkluderade ämnen
Uppdraget för NNR-SR Centre är att på ett transparant och systematiskt arbetssätt sammanställa all tillgänglig forskning inom områden som valts ut av NNR2022-kommittén, sammanlagt nio ämnen:
1. Växtbaserat protein hos småbarn och tillväxt
2. Växtbaserat protein jämfört med animaliskt protein och hjärt- kärlsjukdom samt typ 2-diabetes
3. Vitamin B12och vitamin B12-status i riskgrupper
4. Fettkvalitet och kognitiv nedsättning och demens
5. Baljväxter i relation till hjärt-kärlsjukdom och typ 2-diabetes
6. Vitt kött (främst kyckling) i relation till hjärt-kärlsjukdom och typ 2-diabetes
7. Pre- eller postnatalt tillskott av omega 3-fettsyror kopplat till astma/allergier hos barn
8. Nötter relaterat till hjärt-kärlsjukdom och typ 2-diabetes
9. Högt intag av kostfiber relaterat till tillväxt, järnstatus och tarmfunktion hos småbarn
Utifrån dessa ämnen har kommittén definierat en forskningsfråga och skapat ett PI/ECOTSS som NNR-SR Centre förhåller sig till. Ett PI/ECOTSS är ett protokoll som definierar vilka komponenter som ska ingå i forskningsfrågan: P: population, I/E: intervention/exponering, C: kontroll/jämförelse (Eng.: control), O: resultat (Eng.: outcome), T: tidsram, S: miljö (Eng.: setting), S: studiedesign. En utförligare förklaring av PI/ECOTSS är sedan tidigare publicerad på Nutritionsfakta.
Arbetsprocessen för de systematiska litteraturöversikterna har sedan tidigare publicerats i den vetenskapliga tidskriften Food and Nutrition Research (1, 2). Arbetet är uppdelat i ett flertal moment där varje steg utförs av minst två experter som gör varsin bedömning. Eventuell oenighet avgörs av en tredje person.
Sommaren 2021 presenterade NNR2022-kommittén preliminärt vilka ämnen de systematiska litteraturöversikterna skulle omfatta. Då ingick också en systematisk litteraturöversikt om intag av D-vitamin och D-vitaminstatus, men i det slutgiltiga beslutet ingår inte D-vitamin. Detta beror bland annat på att det publicerats en hel del inom området av andra organisationer.
Arbetsprocessen
Samtliga litteraturöversikter genomgår samma systematiska arbetsprocess som är uppdelade i åtta steg.
1. Utveckla protokoll och registrera arbetssättet i PROSPERO*
Den första punkten i processen handlar om att tydligt definiera och registrera arbetssättet innan arbetet tar fart. Detta görs för att arbetet ska ske systematiskt och transparant. Från detta utgår resten av arbetet.
2. Planera sökstrategi och utföra litteratursökning
Sökstrategin planeras tillsammans med forskningsbibliotekarier för att hitta de mest relevanta artiklarna för forskningsfrågan. Här beslutas vilka söktermer som ska användas och vilka databaser som ska genomsökas. Bibliotekarierna utför därefter litteratursökningen.
3. Screening av abstrakt
När litteratursökningen är avklarad utförs en screening av samtliga abstrakt i det webbaserade programmet Rayyan. Här sker den första selektionen av artiklar och de som inte är relevanta för forskningsfrågan sållas bort. För varje litteraturöversikt screenas först 10 procent av alla artiklar för att se om sökstrategin varit lyckad. Om sökstrategin anses lyckad så screenas resterande 90 procent av abstrakten. I det här skedet reduceras det största antalet artiklar.
4. Läsning av artiklar i full-text
De artiklar som anses relevanta utifrån abstrakten läses i fulltext innan beslut tas. Bedöms artiklarna följa de riktlinjer som utformats i PI/ECOTSS och PROSPERO inkluderas de i litteraturöversikten.
5. Dataextraktion
För varje litteraturöversikt skapas ett underlag i form av tabeller som specificerar vilken information som ska samlas in från de inkluderade artiklarna. Tabellerna används sedan som underlag vid bedömning av risken för bias (snedvridning av resultaten), vid rapportskrivning och vid metaanalyser (inom de litteraturöversikter där en metaanalys anses lämplig). I en metaanalys vägs resultat från flera studier samman genom att studier med likartad frågeställning samlas ihop och nya statistiska analyser görs.
6. Bedömning av risken för bias
Varje studie som inkluderats genomgår även en bedömning av risk för bias. Bedömningen, som är en stor del av arbetet, utförs för att fastställa om studien genomförts på ett korrekt sätt, om resultaten kan anses pålitliga och om artikeln svarat på forskningsfrågan på ett korrekt sätt. Det finns flera verktyg tillgängliga för bedömningen och i dessa systematiska litteraturöversikter används verktyget ‘Risk of bias 2.0’ från Cochrane för randomiserade kontrollstudier, ’Risk of Bias in Non-randomized Studies – of Interventions’ (ROBINS-I) för icke-randomiserade interventioner (3, 4). För observationsstudier används ‘Risk of Bias for Nutrition Observational Studies’ (RoB-NObS) skapad av US Department of Agriculture (5).
7. Evidensgradering och metaanalys
När de föregående stegen slutförts sammanställs kvaliteten på de individuella studierna. Utifrån denna information kan styrkan av evidensen fastställas för varje specifik forskningsfråga. Evidensgradering utgår från kriterierna utvecklade av ’World Cancer Research Fund’ och finns beskrivna i tabell 1 (6).
Tabell 1. Evidensgradering av studierna utifrån kriterier från ’World Cancer Research Fund’.
| Originalet på engelska | Svensk översättning |
| Convincing (high) | Övertygande (hög) |
| Probable (moderate) | Sannolik (måttlig) |
| Limited – suggestive (low) | Begränsad – tvetydig (låg) |
| Limited – no conclusion (insufficient) | Begränsad – ingen slutsats (otillräcklig) |
| Substantial effect on risk unlikely (strong) | Betydande effekt på risken osannolik (stark) |
Det är värt att notera att ’övertygande’ och ’sannolik’ anses som starka bevis.
Om det anses lämpligt för forskningsfrågan utförs även en metaanalys för att identifiera skillnader mellan studier och urskilja tendenser i resultaten. En metaanalys görs endast om det finns tillräckligt med studier inom ämnet med en liknande metodologi.
8. Rapportskrivning
Det slutgiltiga steget i processen består av att skriva ihop en rapport av litteraturöversikten, vilket sker enligt det standardiserade rapportformatet ’PRISMA’ (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) (7). Samtliga medlemmar i NNR-SR Centre granskar rapporten i sin helhet innan den skickas till den vetenskapliga tidskriften ’Food & Nutrition Research’ för granskning av andra experter inom respektive fält.
Arbetet med de systematiska litteraturöversikterna är omfattande och samtliga involverade arbetar för fullt för att slutföra projektet så snart som möjligt.
*PROSPERO är en internationell och fritt tillgänglig databas som innehåller protokoll för systematiska översikter.
Referenser
1. Arnesen EK, Christensen JJ, Andersen R, Eneroth H, Erkkola M, Høyer A, et al. The Nordic Nutrition Recommendations 2022 – structure and rationale of qualified systematic reviews. Food & nutrition research. 2020;64.
2. Arnesen EK, Christensen JJ, Andersen R, Eneroth H, Erkkola M, Høyer A, et al. The Nordic Nutrition Recommendations 2022 – handbook for qualified systematic reviews. Food & nutrition research. 2020;64.
3. Sterne JAC, Savović J, Page MJ, Elbers RG, Blencowe NS, Boutron I, et al. RoB 2: a revised tool for assessing risk of bias in randomised trials. BMJ (Clinical research ed). 2019;366:l4898.
4. Sterne JA, Hernán MA, Reeves BC, Savović J, Berkman ND, Viswanathan M, et al. ROBINS-I: a tool for assessing risk of bias in non-randomised studies of interventions. BMJ (Clinical research ed). 2016;355:i4919.
5. Nutrition Evidence Systematic Review. Risk of Bias for Nutrition Observational Studies (RoB-NObs) Tool 2019 [cited 2021 Nov 17]. Available from: https://nesr.usda.gov/sites/default/files/2019-07/RiskOfBiasForNutritionObservationalStudies-RoB-NObs.pdf.
6. World Cancer Research Fund, American Institute for Cancer Research. Continuous Update Project Report. Judging the evidence London: World Cancer Research Fund: 2018 [cited 2021 Nov 22]. Available from: https://www.wcrf.org/wp-content/uploads/2021/02/judging-the-evidence.pdf.
7. Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) [cited 2021 Nov 22]. Available from: http://www.prisma-statement.org/.
Nutritionsfakta önskar er alla en riktigt god jul och ett gott nytt 2022!
Tack alla läsare och alla forskare som skrivit på Nutritionsfakta för det gångna året. Vi hoppas ni får en fin ledighet!
Kopplingen mellan kostmönster, inflammation och sjukdomar
Forskningen visar att låggradiga och ihållande inflammationer kan skada kroppens celler och leda till hjärtkärlsjukdomar och cancer. Det är däremot inte klarlagt hur stor roll kosten spelar i utvecklingen av inflammationer. En väg framåt är att undersöka vilken betydelse som individers kostmönster har, alltså allt vad en person äter och dricker.
Dietisten Stina Bodén har i sin doktorsavhandling studerat just sambanden mellan kostmönster, inflammation och sjukdomar, som tjock- och ändtarmscancer. Hon visar bland annat att typ av kostmönster till viss del bidrar till hjärtinfarkt. Resultaten från avhandlingen visar också att det är svårt att fastställa i vilken grad kronisk låggradig inflammation bidrar till sambandet mellan kost och utvecklingen av kroniska sjukdomar. Antagligen är flera mekanismer involverade.
>>text: Stina Bodén leg dietist, med dr, Dietistmottagningen, Östersunds sjukhus, Region Jämtland Härjedalen
Inflammation och risk för sjukdom
Forskning visar att inflammation kan bidra till utvecklingen av flera kroniska sjukdomar, som metabola syndromet, diabetes, hjärtkärlsjukdom och cancer (1). Men inflammation är också immunförsvarets viktigaste mekanism och livsnödvändigt för att reparera och eliminera ämnen som är skadliga för kroppen. En akut inflammation efter en skada eller infektion ger ofta höga infektionsparametrar, men avtar i takt med att skadan eller infektionen läker. En låggradig och ihållande inflammation kan däremot skada våra celler, vävnader och organ.
Låggradig inflammation som påverkar flera organ samtidigt – systemiskt – verkar ha ett samband med våra levnadsvanor, och det är känt att vissa näringsämnen är involverade i inflammationsprocessen. Men det är dock inte klarlagt hur stor roll kosten spelar för låggradig inflammation hos människan, och vilken betydelse kostens eventuella inflammatoriska effekt kan ha för utvecklingen av bland annat hjärtkärlsjukdom och cancer.
Sambanden är också komplicerade eftersom både hjärtkärlsjukdom och cancer i sig har en inflammatorisk komponent som kan agera som både ”vän och fiende” (2). Flera inflammationsmarkörer, som fibrinogen, serum amyloid A, interleukin 6 (IL-6) och C-reaktivt protein (CRP) har visat sig förutsäga framtida hjärtkärlsjukdom (3). För cancer är inflammation en mekanism som både kan främja tumörcellen och dess tillväxt (4) – men också motverka tumörens tillväxt (2).
Kostmönster
Det finns en rad etablerade samband mellan mat och ohälsa/sjukdom. Energirik mat eller för mycket mat kan orsaka övervikt och fetma. Ett överskott av kroppsfett ger i sin tur ökad risk för en rad olika sjukdomar, däribland hjärtkärlsjukdom och flera typer av cancer, inklusive tjocktarmscancer (5). Det finns även övertygande evidens att det är bra för hälsan att äta mycket frukt, grönsaker, fisk, kostfiber och omättat fett – och mindre av mättat fett och socker. En sådan kost skulle också kunna definieras som traditionell medelhavskost, en kost som är väl studerad och brukar lyftas fram som en hälsofrämjande evidensbaserad typ av kost (6). Mekanismerna bakom dessa samband är inte klarlagda och inte heller i vilken utsträckning risken för olika sjukdomar ökar eller minskar i relation till intag av dessa livsmedelsgrupper.
För att kunna bedöma sambandet mellan kosten i sin helhet och dess inverkan på risk för sjukdom är det lämpligt att studera individers kostmönster, alltså att försöka mäta allt individen äter. Kostmönster kan också ge en bild av möjliga interaktioner mellan kostfaktorer och näringsämnen, som man riskerar att missa om man endast studerar delar av kosten eller enskilda näringsämnen.
Inom nutritionsområdet sker ett allt större fokus på kostmönster, både hur kostråd utformas och hur de kommuniceras. De senaste amerikanska nationella kostråden (Dietary Guidelines for Americans 2020-2025) understryker just vikten av ett hälsosamt kostmönster genom livet. Också våra nordiska näringsrekommendationer (NNR2012) poängterar betydelsen av kostmönster, och sannolikt kommer den kommande uppdateringen, NNR2022, att ha ett ännu större fokus på det. En orsak är att man i allt högre grad inom forskningen det senaste årtiondet studerat kostmönster i stället för enskilda näringsämnen och kan sammanställa kostmönsters effekter på hälsa. Vi äter ju inte enskilda näringsämnen, utan flera livsmedel med varierande innehåll av näringsämnen vid varje måltid, dag efter dag.
Att studera kostmönster innebär att studierna innefattar kvantiteter, proportioner och kombinationer, men också kumulativa effekter av mat och dryck. Det är viktigt att studera kosten över tid, och inte en enskild dag, för att undersöka exponering i relation till risk för olika sjukdomar. Detta utesluter inte studier av hur enskilda livsmedel eller näringsämnen påverkar kroppen, men den typen av studier kan aldrig mäta den komplexitet som hela kosten står för. En människas kostintag innefattar tusentals biologiska substanser som har såväl individuella som samverkande effekter och kan påverka processer i cellerna och hormonreglering (7).
Biomarkörer som markör för mekanismer
Biomarkörer i biologiska prover – blod, urin, avföring, saliv – är en viktig del av nutritionsforskning idag. Syftet kan vara att bättre mäta kostintaget som ett komplement till självrapporterat kostintag eftersom det är vanligt med under- och felrapportering. Syftet kan också vara att undersöka mekanismerna bakom ett samband mellan kostintag och sjukdom. Man kan till exempel mäta inflammationsmarkörer i blodprover för att studera hur inflammationsprocesser påverkas av en viss typ av kost – och för att se om inflammation är relaterad till sjukdomar som hjärtinfarkt eller cancer. Tekniker som används för att mäta biomarkörer inom nutrition är proteomik – storskalig analys av proteiner – och metabolomik – identifiering och kvantifiering av mycket små molekyler eller metaboliter som kan vara spår av ämnen eller spår av metabola processer.
Om avhandlingen
Syftet med min avhandling var att undersöka hur kronisk låggradig inflammation påverkar risken för hjärtinfarkt och cancer, framför allt tjock- och ändtarmscancer, och med särskilt fokus på olika kostmönsters inverkan (8). I de första två arbetena i avhandlingen studerade jag ett kostinflammationsindex, framtaget utifrån tidigare kunskap om sambandet mellan intag av vissa näringsämnen och inflammation i kroppen (9). I avhandlingen relaterades kostinflammationsindex både till risk för hjärtinfarkt och till risk för cancer. I studien om hjärtinfarkt användes två blodprovsmått på inflammation, CRP och IL-6. I studierna i avhandlingen undersökte jag hur väl kostinflammationsindex kunde fånga den inflammatoriska effekten av kosten.
Tjock- och ändtarmscancer
I studien om cancer ingick de vanligaste cancerformerna, och då användes även ett annat kostindex för att mäta studiedeltagarnas följsamhet med en medelhavsliknande kost (10). De två senare arbetena i avhandlingen fokuserade på risken för tjock- och ändtarmscancer. Jag undersökte nivåer av CRP, ett mått på inflammation som även kallas för ”snabbsänka ”, i blodprover och risken för olika undergrupper av tjock- och ändtarmscancer. Tidigare studier har gett olika resultat för sambandet mellan CRP och risk för tjock- och ändtarmscancer – men ingen har studerat om särskilda molekylära undergrupper har starkare samband än andra.
Faktorer relaterade till levnadsvanor, som övervikt, rökning, inaktivitet, låg konsumtion av kostfiber och hög konsumtion av rött kött och charkuterier, har visat sig vara särskilt förknippade med risken för tjock- och ändtarmscancer. Tjock- och ändtarmscancer tar många år att utveckla och därför borde det finnas goda förutsättningar för att förhindra eller skjuta upp sjukdomen med hjälp av långsiktiga livsstilsförändringar. Tumörens egenskaper, både var i tarmen den sitter och dess molekylära egenskaper, har betydelse för behandling och prognos (11). Var tumören sitter och olika egenskaper kan också vara kopplade till olika riskfaktorer, bland annat kostintag (12). Men sambanden är inte klarlagda varför vi även ville studera potentiella skillnader mellan olika typer av tumörer.
Den sista delen i avhandlingen var en studie om så kallade icke hypotesdrivna – eller data-drivna – kostmönster kunde kopplas till framtida risk för tjock- och ändtarmscancer- och om dessa kostmönster avspeglade olika metabola profiler i blodet. Detta arbete gjordes i samarbete med Rikard Landbergs forskargrupp på Chalmers tekniska högskola, specialiserad på nutritionell metabolomik.
Västerbottensprojektet och MONICA-studien
Deltagarna i avhandlingens studier kom från två stora befolkningsstudier i norra Sverige: Västerbottensprojektet och MONICA-studien. I Västerbottensprojektet bjuder man in invånare i Västerbotten det år de fyller 40, 50 och 60 år. I MONICA-studien bjuder man var femte år in slumpvalda invånare i Västerbotten och Norrbotten i åldrarna 25 till 74 år. Deltagarna lämnar blodprover som sparas för att kunna användas i forskning. Utifrån enkätsvar från deltagarna har olika kostmönster studerats hos deltagare som senare utvecklat hjärtinfarkt eller cancer – och deltagare som inte gjorde det. Enkätsvaren ger också information om andra egenskaper och livsstilsvanor. Blodproverna har också analyserats för inflammationsmarkörer och metaboliter. Enkäterna och blodproverna i Västerbottensprojektet och MONICA-studien samlades in flera år innan sjukdomsdiagnosen.
Kostindex, inflammation och hjärtinfarkt
Den första studien visade att risken för en framtida hjärtinfarkt var högre hos män som rapporterade en kost som enligt hypotesen kan ge inflammation. De jämfördes med de män som rapporterat en kost som enligt hypotesen kan ge lägre inflammation (13). Totalt ingick 29 parametrar i beräkningen av kostindexet (av totalt 45 i originalindex) och bland de anti-inflammatoriska parametrarna ingick till exempel omättade fetter och kostfiber. Detta samband fanns inte alls hos kvinnorna i studien. Vi fann också ett svagt men statistiskt signifikant samband mellan de två inflammationsmarkörerna CRP och IL-6 och det kostinflammatoriska indexet som vi använde för att mäta kostintaget hos en subgrupp av deltagarna. Resultatet kan tolkas som att kostens inverkan på risken för hjärtinfarkt kan ha en inflammatorisk komponent. Men det kan likväl också vara andra mekanismer inblandande.
Kostmönster och cancer
I studien om cancer med över 100 000 deltagare fann vi svaga samband mellan en typ av kost och minskad risk för cancer, särskilt för cancer som utvecklats i lunga och magsäck hos männen i studien (14). Det handlade dels om en kost som enligt hypotesen kan ge lägre inflammation, alltså kostinflammationsindex, och dels ett kostindex som mäter följsamheten till en medelhavsliknande kost. De både indexen har den del likheter då några av de mest välstuderade kostkomponenterna med etablerade hälsoeffekter ingår. De båda indexen kan potentiellt mäta samma effekter och utfall men de beräknas på helt olika sätt. Vi studerade också om förändringar i kostmönster över en tioårsperiod var relaterat till cancerrisk, till exempel om man tio år efter den första mätningen rapporterat en mer hälsosam kost – eller tvärtom. Vi fann inga signifikanta associationer till cancerrisk, oavsett om man förändrat sitt kostintag eller inte. Av det totala antalet deltagare som också rapporterat sitt kostintag en andra gång, cirka 10 år senare, var det endast en mindre andel som faktiskt förändrat kostintaget i någon större utsträckning. För många är matvanor något som faktiskt är svårt att ändra på, och något man kanske inte heller vill förändra av olika anledningar.
Inflammation och cancer
I studien om undergrupper av tjock- och ändtarmscancer kunde de olika egenskaperna hos dessa undergrupper inte förklara tidigare varierande resultat för sambandet till inflammationsmarkören CRP (15). Hos individer med mer långt gången sjukdom fanns högre nivåer av CRP i blodprover tagna närmare tidpunkten för diagnos associerade till ökad risk av tjock- och ändtarmscancer. Det berodde mest troligt på att tumören redan hade börjat växa eller att det fanns begynnande cancerceller då blodprovet togs och som i sig gav ökad inflammation. I denna studie ingick ingen analys av kostintaget hos deltagarna.
Datadrivna statistiska metoder för att studera kostmönster
En studie i avhandlingen gjorde jag i nära samarbete med docent Carl Brunius, Chalmers tekniska högskola. Vi tog fram kostmönster med hjälp av datadrivna statistiska metoder, baserat helt på hur studiedeltagarna hade rapporterat sina matvanor (studien är ej publicerad ännu). Ett sådant datadrivet kostmönster, med typisk frukostmat som filmjölk, yoghurt, fiberrika flingor och bär var associerat med en lägre risk för cancer i vänster sida av tjocktarmen, särskilt hos kvinnorna i studien.
Fiber, fullkorn, frukt, grönsaker och alkohol var associerade till metabolitprofiler i blodet. Efter att tagit hänsyn till andra faktorer, som rökning och vikt, där dessa metaboliter potentiellt kan vara inblandade, var vår förhoppning att försöka identifiera 36 specifika metaboliter som ingick i dessa metabolitprofiler. Syftet var att förhoppningsvis få ledtrådar till mekanismerna mellan kostfaktorerna och uppkomsten av cancer i tjock- och ändtarmen. Försöken att identifiera metaboliterna, alltså att förstå från vilka ämnen eller metabola processer de härstammar från, har dock inte gett några nya svar på dessa samband. Två metaboliter som var relaterade till både kostfiber och fullkorn, var kopplade till minskad risk för tjock- och ändtarmscancer.
Ytterligare en analys av de 36 metaboliterna gav en korrelation mellan komponenter i metaboliterna och risk för cancer. Det visade sig att kostfiber och fullkorn var dominerande i en av komponenterna, vilket också associerade till minskad risk för tjock- och ändtarmscancer.
Vår tolkning av resultaten är därmed att de bekräftar tidigare kunskap om positiva effekter av kostfiber och fullkorn på hälsan. Det gäller inte minst effekten via magtarmkanalen, och möjligen också att hälsosamma frukostvanor kan förebygga cancer i tjocktarmen. Vi såg också skillnader mellan kvinnor och män när grupperna analyserades separat, liksom i de två första studierna.
Sammantaget visade avhandlingen att kostmönster i viss mån kan bidra till utvecklingen av hjärtinfarkt och vissa typer av cancer. Ett kostmönster särskilt utvecklat för att fånga den inflammatoriska effekten av kost där totalt 29 parametrar ingick i beräkningen av kostindexet visade liknande svaga samband till cancer som ett kostmönster baserat på traditionell medelhavskost där totalt 8 kostparametrar ingick.
Datadrivna metoder för att studera kostmönster, liksom analyser av metaboliter från biologiska prover, kan i framtiden vara av betydelse för att bättre förstå det komplexa förhållandet mellan kost och sjukdomar. Det är också intressant att vidare studera möjliga skillnader mellan kvinnors och mäns kostvanor i relation till kroniska sjukdomar – och de bakomliggande orsakerna till dessa eventuella skillnader. Det är svårt att fastställa i vilken grad kronisk låggradig inflammation bidrar till sambandet mellan kost och utvecklingen av kroniska sjukdomar. Antagligen är flera mekanismer involverade.
Det främsta målet för att förbättra folkhälsan och förebygga kroniska sjukdomar bör fortsatt vara att främja en hälsosam och hållbar livsstil. Detta baserat på den kunskap vi har idag om kosten, oavsett bakomliggande mekanismer.
Författaren uppger inga jävsförhållanden.
Referenser
1. Furman D, Campisi J, Verdin E, Carrera-Bastos P, Targ S, Franceschi C, et al. Chronic inflammation in the etiology of disease across the life span. Nat Med. 2019;25(12):1822-32.
2. Colotta F, Allavena P, Sica A, Garlanda C, Mantovani A. Cancer-related inflammation, the seventh hallmark of cancer: links to genetic instability. Carcinogenesis. 2009;30(7):1073-81.
3. Andersson J. Inflammation and lifestyle in cardiovascular medicine (Avhandling). Umeå universitet, 2010. Hämtad från: http://urn.kb.se/resolve?urn=urn:nbn:se:umu:diva-36221
4. Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell. 2011;144(5):646-74.
5. Lauby-Secretan B, Scoccianti C, Loomis D, Grosse Y, Bianchini F, Straif K, et al. Body Fatness and Cancer–Viewpoint of the IARC Working Group. N Engl J Med. 2016;375(8):794-8.
6. Trichopoulou A, Costacou T, Bamia C, Trichopoulos D. Adherence to a Mediterranean diet and survival in a Greek population. N Engl J Med. 2003;348(26):2599-608.
7. Scalbert A, Brennan L, Manach C, Andres-Lacueva C, Dragsted LO, Draper J, et al. The food metabolome: a window over dietary exposure. Am J Clin Nutr. 2014;99(6):1286-308.
8. Bodén S. Inflammation and risk of chronic diseases with a focus on colorectal cancer and the impact of dietary patterns [Avhandling], Umeå universitet, 2020. Hämtad från: http://urn.kb.se/resolve?urn=urn:nbn:se:umu:diva-176737
9. Shivappa N, Steck SE, Hurley TG, Hussey JR, Hebert JR. Designing and developing a literature-derived, population-based dietary inflammatory index. Public Health Nutr. 2014;17(8):1689-96.
10. Tognon G, Nilsson LM, Lissner L, Johansson I, Hallmans G, Lindahl B, et al. The Mediterranean diet score and mortality are inversely associated in adults living in the subarctic region. J Nutr. 2012;142(8):1547-53.
11. Ogino S, Chan AT, Fuchs CS, Giovannucci E. Molecular pathological epidemiology of colorectal neoplasia: an emerging transdisciplinary and interdisciplinary field. Gut. 2011;60(3):397-411.
12. Mehta RS, Song M, Nishihara R, Drew DA, Wu K, Qian ZR, et al. Dietary Patterns and Risk of Colorectal Cancer: Analysis by Tumor Location and Molecular Subtypes. Gastroenterology. 2017;152(8):1944-53.e1.
13. Boden S, Wennberg M, Van Guelpen B, Johansson I, Lindahl B, Andersson J, et al. Dietary inflammatory index and risk of first myocardial infarction; a prospective population-based study. Nutr J. 2017;16(1):21.
14. Boden, S., Myte, R., Wennberg, M., Harlid, S., Johansson, I., Shivappa, N., Hebert, J. R., Van Guelpen, B., & Nilsson, L. M. The inflammatory potential of diet in determining cancer risk; A prospective investigation of two dietary pattern scores. PloS One. 2019;14(4), e0214551. https://doi.org/10.1371/journal.pone.0214551
15. Bodén S, Myte R, Harbs J, Sundkvist A, Zingmark C, Löfgren Burström A, et al. C-reactive Protein and Future Risk of Clinical and Molecular Subtypes of Colorectal Cancer. Cancer Epidemiol Biomarkers Prev. 2020;29(7):1482-91.
Tydliga samband mellan intag av sockersötade drycker och ökad risk för kardiometabola sjukdomar
Sambanden mellan intag av sockersötad dryck och ökad risk för kardiometabola sjukdomar till exempel hjärtkärlsjukdomar och typ 2-diabetes är relativt tydliga. Däremot är sambanden för det totala intaget av tillsatt socker inte alls lika tydliga. Det visar en ny avhandling i nutritionsepidemiologi från Lunds universitet.
Resultaten i avhandlingen är i linje med en ny rapport från Europeiska myndigheten för livsmedelssäkerhet, Efsa, som sammanfattar hela kunskapsläget om tillsatt socker. I Efsas sammanställning av epidemiologiska studier fanns inget stöd för att tillsatt socker ökar risken för olika kardiometabola sjukdomar. Däremot fanns ett relativt starkt stöd för att sockersötade drycker ökar risken.
Sammanställningen av randomiserade kontrollerade studier ger en lite annan bild enligt Efsas rapport. Sammantaget visar dessa studier att det finns ett positivt linjärt samband mellan intag av tillsatt socker och flera olika markörer och surrogatmått för kardiometabola sjukdomar.
För framtida epidemiologisk forskning på sockerintag skulle mätningar av sackaros och fruktos i urinen kunna ge en mer korrekt bild av sockerintaget. Dessa markörer behöver dock studeras ytterligare för att säkerställa att de verkligen motsvarar det faktiska sockerintaget.
>>text: Stina Ramne, PhD Nutritionsepidemiologi, Institutionen för kliniska vetenskaper, Lunds universitet, Malmö
Introduktion
Frågan om socker har betydelse för risken att utveckla fetma, typ 2-diabetes och hjärtkärlsjukdom har diskuterats och undersökts flitigt de senaste årtiondena. Kopplingen att socker ökar risken för dessa kardiometabola sjukdomar fastslås ofta som en sanning i media idag. Fast om man tittar närmare på de vetenskapliga studier som har publicerats, så inser man att så enkelt är det inte. Visserligen visar djurstudier att socker skulle kunna öka risken för kardiometabola sjukdomar, men i studier på människor är det svårt att konstatera ett samband mellan konsumtion av socker och ökad risk för typ 2-diabetes och hjärtkärlsjukdomar.
Definitioner av socker och skillnaden mellan olika typer av studier
Vi börjar med några viktiga begrepp och definitioner. Först om ”sockerintag”. I den största delen av den vetenskapliga litteraturen används följande tre definitioner:
Totalt socker innefattar den totala mängden av glukos, fruktos, galaktos, sackaros, maltos och laktos, oavsett livsmedel.
Tillsatt socker innefattar endast de sockerarter som är tillsatt till livsmedel, antigen vid produktionen, tillredningen eller vid bordet – till exempel när man använder socker i kaffet eller på gröten.
Fritt socker innefattar precis som tillsatt socker de sockerarter som är tillsatta, men de sockerarter som är naturligt förekommande i fruktjuicer ingår också: fritt socker = tillsatt socker + naturligt socker i fruktjuice.
En andra viktig definition är skillnaden mellan olika typer av vetenskapliga studier.
Epidemiologiska studier går främst ut på att studera sambanden mellan nivå på exponering, till exempel intagsnivå av tillsatt socker, och risk för sjukdomar, baserat på observationer av individer inom en kohort. En kohort definieras som en grupp individer som har en eller flera gemensamma egenskaper och som följs under en viss tid, vanligtvis flera år. Helst bör dessa studier genomföras prospektivt, det vill säga att exponeringsnivån mäts före insjuknandet, för att undvika att exponeringsnivån uppskattas i efterhand.
Interventionsstudier, helst randomiserade gör till skillnad från epidemiologiska studier en förändring i studiedeltagarnas exponeringsnivå. Försöksdeltagarna kan till exempel lottas till att antingen dricka 500 ml läsk eller 500 ml vatten per dag under en viss tidsperiod. Förändring i sjukdomsrisk under interventionsperioden jämförs sedan mellan grupperna.
Ny avhandling från Lunds universitet
Avhandlingen Sugar consumption and cardiometabolic risk – with a focus on the urinary sucrose and fructose biomarkers (1) försvarades den 10 september 2021. Den första artikeln undersöker sambandet mellan intag av tillsatt socker från olika källor, med uppgifter om dödlighet i Malmö Kost Cancer-kohorten och Västerbottenkohorten, som var och en innefattar nästan 25 000 deltagare.
I båda dessa prospektiva kohortstudier fann vi ett positivt samband mellan intag av sockersötade drycker och förtida död. För det totala intaget av tillsatt socker däremot, så fann vi inget linjärt samband. Dock visade vi att den lägsta risken i förhållande till intag av tillsatt socker inte sågs vid lägst intag, utan något högre, ungefär mellan 7,5 och 10 energiprocent från tillsatt socker. I jämförelse med denna intagsnivå var ett intag på över 20 energiprocent av tillsatt socker associerat med ungefär 30 procent ökad risk för dödlighet i båda kohorterna, och ett lägre intag, på under 5 energiprocent av tillsatt socker, var associerat med 23 procent ökad dödlighet i Malmö Kost Cancer-kohorten och 9 procent ökad dödlighet (ej statistiskt signifikant) i Västerbottenkohorten. Dessa resultat indikerar vad som brukar kallas för ett U-format samband.
Utöver detta fann vi, i båda kohorterna, att sambanden för det sammanlagda intaget av bakverk, desserter, glass, godis och choklad endast visade en ökad risk för dödlighet bland dem som åt allra minst. Dessa resultat med ökad risk vid lågt intag är väldigt svåra att förklara mekanistiskt och kan rimligtvis ha uppstått av olika metodologiska brister, snarare än att spegla ett sant orsakssamband (2).
En annan artikel i avhandlingen studerade sambandet mellan intag av tillsatt socker och sockersötad dryck, och 136 sjukdomsrelaterade proteiner som finns i blodet, hos deltagarna i Malmö Kost Cancer-kohorten. Vi fann att av de sju cirkulerande proteiner som var associerade med intag av sockersötade drycker, så var sex även associerade med typ 2-diabetesrisk. Däremot så var endast två av de nio plasmaproteiner som vi fann var associerarede med det totala intaget av tillsatt socker, även associerade med typ 2-diabetes. Dessa samband var dessutom mycket svagare än för de proteiner som var associerade med intag av sockersötad dryck. Detta kan tolkas som att intag av sockersötad dryck – men inte det totala intaget av tillsatt socker – var associerat med en proteinprofil som är relaterad till en ökad risk för typ 2-diabetes (3).
Vi undersökte också sambandet mellan intag av både tillsatt socker och sockersötad dryck med 64 olika tarmbakterier, samt olika mått för tarmflorasammansättning i Malmö Offspring Study. Vi fann inga samband mellan intag av tillsatt socker och tarmbakterier som var statistiskt signifikanta. Däremot fann vi samband mellan intag av sockersötad dryck och lägre bakterierikedom av släktet (genus) Lachnobacterium, och högre kvot mellan bakteriestammarna (phyla) Firmicutes och Bacteroidetes.
Lachnobacterium är en bakterie som har studerats väldigt sparsamt, så vad det sambandet säger oss vet vi inte ännu. Dock har en högre kvot mellan bakteriestammarna Firmicutes och Bacteroidetes ofta sammankopplats med fetma och högre kardiometabol risk i tidigare studier. Man kan alltså tolka dessa resultat som att intag av sockersötad dryck var sammankopplat med en fetmarelaterad tarmflorasammansättning. Den kopplingen syntes inte för totala intaget av tillsatt socker (4).
Dessa tre studier visade sammanfattningsvis att intag av sockersötade drycker konsekvent var associerat med högre kardiometabol risk i form av ökad dödlighet, en typ 2-diabetesrelaterad proteinprofil och en fetmarelaterad tarmflorasammanstätning. Denna koppling kunde inte visas för det totala intaget av tillsatt socker. Dessa skillnader mellan intag av sockersötade drycker jämfört med det totala intaget av tillsatt socker är i linje med resultat från tidigare epidemiologiska studier.
Efsa summerar kunskapsläget
Efsa har nyligen i en litteraturgenomgång sammanfattat kunskapsläget om socker och hälsoutfall på uppdrag av de fem nordiska länderna. Utkastet till rapporten för denna genomgång publicerades sommaren 2021 och har varit ute för konsultation där aktörer kunde skicka in kommentarer. Den reviderade rapporten kommer att publiceras i februari 2022. Huvudsyftet med Efsas rapport är att försöka sätta en så kallad Tolerable Upper Limit, vilket definieras som den maximala nivån av långvarigt dagligt intag som bedöms att inte utgöra en risk för negativa hälsoeffekter. Det handlar alltså inte om en rekommenderad intagsnivå.
I Efsas utkast till rapporten summeras både prospektiva kohortstudier och randomiserade kontrollerade studier som har studerat intag av socker i relation till flertalet sjukdomar och riskmarkörer. Från det epidemiologiska kunskapsläget, det vill säga prospektiva kohortstudier, fann man inget stöd för att tillsatt eller fritt socker ökar risken för olika kardiometabola sjukdomar. Däremot fanns ett relativt starkt stöd för att intag av sockersötade drycker ökar risken för fetma, typ 2-diabetes, blodfettsrubbningar, högt blodtryck, hjärtkärlsjukdom och gikt.
Efsas sammanfattning av randomiserade kontrollerade studier visar däremot att det finns ett positivt linjärt samband mellan intag av tillsatt socker och vissa riskmarkörer och surrogatmått för kardiometabola sjukdomar.
Detta skulle kunna ha sin förklaring i att randomiserade kontrollerade studier generellt väger tyngre än prospektiva kohortstudier i evidensordningen. Men ett bristande stöd från epidemiologiska studier tyder ändå på att underlaget för slutsatsen inte är helt tillfredställande robust.
Det finns dock rimliga metodologiska brister som kan förklara varför specifikt epidemiologiska studier skulle kunna ha svårt för att visa ett eventuellt samband mellan sockerintag och ökad kardiometabol risk. Det handlar främst om att nästintill alla epidemiologiska studier är baserade på självrapporterade mätningar av kostintag. Vi vet att sådana mätningar är kraftigt begränsade, framförallt på grund av underrapportering. Vi vet att underrapportering ofta är som störst för livsmedel som anses ohälsosamma och som konsumeras utanför ramarna av dagens tre huvudmål, som till exempel sockerrika snacks och drycker. Dessutom är underrapportering ofta större bland individer som har övervikt och fetma. Detta medför att om individer med högre kardiometabol risk systematiskt rapporterar lägre sockerintag, så kan detta förvränga sambanden som observeras. De subjektiva mätningarna av sockerintaget kan vara en bidragande faktor till skillnaden i resultat mellan epidemiologiska och randomiserade kontrollerade studier.
Att mäta sockerintag objektivt
Efsa avslutar sin rapport med att ge rekommendationer för framtida forskning för att fylla de kunskapsluckor som identifierats som följd av litteraturgenomgången. Viktigast enligt Efsa är: ”To develop and validate reliable methods and (bio)markers of intake of dietary sugars”.
Detta konstaterande för oss tillbaka till avhandlingen Sugar consumption and cardiometabolic risk – with a focus on the urinary sucrose and fructose biomarkers. Ett av syftena med avhandlingen var att utvärdera mätningar av sackaros och fruktos i urinen som objektiva mått, så kallade biomarkörer, för sockerintag, för att på så sätt komma ifrån bristerna med självrapporterade subjektiva mätningar av sockerintag.
Mätning av sackaros och fruktos i urinen i 24-timmars urinprov har sedan 2005 varit en validerad metod för att objektivt mäta sockerintag (6). Men det är fortfarande mycket vi inte vet om denna kostbiomarkör.
En av studierna i avhandlingen har indikerat att denna markör kan vara användbar även i formen av natturinprov (7) som såklart är enklare att samla in än 24-timmars urinprov, vilket skulle kunna underlätta framtida forskning. Däremot så indikerar en annan studie i avhandlingen att markören eventuellt inte motsvarar det sanna sockerintaget tillräckligt bra hos individer med prediabetes, det vill säga nedsatt metabol kontroll och ökad risk för typ 2-diabetes (8). Dessa fynd behöver dock verifieras i kontrollerade studier eftersom undersökningarna i denna avhandling endast har kunnat jämföra sackaros- och fruktosutsöndringen med självrapporterat sockerintag – och inte det sanna sockerintaget.
Denna kostbiomarkör har stor potential att stärka framförallt den epidemiologiska forskningen om sockerintag i framtiden – om vi bara lär oss förstå dess verkningsmekanismer och begränsningar till fullo.
Folkhälsostrategiska aspekter
Men – spelar det någon roll ifall vi har tillräcklig evidens för de potentiella effekterna av tillsatt sockerintag på hälsan? Även om vi inte har tillräckligt med evidens kan vi ju ge den allmänna rekommendationen att minska intaget av tillsatt socker, eftersom det inte finns några kända fördelar med att konsumera tillsatt socker. Svaret på frågan är – jo, det behövs trots det stadig evidens för att vi ska kunna ge rätt näringsrekommendationer, göra korrekta folkhälsostrategier och hantera eventuell lobbying från industrin.
Den heta frågan om socker- eller läskskatt i Sverige bör grundas på vetenskaplig evidens. Det är i nuläget svårt att utifrån vetenskapligt underlag motivera en skatt på allt socker. Däremot är en skatt på specifikt sockersötade drycker välmotiverad utifrån vetenskapliga studier. Hur denna skatt ska formuleras i detalj kräver dock ytterligare stöd från vetenskapen. Ska skatten riktas till konsumenter för att uppnå sänkt läskkonsumtion? Hur hög ska i så fall skatten vara för att verkligen påverka konsumtionsvanorna? Eller ska skatten riktas mot industrin för att uppnå sänkt sockerinnehåll i läsken? Hur hanterar vi i så fall substitution mot artificiella sötningsmedel i all läsk?
Det är många frågor som behöver besvaras. Underlaget är idag knaggligt och det kan vara riskabelt att dra förhastade slutsatser. Ett varnande exempel är den tidigare inriktningen på att sänka fetthalten i många livsmedel, som å ena sidan baserades på viss vetenskaplig grund, men som man trots allt nu har börjat gå ifrån. Det vore synd om vi på samma sätt gjorde liknande förhastade åtgärder med sockret som vi tidigare gjort med fettet.
Frågan om mängden socker i vår kost har betydelse för risken att utveckla fetma, typ 2-diabetes och hjärtkärlsjukdom är långt ifrån färdigbesvarad och i behov av mycket ytterligare forskning.
Slutsats
Epidemiologiska studier visar att intaget av sockersötad dryck är tydligt förknippat med en ökad kardiometabol risk. Motsvarande samband syns däremot inte för det totala intaget av tillsatt socker. Men mycket tyder ändå på att en allmän minskning av intaget av tillsatt socker bör uppmuntras, eftersom dessa epidemiologiska studier generellt lider av vissa metodologiska begränsningar och att resultat från randomiserade kontrollerade studier tenderar att stödja ett samband mellan intag av tillsatt socker och kardiometabola sjukdomar, om än ganska begränsat. Dessutom finns det inga kända fördelar med att konsumera tillsatt socker.
För arbetet med folkhälsostrategier finns ett starkt vetenskapligt underlag för att hantera konsumtionsvanorna av sockersötad dryck. För det totala intaget av socker är kunskapsunderlaget relativt otydligt och heterogent. Det är nödvändigt med ytterligare forskning för att hitta svar på frågan om hur socker påverkar vår hälsa. Det som kan uppfattas som självklart, kan i verkligheten vara långt ifrån självklart.
Författaren uppger inga jävsförhållanden.
Referenser
1. Ramne S. Avhandling: Sugar consumption and cardiometaoblic risk – With a focus on the urinary sucrose and fructose biomarkers. Lunds universitet, 2021.
2. Ramne S, Alves Dias J, González-Padilla E, Olsson K, Lindahl B, Engström G, Ericson U, Johansson I, Sonestedt E. Association between added sugar intake and mortality is nonlinear and dependent on sugar source in 2 Swedish population-based prospective cohorts. The American Journal of Clinical Nutrition 2019;109(2):411-23. doi: 10.1093/ajcn/nqy268.
3. Ramne S, Drake I, Ericson U, Nilsson J, Orho-Melander M, Engström G, Sonestedt E. Identification of Inflammatory and Disease-Associated Plasma Proteins that Associate with Intake of Added Sugar and Sugar-Sweetened Beverages and Their Role in Type 2 Diabetes Risk. Nutrients 2020;12(10). doi: 10.3390/nu12103129.
4. Ramne S, Brunkwall L, Ericson U, Gray N, Kuhnle GGC, Nilsson PM, Orho-Melander M, Sonestedt E. Gut microbiota composition in relation to intake of added sugar, sugar-sweetened beverages and artificially sweetened beverages in the Malmö Offspring Study. European Journal of Nutrition 2020. doi: 10.1007/s00394-020-02392-0.
5. EFSA Panel on Nutrition Novel Foods and Food Allergens DT, Jacqueline Castenmiller, Stefaan de Henauw, Karen Ildico Hirsch-Ernst, Torsten Bohn, Helle Katrine Knutsen, Alexander Maciuk, Inge Mangelsdorf, Harry J McArdle, Androniki Naska, Carmen Peláez, Kristina Pentieva, Alfonso Siani, Frank Thies, Sophia Tsabouri, Roger Antonius Henricus Adan, Pauline Emmett, Carlo Galli, Mathilde Kersting, Paula Moynihan, Luc Tappy, Laura Ciccolallo, Agnès de Sesmaisons-Lecarré, Lucia Fabiani, Zsuzsanna Horvath, Laura Martino, Irene Muñoz Guajardo, Silvia Valtueña Martínez and Marco Vinceti. Scientific opinion on the Tolerable Upper Intake Level for dietary sugars. 2021.
6. Tasevska N, Runswick SA, McTaggart A, Bingham SA. Urinary sucrose and fructose as biomarkers for sugar consumption. Cancer epidemiology, biomarkers & prevention : a publication of the American Association for Cancer Research, cosponsored by the American Society of Preventive Oncology 2005;14(5):1287-94. doi: 10.1158/1055-9965.Epi-04-0827.
7. Ramne S, Gray N, Hellstrand S, Brunkwall L, Enhörning S, Nilsson PM, Engström G, Orho-Melander M, Ericson U, Kuhnle GGC, Sonestedt E. Comparing Self-Reported Sugar Intake With the Sucrose and Fructose Biomarker From Overnight Urine Samples in Relation to Cardiometabolic Risk Factors. Frontiers in Nutrition 2020;7. doi: 10.3389/fnut.2020.00062.
8. Ramne S, Sonestedt E, Brand-Miller J, Fogelholm M, Larsen TM, Raben A, Dragsted LO. 24-hour urinary sucrose and fructose excretion as biomarkers of sugar intake in individuals with prediabetes – a PREVIEW substudy. Unpublished manuscript 2021.
Podd om proteinskiftet
Matskiftet är en populärvetenskaplig podcast som handlar om olika aspekter av proteinskiftet och hållbar kost. Med hållbar kost menas en mer hållbar kost än vad genomsnittssvensken äter idag och det kan uppnås genom att äta mer växtbaserat. Podden leds av doktorand Inger-Cecilia Mayer Labba från Chalmers Livsmedelsvetenskap och i de olika avsnitten deltar professor Ann-Sofie Sandberg och professor Ingrid Undeland båda från Chalmers Livsmedelsvetenskap, doktorand Mari Wollmar från Kostvetenskap, Göteborgs universitet, och docent och husdjursagronom Anna Hessle från SLU, Sveriges lantbruksuniversitet.
I de fyra avsnitten diskuteras utmaningar med den växtbaserade kosten, växtbaserat i offentliga måltider, naturbete och nötköttsproduktion i Sverige, och om hur fisk kan vara en del av en hållbar kost.
Näringslära för högskolan – sjunde utgåvan
Bokrecension
Redaktörer: Christina Berg, Lars Ellegård, Christel Larsson
Förlag: Liber
Näringslära för högskolan är ett svenskt standardverk som genom åren regelbundet har uppdaterats. Mycket innehållsrik, lätt att hitta i och leder vidare till fördjupningar, anser Cecilia Nälsén om den nyutkomna sjunde utgåvan.
Näringslära för högskolan utkom första gången för 40 år sedan och har sedan dess uppdaterats regelbundet. Boken kan användas både som uppslagsbok för yrkesverksamma inom mat och hälsa och används också som kurslitteratur på flera utbildningar inom nutritionsområdet.
Nytt för denna utgåva är att boken har delats in i sju avsnitt och varje avsnitt är sedan uppdelat i flera kapitel. Följande avsnitt ingår: Kostrelaterade sjukdomar, Från mat till metabolism, Rekommendationer och regler, Energi och näringsämnen, Övriga bioaktiva ämnen, livsmedel och kostmönster, Nutrition under livscykeln, Metodik inom kost och nutrition.
Denna utgåva innehåller också fler kapitel än den förra utgåvan. En del kapitel har delats upp, men nya kapitel har också tillkommit, till exempel Nutritionstoxikologi, Metabolomik (analys av olika metaboliter som kan visa på kostmönster), och Kost och genetik. En utförlig och detaljerad innehållsförteckning baserad på avsnitten och kapitlen gör det lätt att hitta. Avsnitten har olika färger vilket ytterligare tydliggör bokens indelningar. Referenser har lagts in som löpande text vilket underlättar för läsare som önskar fördjupning.
Mycket litteratur är på engelska inom nutritionsområdet och baseras inte på svenska förhållanden. Näringslära för högskolan utgår både från det internationella kunskapsläget och svenska förhållanden och perspektiv där man tar hänsyn till exempelvis våra matvanor, rekommendationer och lagar. Författarlistan är omfattande, totalt är det 26 författare med stor vetenskaplig kompetens och erfarenhet inom sitt område som bidrar till Näringslära för högskolan.
Som verksam inom nutritionsområdet tycker jag att boksläppet av en ny utgåva av Näringslära för högskolan är en stor händelse. Även denna gång får jag möjlighet att ta del av ett gediget innehåll, skrivet av författare med stor kunskap och erfarenhet inom området.
Många invandrare byter goda matvanor mot sämre i Sverige – dietisten har en roll att lotsa fram till det bästa av två kulturer
FN:s migrationsorgan IOM bedömer att migranters hälsa och livsstil är en del av migrationsprocessen som bör uppmärksammas av internationella beslutsfattare och experter. Detta för att kunna hantera de stora migrationsströmmarna som förväntas i framtiden.
Den forskning som finns visar att invandrare till Sverige, särskilt de som är födda utanför Europa, har en tendens att ändra sina matvanor i det nya landet. Förändringen leder ofta till mer energirik kost, lägre intag av fibrer, mindre med essentiella fettsyror och viktiga mikronutrienter. De nya matvanorna, där man bytt bort en mer hälsosam kost, leder till en ökad risk för diabetes, övervikt och fetma samt kardiovaskulära sjukdomar. Det bästa vore att kombinera de mest hälsosamma delarna i den gamla och den nya matkulturen. I den processen har hälsoprofessionerna, och i synnerhet de legitimerade dietisterna, en avgörande roll för att vägleda invandrare till att sätta upp rimliga mål för kost och fysisk aktivitet.
Det finns få svenska studier på matvanor hos invandrare och de flesta är dessutom minst 20 år gamla. Därför behövs mer forskning för att ge en mer fullständig bild av hur matvanorna ändras, skriver Afsaneh Koochek.
>>text: Afsaneh Koochek, legitimerad dietist, docent, Institutionen för kostvetenskap, Uppsala universitet, Uppsala
Det finns ingen allmänt vedertagen definition av migration eller invandrare/migranter och begreppet definieras olika i olika delar av världen. I denna artikel utgår begreppen migration och migranter från definitionen från FN-organet International Organization for Migration (IOM) (1). Den ger en bred och allmän beskrivning av en migrant som en individ som flyttar eller har flyttat från sin vanliga bostadsort och över en internationell gräns, oavsett orsakerna till flytten. Denna definition inkluderar flyktingar såväl som migranter som flyttar för att få ett bättre liv genom arbete, utbildning eller på grund av familjeband.
Den globala migrationsrörelsen som startades för minst tre hundra år sedan har nästan aldrig avstannat helt. Migrationen fortsatte även när allt annat inklusive världsekonomi stoppades på grund av covid-19-pandemin. Även om majoriteten av den globala migrationen sker inom låg- och medelinkomstländer, fokuserar den mest framträdande dialogen nästan uteslutande på migration från låg- och medelinkomstländer till höginkomstländer. IOM uppskattade antalet internationella migranter i världen till omkring 281 miljoner år 2020, vilket motsvarar 3,6 procent av jordens befolkning (1).
Historien av migrationen till Sverige började på 1200-talet när tyska immigranter bosatte sig i Visby och Stockholm (2). Mellan 1850 och 1930 blev Sverige däremot ett utvandrarland på grund av svält och cirka 1,3 miljoner av den svenska befolkningen utvandrade, främst till Amerika. En av de största migrationsvågorna till dagens Sverige började under andra världskriget.
Enligt Migration Information Source (2, 3), är Sveriges migrationsrörelser i modern tid indelade i följande fem perioder, som var och en karakteriseras av olika typer av migranter:
1. Flyktingar från Sveriges grannländer (1938–1948).
2. Arbetskraftsinvandrare från Finland och sydeuropeiska länder (1949–1971).
3. Familjeåterförening och flyktingar från utvecklingsländer (1972–1989).
4. Asylsökande från Balkanländer och den fria rörligheten för EU-medborgare i Europeiska unionen (från 1990).
5. Sverige tog i en global jämförelse emot flest asylsökande per capita 2015 (3). De flesta kom från Syrien, Afghanistan och Irak. Näst största grupperna var iranier, somalier och eritreaner.
År 2020 uppgick antalet första generationens immigranter i Sverige till strax över 2 miljoner, vilket motsvarar omkring 20 procent av Sveriges befolkning (4). Tabell 1 visar de tio vanligaste födelseländerna bland migranter i Sverige år 2020.
Tabell 1. De tio största grupperna av immigranter i Sverige efter födelseland år 2020.
| Födelseland | Kvinnor | Män | Totalt |
| Syrien | 85 325 | 108 269 | 193 594 |
| Irak | 67 680 | 78 760 | 146 440 |
| Finland | 85 421 | 54 916 | 140 337 |
| Polen | 49 333 | 44 429 | 93 762 |
| Iran | 38 437 | 42 864 | 81 301 |
| Somalia | 35 490 | 34 694 | 70 184 |
| Före detta Jugoslavien | 31 722 | 31 697 | 63 419 |
| Afghanistan | 21 024 | 39 834 | 60 858 |
| Bosnien och Hercegovina | 30 352 | 29 809 | 60 161 |
| Turkiet | 23 639 | 28 989 | 52 628 |
Källa: Befolkningsstatistik (5).
Migration och nutritionsrelaterad hälsa i ett internationellt perspektiv
Vid ankomsten till ett nytt land, har invandare oftast färre kroniska sjukdomar och är friskare jämfört med befolkningen i det nya landet de flyttar till. Detta samband är känt som ”the healthy migrant effect” (HME) (6) och har rapporterats i flera studier bland immigranter i USA (7, 8), Kanada (9, 10), och i mindre omfattning i Europa (11) och Australien (12).
Hypotesen bakom HME är att migranter är en selekterad grupp: de har mer motivation och resurser i form av bättre ekonomi och bättre fysisk och psykisk hälsa än de som stannar i sina ursprungsländer. Med andra ord, dålig hälsa är ett hinder för utvandring (6). Immigranter tenderar dock att uppleva en snabb försämring av sitt allmänna hälsotillstånd efter några år i det nya landet på grund av framför allt livsstilsförändringar, som innefattar fysisk aktivitet och matvanor (13-16).
Å andra sidan kan dålig hälsa vara en anledning till migration bland äldre eftersom äldre personer med dålig hälsa vill flytta till ett nytt land för att komma närmare sina barn och andra anhöriga som i sin tur kan vårda sina äldre och sjuka föräldrar (17, 18).
Forskning i Sverige som har studerat HME ur ett svenskt perspektiv, har emellertid visat att hälsoutfallen efter migration kan variera beroende på vilket land migranterna kommer ifrån – och vilka hälsovariabler som har studerats. HME stämmer inte heller alltid på migranter från västvärlden som för det mesta emigrerar frivilligt från sina länder, jämfört med ofrivilliga emigranter från länder utanför Europa (19).
Det som kallas ”nutritional transition” är en av många faktorer som kan motverka HME. Det handlar här om att byta matvanor med mycket fibrer och fullkornsprodukter, mot en kost med en högre andel fett, socker och processade livsmedel – och dessutom mer stillasittande.
Befolkningen i flera låg- och medelinkomstländer har under en period av snabb industrialisering och urbanisering även fått större tillgång till matolja och livsmedel med tillsatt socker (20). Under de senaste decennierna har tillgången på energigivande livsmedel ökat från 2000 kcal till nästan 3000 kcal per person och dag i Mellanöstern (21).
Denna globala utveckling är en av de viktigaste orsakerna till ökad förekomst av fetma och andra riskfaktorer för kardiovaskulära sjukdomar i låg- och medelinkomstländer (22-24). Denna trend kan också leda till att nyanlända från låg- och medelinkomstländer redan ändrat sin livsstil och sina matvanor och därmed har sämre hälsa kopplat till kardiovaskulära riskfaktorer, jämfört med de tidigare nyanlända migranterna (25).
Processen bakom ändrade matvanor efter migration – ackulturation
Tidigare internationella studier visar att genetiska faktorer inte kan förklara förekomsten av bland annat kardiovaskulära sjukdomar hos olika grupper av migranter. Sjukdomsförekomsten kan därför troligen bero på andra miljö- och livsstilsfaktorer, som till exempel matvanor. Studier av tre grupper av japaner i Japan, Hawaii och San Francisco, visade för första gången att matvanorna i det nya landet har en avgörande betydelse för förekomsten av kardiovaskulära sjukdomar bland personer med samma genetiska bakgrund (26, 27). Även senare studier bland andra grupper av migranter i Europa, Amerika och Australien bekräftar resultaten av de japanska studierna genom att visa starka samband mellan förändrade matvanor efter migrationen, och ökad dödlighet bland migranterna (15, 28-31).
En drivkraft som leder till ändrade matvanor bland migranterna är kostanpassning, ”dietary acculturation”, som är den process genom vilken migranterna anpassar sig till värdlandets matvanor (25). Processen är ett komplext möte mellan kulturer – och efterföljande anpassningar till det nya landets matkultur. Amerikanska och europeiska studier visar att det finns samband mellan graden av kostanpassning och riskfaktorer för kroniska sjukdomar (14, 32-35).
En av de mest använda modellerna för ackulturation, alltså vad som händer när två kulturer möts, introducerades av Berry och hans kollegor (36). I modellen föreslås assimilation, separation, integration och marginalisering som fyra anpassningsstrategier som individer brukar tillämpa i mötet med den nya kulturen vid migration. För kostanpassning i det nya landet kan modellen sammanfattas enligt följande:
- Integration innefattar både bevarande av den ursprungliga – och anpassning till den nya matkulturen.
- Assimilering innebär anpassning av matvanorna till den nya landets vanor. Den ursprungliga matkulturen förloras.
- Separation innebär att de ursprungliga matvanorna bevaras utan anpassning till den nya matkulturen.
- Marginalisering innebär förlust av den ursprungliga matkulturen samtidigt som den nya matkulturen avvisas. Snabbmat som till exempel hamburgare, pommes frites och kebab kan vara mat som individen väljer istället.
Immigranternas matvanor i Sverige
Antalet nya studier som beskriver immigranternas matvanor och livsmedelsval i Sverige är mycket begränsat och de flesta studier är minst 20 år gamla. Dessutom är andelen personer med migrationsbakgrund mindre representerade i nationella matvaneundersökningar – delvis på grund av stora bortfall (37). Bilden av hur matvanorna ändras efter migration är dock komplex och beror på faktorer som bland andra födelseland, socioekonomi, situationen i det nya landet (15).
Förändringarna av matvanor visar framför allt en väsentlig ökning av energi- och fettintag, animaliska produkter – samt minskat intag av kolhydrater, vilket leder till lågt intag av fibrer (29-31). Dessutom ökar intaget av mättade fettsyror på bekostnad av minskat intag av fleromättade fettsyror, från bland annat olivolja (30).
Ökat fettintag och minskad fysisk aktivitet relaterat till migration kan sannolikt förklara ökningen av sjukdomar som diabetes (35, 38) övervikt/fetma (39) och hjärt- och kärlsjukdomar (40, 41). Dessutom (se figur 1) verkar övervikt eller fetma vara vanligare bland personer som har bott i Sverige i mer än 10 år, jämfört med dem med kortare vistelsetid, samt svenskfödda personer (39).
En sammanställning av studier om nutritionsstatus bland utomeuropeiska migranter i Norden visade även hög förekomst av D-vitaminbrist, särskilt bland kvinnor i allmänhet, och i synnerhet gravida kvinnor (35).

Figur 1. Andel (%) personer över 16 år med övervikt eller fetma (BMI är 25,0 eller mer) fördelat på migrationsstatus och vistelsetid i Sverige, år 2020 (39).
Studier bland barn med migrationsbakgrund
Resultaten av de få studier som finns på barns matvanor visar att barn med utlandsfödda föräldrar äter mer frukt och grönsaker och dricker mindre mjölk jämfört med jämnåriga barn med svenskfödda föräldrar (42-44). Intaget av frukt och grönsaker är däremot ungefär hälften av det rekommenderade intaget bland de undersökta barnen med utlandsfödda föräldrar (42). Även intaget av en del viktiga mikronutrienter, som D-vitamin, kalcium och järn var mindre än näringsrekommendationer bland dessa barn (42, 43). Emellertid visade resultaten att barn med utlandsfödda föräldrar äter en kost som mer följer näringsrekommendationerna, jämfört med barn med svenskfödda föräldrar. Trots det var övervikt och fetma vanligare i den gruppen än hos barn med svenskfödda föräldrar på grund av lägre fysisk aktivitet (43).
I en annan svensk studie som undersökte förekomsten av karies bland barn, konstaterades att migrationsbakgrund var den starkaste prediktorn för kariesutveckling hos barn yngre än åtta år. Resultaten visade också att en större andel av barnen med migrationsbakgrund jämfört med barn med svenskfödda föräldrar konsumerade godis och läsk mer än en gång per vecka (45). Stora intag av söta och processade livsmedel bland utlandsfödda barn samt barn och ungdomar med föräldrar födda utanför Norden har också rapporterats i andra studier (44, 46).
Slutsats och förslag till förebyggande åtgärder
Migranter, och i synnerhet de som är födda utanför Europa, har en tendens att ändra sina matvanor i det nya landet. Denna förändring har oftast lett till högre intag av energi i relation till behovet och lägre intag av kostfibrer, essentiella fettsyror och viktiga mikronutrienter. Den nya anpassade kosten har visat sig vara en bakomliggande orsak till uppkomsten av flera riskfaktorer för kroniska sjukdomar som diabetes typ 2, övervikt och fetma samt kardiovaskulära sjukdomar.
Utifrån definitionen av integration som en strategi att anpassa sig till den nya kulturen, vore det bästa om immigranterna kan behålla hälsosamma matvanor från ursprungslandet – samtidigt som de lär sig en ny hälsosam matkultur i det nya landet. I denna process har hälsoprofessionerna inom vården, och i synnerhet legitimerade dietister, en avgörande roll för att vägleda personer med migrationsbakgrund till att formulera rimliga mål som kan uppnås och upprätthållas.
Målsättningen ska fokusera på förändringar i matvanor och ökad fysisk aktivitet som kan leda till energibalans som innebär att energiintaget via maten stämmer med energiförbrukningen. Vid behandling av övervikt eller fetma fokuserar behandlingsmålet däremot på lägre energiintag i förhållande till energiförbrukningen.
Legitimerade dietister kan också hjälpa personer med migrationsbakgrund till att upprätthålla sina traditionella matvanor och anta de hälsosamma aspekterna av det nya landets matkultur – eller båda. Dietisterna kan ge kostråd som inkluderar alla livsmedel som kan passa in i en hälsosam kost, utan att behöva eliminera livsmedel som har kulturella värden för individen. Mindre hälsosamma livsmedel med kulturella värden kan snarare ätas mer sällan eller i mindre mängder. Recepten kan också modifieras med avseende på salt, fettkvalitet, socker och tillagningsmetod.
Kostråden bör också inkludera information om portionsstorlekar, märkning av livsmedel, innehållsförteckning och grundläggande näringslära med fokus på energi- och näringsinnehåll i olika livsmedel. Den typen av information ger förutsättningar för en bättre förståelse av näringsdeklarationer som finns på de flesta färdigförpackade livsmedel, och därmed underlätta hälsosammare livsmedelsval.
Pedagogiskt informationsmaterial och andra skrifter från bland andra Livsmedelsverket (47) som baseras på nordiska näringsrekommendationer (48), kan vara bra hjälpmedel vid kostrådgivningen. Kostråden på en minut (se figur 2), är ett exempel på material som ger förslag till hälsosamma livsmedelsval baserade på de nordiska näringsrekommendationerna (49). Förslagen visar på ett enkelt sätt hur mindre hälsosamma livsmedel kan bytas till hälsosammare alternativ.

Figur 2. Kostråden på en minut – sammanfattning av Livsmedelsverkets kostråd vid val av hälsosamma livsmedel (49).
Det finns relativt få tillgängliga uppgifter om invandrarnas matvanor i Sverige och även om matvanorna i de tidigare hemländerna. Därför är det svårt att kunna ge en fullständig bild av hur matvanorna ändras efter migrationen till Sverige. Däremot finns det fler studier på födelselandets betydelse för förekomsten av nutritionsrelaterade sjukdomar, som i sin tur kan tyda på ohälsosamma matvanor bland utlandsfödda. Därför behövs mer omfattande forskning om hur matvanorna ändras i samband med migrationen till Sverige.
Författaren uppger inga jävsförhållanden.
Referenser
1. McAuliffe M, Khadria B. World migration report 2020. Geneva: International Organization for Migration. 2019.2.
2. Westin C. Sweden: Restrictive immigration policy and multiculturalism. Migration Information Source. 2006.3.
3. Skodo A. Sweden: By turns welcoming and restrictive in its immigration policy. Migration Information Source. 2018.
4. Utrikes födda i Sverige [Internet]. Statistiska centralbyrån, SCB 2021 [cited 2021-07-05]. Available from: https://www.scb.se/hitta-statistik/sverige-i-siffror/manniskorna-i-sverige/utrikes-fodda/
5. Statistikmyndigheten SCB. Befolkningsstatistik. 2020.
6. Marmot MG, Adelstein AM, Bulusu L. Lessons from the study of immigrant mortality. Lancet (London, England). 1984;1(8392):1455-7.
7. Cunningham SA, Ruben JD, Narayan KV. Health of foreign-born people in the United States: a review. Health & Place. 2008;14(4):623-35.
8. Singh GK, Rodriguez-Lainz A, Kogan MD. Immigrant health inequalities in the United States: use of eight major national data systems. The Scientific World Journal. 2013.
9. Beiser M. The health of immigrants and refugees in Canada. Canadian Journal of Public Health. 2005;96(2):30-44.
10. McDonald JT, Kennedy S. Insights into the ‘healthy immigrant effect’: health status and health service use of immigrants to Canada. Social Science & Medicine. 2004;59(8):1613-27.
11. Moullan Y, Jusot F. Why is the ‘healthy immigrant effect’ different between European countries? The European Journal of Public Health. 2014;24(suppl_1):80-6.
12. Anikeeva O, Bi P, Hiller JE, Ryan P, Roder D, Han G-S. Trends in cancer mortality rates among migrants in Australia: 1981–2007. Cancer Epidemiology. 2012;36(2):e74-e82.
13. Alyousif Z, Mathews AE. Impact of migration on diet, physical activity, and body weight among international students moving from the Gulf Countries to the United States. Case Rep J. 2018;2(7).
14. Gilbert PA, Khokhar S. Changing dietary habits of ethnic groups in Europe and implications for health. Nutrition Reviews. 2008;66(4):203-15.
15. Holmboe-Ottesen G, Wandel M. Changes in dietary habits after migration and consequences for health: a focus on South Asians in Europe. Food & Nutrition Research. 2012;56(1):889.
16. Koochek A, Mirmiran P, Azizi T, Padyab M, Johansson S-E, Karlström B, et al. Is migration to Sweden associated with increased prevalence of risk factors for cardiovascular disease? European Journal of Preventive Cardiology. 2008;15(1):78-82.
17. Bentham G. Migration and morbidity: implications for geographical studies of disease. Social Science & Medicine. 1988;26(1):49-54.
18. Maheswaran R, Strong M, Clifford P, Brewins L. Socioeconomic deprivation, mortality and health of within-city migrants: a population cohort study. J Epidemiol Community Health. 2018;72(6):519-25.
19. Helgesson M, Johansson B, Nordquist T, Vingård E, Svartengren M. Healthy migrant effect in the Swedish context: a register-based, longitudinal cohort study. BMJ Open. 2019;9(3):e026972.
20. Mendez MA, Popkin BM. Globalization, urbanization and nutritional change in the developing world. eJADE: electronic Journal of Agricultural and Development Economics. 2004;1(853-2016-56106):220-41.
21. Ghassemi H, Harrison G, Mohammad K. An accelerated nutrition transition in Iran. Public Health Nutrition. 2002;5(1a):149-55.
22. Imamura F, Micha R, Khatibzadeh S, Fahimi S, Shi P, Powles J, et al. Dietary quality among men and women in 187 countries in 1990 and 2010: a systematic assessment. The Lancet Global Health. 2015;3(3):e132-e42.
23. World Health Organization. Global status report on noncommunicable diseases 2014: World Health Organization; 2014.
24. Popkin BM, Adair LS, Ng SW. Global nutrition transition and the pandemic of obesity in developing countries. Nutrition Reviews. 2012;70(1):3-21.
25. Koochek A, Johansson S, Kocturk T, Sundquist J, Sundquist K. Physical activity and body mass index in elderly Iranians in Sweden: a population-based study. European Journal of Clinical Nutrition. 2008;62(11):1326-32.
26. Kato H, Tillotson J, Nichaman MZ, Rhoads GG, Hamilton HB. Epidemiologic studies of coronary heart disease and stroke in Japanese men living in Japan, Hawaii and California: serum lipids and diet. American Journal of Epidemiology. 1973;97(6):372-85.
27. Robertson TL, Kato H, Gordon T, Kagan A, Rhoads GG, Land CE, et al. Epidemiologic studies of coronary heart disease and stroke in Japanese men living in Japan, Hawaii and California: coronary heart disease risk factors in Japan and Hawaii. The American Journal of Cardiology. 1977;39(2):244-9.
28. Dixon LB, Sundquist J, Winkleby M. Differences in energy, nutrient, and food intakes in a US sample of Mexican-American women and men: findings from the Third National Health and Nutrition Examination Survey, 1988–1994. American Journal of Epidemiology. 2000;152(6):548-57.
29. Koochek A. Avhandling: Elderly Iranians in Sweden: The impact of migration on risk factors for cardiovascular disease. Karolinska Institutet, Institutionen för neurobiologi, vårdvetenskap och samhälle, 2008.
30. Kouris-Blazos A, Wahlqvist ML, Trichopoulou A, Polychronopoulos E, Trichopoulos D. Health and nutritional status of elderly Greek migrants to Melbourne, Australia. Age and Ageing. 1996;25(3):177-89.
31. Patel J, Vyas A, Cruickshank J, Prabhakaran D, Hughes E, Reddy K, et al. Impact of migration on coronary heart disease risk factors: comparison of Gujaratis in Britain and their contemporaries in villages of origin in India. Atherosclerosis. 2006;185(2):297-306.
32. Ayala GX, Baquero B, Klinger S. A systematic review of the relationship between acculturation and diet among Latinos in the United States: implications for future research. Journal of the American Dietetic Association. 2008;108(8):1330-44.
33. Rechel B, Mladovsky P, Ingleby D, Mackenbach JP, McKee M. Migration and health in an increasingly diverse Europe. The Lancet. 2013;381(9873):1235-45.
34. Wallace PM, Pomery EA, Latimer AE, Martinez JL, Salovey P. A review of acculturation measures and their utility in studies promoting Latino health. Hispanic Journal of Behavioral Sciences. 2010;32(1):37-54.
35. Wändell PE. Population groups in dietary transition. Food & Nutrition Research. 2013;57(1):21668.
36. Berry JW. Contexts of acculturation. In: Berry SJW, editor. The Cambridge handbook of acculturation psychology: Cambridge University Press; 2006. p. 27–42.
37. Amcoff E. Riksmaten-vuxna 2010-11: Livsmedels-och näringsintag bland vuxna i Sverige: Livsmedelsverket; 2012.
38. Bennet L, Nilsson C, Mansour‐Aly D, Christensson A, Groop L, Ahlqvist E. Adult‐onset diabetes in Middle Eastern immigrants to Sweden: Novel subgroups and diabetic complications—The All New Diabetes in Scania cohort diabetic complications and ethnicity. Diabetes/Metabolism Research and Reviews. 2020:e3419.
39. Undersökningarna av levnadsförhållanden [Internet]. Statistiska centralbyrån. 2020 [cited 2021-09-07]. Available from: http://www.statistikdatabasen.scb.se/pxweb/sv/ssd/START__LE__LE0101__LE0101H/LE01012019H01N/.
40. Hedlund E, Lange A, Hammar N. Acute myocardial infarction incidence in immigrants to Sweden. Country of birth, time since immigration, and time trends over 20 years. European Journal of Epidemiology. 2007;22(8):493-503.
41. Wändell P, Carlsson AC, Li X, Gasevic D, Ärnlöv J, Holzmann MJ, et al. Heart failure in immigrant groups: a cohort study of adults aged 45 years and over in Sweden. Scandinavian Cardiovascular Journal. 2018;52(6):292-300.
42. Enghardt Barbieri H, Pearson M, Becker W. Riksmaten-barn 2003: Livsmedels-och näringsintag bland barn i Sverige. In: Livsmedelsverket, editor. Uppsala: Ord & Form; 2006. p. 216.
43. Besharat Pour M, Bergström A, Bottai M, Kull I, Wickman M, Håkansson N, et al. Effect of parental migration background on childhood nutrition, physical activity, and body mass index. Journal of Obesity. 2014.
44. Säfsten E, Nyberg G, Elinder LS, Norman Å, Patterson E. The intake of selected foods by six‐year‐old Swedish children differs according to parental education and migration status. Acta Paediatrica. 2016;105(4):421-6.
45. Anderson M, Dahllöf G, Warnqvist A, Grindefjord M. Development of dental caries and risk factors between 1 and 7 years of age in areas of high risk for dental caries in Stockholm, Sweden. European Archives of Paediatric Dentistry. 2021:1-11.
46. Statens folkhälsoinstitut. Barn och unga 2013–utvecklingen av faktorer som påverkar hälsan och genomförda åtgärder. Samordnad folkhälsorapportering. 2013;2013:02.
47. Livsmedelsverket. Hitta ditt sätt – Att äta grönare, lagom mycket och röra på dig, Råd om bra matvanor – lättläst svenska. Livsmedelsverket. 2015.
48. Nordiska näringsrekommendationer (NNR). Bakgrund, principer och användning. Nordiska näringsrekommendationer 2012 – rekommendationer om näring och fysisk aktivitet. Livsmedelsverket. Hämtad; 2012.
49. Livsmedelsverket. Hitta ditt sätt – De svenska kostråden. 2015. p. 26.
Efsa utvärderar samband mellan socker och hälsa – och öppnar för synpunkter
Den Europeiska myndigheten för livsmedelssäkerhet, Efsa, har slutfört en vetenskaplig systematisk genomgång av sambandet mellan intag av socker – och olika sjukdomar och andra effekter på hälsan. Utvärderingen är omfattande, men kom inte fram till att fastställa ett högsta intag av socker där inga negativa hälsoeffekter uppkommer. Efsas slutsats är ändå att intaget av tillsatt och så kallat fritt socker, bör vara så lågt som möjligt för att inte påverka hälsan negativt. Nu är utvärderingen ute på remiss och Efsa välkomnar synpunkter från experter, organisationer och allmänheten.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
Utvärderingen visar ett samband mellan tillsatt och fritt socker och risk för flera sjukdomar, som fetma, höga blodfetter, typ 2-diabetes, fettlever och högt blodtryck. Sambandet mellan tillsatt socker och karies är väl etablerat. För gravida ingick i utvärderingen även risken för graviditetsdiabetes och påverkan på barnets födelsevikt.
Slutsatsen i Efsas utvärdering är att intaget av tillsatt och fritt socker bör vara så lågt som möjligt för att inte påverka hälsan negativt. Fritt socker är en typ av socker som bland annat finns naturligt i honung och fruktjuicer. Trots Efsas omfattande utvärdering var det inte möjligt att fastställa ett så kallat UL-värde eller en säker intagsnivå för socker utan att negativa hälsoeffekter kan uppkomma. UL (tolerable upper intake level) är en övre gräns för intag som bedöms att inte utgöra en risk för negativa hälsoeffekter för människor.
Genomgången visar att godis, drycker (sockersötade drycker och fruktjuicer) och bakverk är de livsmedelsgrupper som bidrar mest till intaget av tillsatt och fritt socker i de europeiska länderna. För barn och ungdomar handlar det också om sötade mjölk- och yoghurtprodukter. Intaget varierar mycket mellan olika grupper i befolkningen och variationen mellan länder är också stor.
Det är komplext att utvärdera sambandet mellan socker och hälsa, bland annat att skilja på vad som är sockrets enskilda effekt, på molekylnivå, och på vilket sätt socker påverkar energiintaget.
Efsa välkomnar nu synpunkter på den vetenskapliga utvärderingen – senast den 30 september.
Efsa arrangerar ett seminarium om utvärderingen den 21 september.
Länkar till infografik: Draft conclusions Efsa explains
Klart med fler systematiska litteraturöversikter för NNR2022
Uppdateringen av de nordiska näringsrekommendationerna, NNR2022, omfattar en rad systematiska litteraturöversikter inom vissa områden. Nu är det andra urvalet gjort.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
NNR2022-kommittén har beslutat om ytterligare fyra områden för systematiska litteraturöversikter, som ska ge en samlad bedömning av de samband man vill studera:
- Intag av vitt kött (främst kyckling) – och riskfaktorer, typ 2-diabetes och mortalitet av alla orsaker
- Intag av långkedjiga n-3 fettsyror från tillskott hos gravida – och astma och allergier hos barnet
- Intag av nötter hos vuxna – och hjärt- och kärlsjukdom och typ 2-diabetes
- Intag av kostfibrer hos barn – och tarmfunktion
Följande fem områden presenterades under våren:
- Intag av växtbaserat protein hos barn – och tillväxt hos barn
- Intag av baljväxter – och hjärt- och kärlsjukdom och typ 2-diabetes
- Intag av växtbaserat protein hos vuxna – och hjärt- och kärlsjukdom och typ 2-diabetes
- Vitamin B12 och vitamin B12-status i riskgrupper
- Fettkvalitet och mental hälsa
Uppdatering oktober 2021
Preliminärt ingick också ”Intag av D-vitamin från mat och tillskott hos barn, vuxna och äldre – och D-vitaminstatus” bland de prioriterade systematiska litteraturöversikterna, men i det slutgiltiga beslutet från hösten 2021 ingår inte D-vitamin. Detta beror bland annat på att det publicerats en hel del inom området av andra organisationer.
Ny avhandling presenterar en viktig väg för att främja hållbara matvanor
Maten är en av de största orsakerna till klimatförändringar och ohälsa globalt. Frågan är hur vi kan förändra våra matvanor för att stoppa dessa effekter. Skolmåltider kan nå barn av alla socioekonomiska bakgrunder och har en unik potential att främja hållbara matvanor hos den yngre generationen – som kan bestå till vuxen ålder. I sin doktorsavhandling visar Patricia Eustachio Colombo att det på olika sätt går att introducera barn till klimatvänliga, näringsrika, prisvärda och kulturellt lämpliga skolluncher utan att få ett ökat matsvinn eller ett minskat intag. Detta med skolluncher som minskar klimatpåverkan med 40 procent och har en lägre kostnad.
>>text: Patricia Eustachio Colombo, med dr i hållbar nutrition, Institutionen för global folkhälsa, Karolinska Institutet, Stockholm
Hållbara matvanor – varför och hur?
Det finns ett akut behov av att anpassa våra matvanor till målen för miljömässig hållbarhet och folkhälsa. Matvanor med låga intag av fullkorn, baljväxter, frukt och grönsaker, kombinerat med stor konsumtion av rött och processat kött, socker och salt bidrar alltmer till dödlighet och kroniska sjukdomar i många regioner i världen (1). Den nuvarande efterfrågan på livsmedel vidmakthåller också produktionssystem som idag står för ungefär en fjärdedel av alla växthusgasutsläpp (2). Att gå över till hållbara matvanor — ”med låg miljöpåverkan som bidrar till livsmedels- och näringssäkerhet och till ett hälsosamt liv för nuvarande och framtida generationer” (3) — är därför brådskande. För att lyckas ändra konsumtionsmönstren krävs både en fördjupad förståelse för de faktorer som påverkar våra matval i olika miljöer – och effektiva insatser som kan förhindra ohållbara matvanor (4).
Skolmåltider har identifierats som en viktig arena för att främja hälsa i samhället och minska sociala hälsoskillnader samtidigt som miljömässig hållbarhet beaktas (5). Skolmåltiderna kan nå de flesta, eller rent av alla barn, beroende på skolmåltidssystem (6, 7). Sverige är ett av få länder i världen där alla barn från förskoleklass till årskurs 9 nås av en fullt subventionerad lunch (8). I Sverige serveras årligen nästan 200 miljoner måltider i landets nästan 5000 grundskolor (8). Svenska skolmåltider har alltså stor potential att bidra till att främja sunda och miljövänliga matvanor hos alla barn, både på kort och lång sikt (9, 10).
I min avhandling ”Optimizing school meals today: a pathway to sustainable dietary habits tomorrow” (11) har jag gjort fyra forskningsstudier som på olika sätt bidrar till kunskap om hur hållbara matvanor kan uppnås genom skolmåltidssystemet i både teori och praktik.
Betydelsen av skolmåltider för kostintaget hos barn i Sverige
Den första delstudien (12) handlar om barnens intag av energi, näringsämnen och livsmedelsgrupper från skollunchen. Intaget beräknas och jämförs mellan flickor och pojkar, och mellan elevernas olika socioekonomiska bakgrund. Studien bygger på analyser som gjorts av matintaget hos de elever i årskurs 5 och 8 som deltog i den nationella matvaneundersökningen Riksmaten ungdom (2016-2017) (13).
Studien visar att skollunchen i genomsnitt stod för 20-30 procent av energi- och näringsintaget, och hamnar således under det mål på 30 procent av dagsbehovet som har satts upp för skolluncher (14). Resultaten visar också att skollunchen bidrog med nästan hälften av det totala dagsintaget av grönsaker, och ungefär två tredjedelar av fiskintaget.
Skollunchen har också en högre näringstäthet (g/10 MJ) och en lägre energitäthet (kJ/g) än de måltider som intogs under resten av dagen. Näringstäthet ger ett mått på måltidens kvalitet genom att beräkna mängd näringsämnen per energiinnehåll. Energitäthet mäter energiinnehåll relaterat till mängden av ett livsmedel eller en maträtt. För hög energitäthet i en måltid kan leda till ett för högt energiintag. Pojkar äter mer rött och processat kött och mindre med grönsaker och fibrer än flickor, både sett över hela dagen och under skollunchen. Detta reflekterar även matvanor hos vuxna i dag.
Sett över hela dagen så var intaget av energi samt de flesta näringsämnen och livsmedelsgrupper, som till exempel grönsaker, lägre hos barn till föräldrar med kortare utbildning. Under skollunchen däremot fanns nästan inga skillnader i energi- eller näringsintag eller mängden grönsaker mellan barn till föräldrar med kortare respektive längre utbildning. Detta visar att skollunchen kan spela en viktig roll i att utjämna sociala skillnader i matvanor, och ha betydelse för folkhälsan.
Hållbara skolluncher i teorin
Den andra delstudien (15) utvecklar en övergripande strategi för att utforma hållbara skolmåltider med hjälp av en metod som kallas linjär optimering. Utgångspunkten är livsmedelslistor från svenska grundskolor. Listorna innehåller information om all mat och dryck som köpts in för att tillaga skolluncher under ett helt skolår (2015/2016). Listan omfattar information om total inköpt vikt av respektive livsmedel, runt 700 olika livsmedel beroende på skola, samt jämförelsepriser. Livsmedelslistorna kopplades till Livsmedelsverkets livsmedelsdatabas – för matens näringsinnehåll – och RISE (Research Institutes of Sweden) klimatdatabas – för matens klimatpåverkan.
Jag använde sedan denna matematiska modell för att beräkna nya livsmedelslistor som uppfyller krav på näringsintaget och lägre klimatpåverkan – samtidigt som de skulle vara så lika ursprungslistorna som möjligt med avseende på livsmedelssammansättning och kostnad.
Beräkningarna visar att det var möjligt att minska på skolmåltidernas växthusgasutsläpp med omkring 40 procent utan att utesluta några livsmedel eller öka kostnaden. Detta samtidigt som måltidernas näringsriktighet uppfylldes. De nya listorna innehöll mindre med animaliska produkter och en större andel växtbaserade livsmedel.
Hållbara skolluncher i praktiken
Den tredje delen (16) i avhandlingen är en interventionsstudie som genomfördes för att studera acceptansen hos elever i grundskolan av skolluncher som bygger på resultatet i ovanstående studie. Den nya matsedeln, en hållbar 4-veckors skollunchmeny – som var näringsriktig, hade en 40 procent lägre klimatpåverkan och en 11 procent lägre kostnad än ursprungsmatsedeln—användes i tre grundskolor i Botkyrka kommun. Elevernas acceptans utvärderades genom att mäta det dagliga matsvinnet och lunchkonsumtionen under fyra veckor med den nya menyn. Perioden jämfördes sedan med fyra veckor med den ursprungliga matsedeln. Eleverna svarade också på ett frågeformulär som mätte deras tillfredsställelse med de olika typerna av skolluncher.
Analyserna visade att den nya hållbara menyn varken ökade matsvinnet eller förändrade elevernas konsumtion och tillfredsställelse med skolluncherna.
Möjligheter att skala upp
Den sista delstudien (17) fördjupar de tidigare delstudierna med fokusgruppsintervjuer för att utforska elevernas och kökspersonalens åsikter om den nya menyn. Syftet var också att identifiera utmaningar och möjligheter att framgångsrikt introducera hållbara skolmåltider i stor skala. Sex fokusgruppsdiskussioner genomfördes med elever i årskurs 5 (10-11 år) och årskurs 8 (14-15 år), och tre med kökspersonal. Data analyserades med hjälp av kvalitativ innehållsanalys, vilket innebar att en tolkning av innehållet i intervjuerna gjordes genom en systematisk kategorisering av teman och mönster.
Resultatet kan delas upp i fem huvudkategorier och 11 underkategorier. De fem huvudkategorierna är:
1. Erfarenheter av den nya menyn. Visade hur den nya menyn på olika sätt uppfattades av eleverna, och kökspersonalens erfarenheter av att arbeta med menyn. Kökspersonalen upplevde att eleverna var mindre nöjda med de nya måltiderna. Eleverna däremot uttryckte i allmänhet att de knappt märkte några skillnader alls på skolluncherna under den tid då den nya menyn serverades.
2. Betydelsen av hållbar mat. Det handlar om elevernas och kökspersonalens uppfattningar om konceptet hållbara matvanor och hur det präglade deras vardag. Båda grupperna framhåller hållbart ätande som viktigt i teorin men samtidigt någonting som är svårt att ta hänsyn till i vardagen.
3. Faktorer som påverkar acceptans av växtbaserade livsmedel. Innefattar aspekter såsom påverkan av sensoriska faktorer (smak, utseende och lukt), befintliga matvanor och grupptryck i valet att äta eller inte äta av skollunchen.
4. Möjligheter att öka växtbaserat ätande. Omfattar faktorer relaterade till elevernas och kökspersonalens idéer om hur man kan öka acceptansen av växtbaserade livsmedel. Här diskuterade både elever och kökspersonalen vikten i att introducera barn för växtbaserade rätter i tidig ålder, och att fokusera på sådant som barnen redan gillar snarare än att hitta på helt nya rätter.
5. Behovet av en stöttande miljö för att uppnå kostförändringar. Det handlar om elevernas och kökspersonalens tankar om vikten av mer kunskap, tid och resurser. Här betonar både elever och kökspersonal betydelsen av att göra elever, kökspersonal och andra aktörer mer engagerade i processen att introducera hållbara skolmåltider.
Slutsatser
Denna avhandling presenterar forskning som undersöker hur hållbara matvanor kan främjas genom skolmåltidssystemet. Min avhandling visar att det svenska skolmåltidssystemet har stor potential att främja hälsosamma och näringsrika matvanor hos barn. Skolmåltiderna kan också jämna ut ojämlikheter i matvanor mellan könen och social bakgrund på lång sikt.
Resultaten visar också att det är möjligt i praktiken att introducera näringsriktiga, överkomliga och klimatvänliga skolmåltider, utan att öka matsvinnet signifikant eller förändra elevernas konsumtion eller tillfredsställelse med skolluncher.
Den metod jag använder i avhandlingen fungerade i det svenska skolmåltidssystemet och skulle sannolikt också kunna överföras till andra offentliga måltidssystem som syftar till att upphandla och servera mer klimatvänliga och hälsosamma måltider.
Författaren uppger inga jävsförhållanden.
Referenser
1. Afshin A, Sur PJ, Fay KA, Cornaby L, Ferrara G, Salama JS, Mullany EC, Abate KH, Abbafati C, Abebe Z, et al. Health effects of dietary risks in 195 countries, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet 2019;393:1958–1972.
2. Climate Change and Land: An IPCC special report on climate change, desertification, land degradation, sustainable land management, food security, and greenhouse gas fluxes in terrestrial ecosystems. Intergovernmental Panel on Climate Change (IPCC), Geneva, Switzerland, 2019.
3. FAO. Sustainable diets and biodiversity – Directions and solutions for policy research and action. Proceedings of the International Scientific Symposium Biodiversity and Sustainable Diets United Against Hunger. Food and Agriculture Organization of the United Nations, Rome, 2010.
4. Garnett T, Finch J. What can be done to shift eating patterns in healthier, more sustainable directions? (Foodsource: chapters). Food Climate Research Network, University of Oxford, 2016.
5. WHO Regional Office for Europe. Food and nutrition policy for schools: a tool for the development of school nutrition programmes in the WHO European Region, 2016.
6. Willett W, Rockström J, Loken B, Springmann M, Lang T, Vermeulen S, Garnett T, Tilman D, DeClerck F, Wood A, et al. Food in the Anthropocene: the EAT–Lancet Commission on healthy diets from sustainable food systems. Lancet 2019;393:447–492.
7. Oostindjer M, Aschemann-Witzel J, Wang Q, Skuland SE, Egelandsdal B, Amdam GV, Schjøll A, Pachucki MC, Rozin P, Stein J, et al. Are school meals a viable and sustainable tool to improve the healthiness and sustainability of children´s diet and food consumption? A cross-national comparative perspective. Crit Rev Food Sci Nutr 2017;57:3942–3958.
8. Skolverket. Statistik om förskola, skola och vuxenutbildning. https://www.skolverket.se/skolutveckling/statistik/sok-statistik-om-forskola-skola-och-vuxenutbildning. Åtkomst 27 maj 2020.
9. State of School Feeding Worldwide. United Nations World Food Programme, Vienna, 2013.
10. Gauci C, Furtado A, Calleja A, Caldeira S, Storcksdieck genannt Bonsman S, Bakogian I, European Commission, Directorate-General for Health and Food Safety, Maltese EU Presidency team, European Commission, et al. Public procurement of food for health technical report on the school setting, 2017.
11. Eustachio Colombo P. Avhandling: Optimizing school meals today: a pathway to sustainable dietary habits tomorrow. Karolinska Institutet, 2021.
12. Eustachio Colombo P, Patterson E, Elinder LS, Lindroos AK. The importance of school lunches to the overall dietary intake of children in Sweden: a nationally representative study. Public Health Nutr 2020;23:1705–1715.
13. Moraeus L, Lemming EW, Hursti U-KK, Arnemo M, Sipinen JP, Lindroos A-K. Riksmaten Adolescents 2016–17: A national dietary survey in Sweden – design, methods, and participation. Food Nutr Res 2018;62:1381. https://doi.org/10.29219/fnr.v62.1381
14. Bra mat i skolan: råd för förskoleklass, grundskola, gymnasieskola och fritidshem. Livsmedelsverket, 2018.
15. Eustachio Colombo P, Patterson E, Elinder LS, Lindroos AK, Sonesson U, Darmon N, Parlesak A. Optimizing School Food Supply: Integrating Environmental, Health, Economic, and Cultural Dimensions of Diet Sustainability with Linear Programming. Int J Environ Res Public Health 2019;16:3019.
16. Eustachio Colombo P, Patterson E, Lindroos AK, Parlesak A, Elinder LS. Sustainable and acceptable school meals through optimization analysis: an intervention study. Nutr J 2020;19:61. https://doi.org/10.1186/s12937-020-00579-z
17. Eustachio Colombo P, Elinder LS, Patterson E, Parlesak A, Lindroos AK, Andermo S. Barriers and Facilitators to Successful Implementation of Sustainable School Meals: A Qualitative Study of the OPTIMAT-Intervention. 2021. https://doi.org/10.21203/rs.3.rs-139427/v1
Uppdatering av de nordiska näringsrekommendationerna – vad är på gång?
Revideringen av de nordiska näringsrekommendationerna, NNR, är i full gång och flera av projektets milstolpar har nåtts. En del är processen för prioriteringen av de systematiska litteraturöversikterna inom projektet.
>>text: Eva Warensjö Lemming, med dr och Hanna Eneroth, med dr, båda risk- och nyttovärderare vid Risk- och nyttovärderingsavdelningen, Livsmedelsverket, Uppsala
Just nu pågår arbetet med att revidera de nordiska näringsrekommendationerna (NNR) inför den sjätte upplagan (NNR2022), som beräknas vara klar i slutet av 2022. Upplagan innehåller, precis som tidigare, rekommendationer och referensvärden för energi och näringsämnen som ska tillgodose behovet för tillväxt, utveckling, funktion och hälsa genom hela livet. En nyhet i NNR2022 är en större vikt på livsmedelsgrupper och livsmedelsbaserade råd. Även samband mellan matvanor och miljömässig hållbarhet finns med i högre grad än tidigare.
Arbetet leds från Norge och två representanter från varje nordiskt land ingår i arbetsgruppen. Dessutom ingår observatörer från de baltiska länderna. Projektet finansieras av Nordiska ministerrådet och hälso-och livsmedelsmyndigheter i de deltagande länderna.
Arbetsprocess för att ta fram referensvärden och livsmedelsbaserade råd
Arbetet med att ta fram referensvärden och livsmedelsbaserade råd i NNR2022 genomförs i fyra steg (se figur 1) där oberoende ”funktioner” gör olika delar av arbetet och alla delar dessutom granskas. Uppdelning ska kvalitetssäkra underlagen, som denna gång tagits fram på ett mer transparent sätt än i tidigare revideringar. De livsmedelsbaserade råden i NNR ska ligga till grund för detaljerade kostråd i de olika länderna.
 Figur 1. Schematisk bild över processen för att ta fram referensvärden och livsmedelsbaserade råd i NNR2022. Referens: Figur översatt från projektets webbplats.
Figur 1. Schematisk bild över processen för att ta fram referensvärden och livsmedelsbaserade råd i NNR2022. Referens: Figur översatt från projektets webbplats.
Steg 1-Strategi
Den initiala strategiska planeringen är klar (steg ett). Bland annat har tre artiklar som beskriver ramverket för uppdateringen publicerats (1, 2, 3). Dessutom har experter rekryterats för att delta i arbetet med att utföra nya systematiska litteraturöversikter, så kallade de novo SR, i ett virtuellt center, NNR Systematic Review Centre (NNR SR-center). Andra experter ska också skriva och granska alla kapitel i NNR. Experterna rekryterades efter en allmän utlysning och hundratalet forskare är nu engagerade som experter i projektet. NNR SR-centret består av ett tiotal forskare från de nordiska länderna.
Steg 2-Orsakssamband
Just nu befinner sig arbetet med revideringen i steg två. För att undersöka och presentera samband mellan en nutritionsfaktor, exponering, och olika utfall används olika typer av underlag, som till exempel olika typer av litteraturöversikter. Se nedan förklaring av de olika typerna av litteraturöversikter som används.
Scoping review – en kartläggande litteraturöversikt som på ett systematiskt sätt går igenom samband mellan exponering och utfall utan att göra en slutlig sammanvägning av resultaten utifrån en specifik frågeställning.
Kvalificerad systematisk litteraturöversikt – redan tillgängliga systematiska litteraturöversikter som systematiskt gått igenom samband mellan exponering och utfall utifrån specifika frågeställningar och som uppfyller NNR:s kvalitetskrav. Innehåller kvalitetsgradering av de ingående studierna och en slutlig sammanvägning av resultaten.
De novo systematisk litteraturöversikt – nya systematiska litteraturöversikter, här ingår de som ska göras inom ramen för NNR2022.
Varje kapitel i NNR baseras på en uppdaterad kartläggande litteraturöversikt men även de andra typerna av litteraturöversikter som beskrivits och andra relevanta studier kan ingå. I steg två sker också det stora arbetet med att genomföra nya systematiska litteraturöversikter i NNR SR-centret och att foga samman de ingående kapitlen.
Steg 3-Integrering
I steg tre ska faktorer och förhållanden som kan påverka referensvärden och livsmedelsbaserade råd beaktas. För att kunna göra bedömningen kommer det att finnas fem bakgrundsartiklar som belyser livsmedels- och näringsintag, hälsoutmaningar i de nordiska och baltiska länderna, fysisk aktivitet, miljömässig hållbarhet och övervikt/fetma.
Steg 4-Referensvärden och livsmedelsbaserade råd
I steg fyra ska alla kapitel göras klara och referensvärden och livsmedelsbaserade råd fastställas.
Prioritering av ämnen till nya systematiska litteraturöversikter
Prioritering av ämnen till nya systematiska litteraturöversikter är centralt i uppdateringen av NNR, eftersom resultaten kan påverka referensvärden och livsmedelsbaserade råd. Prioriteringen har gjorts enligt en metod som beskrivs i detalj i en artikel som kommer att publiceras i Food & Nutrition Research. I korthet bygger prioriteringen på ämnen som nominerats av forskare, myndigheter, livsmedelsföretag, andra intressenter och allmänheten via en allmän utlysning. Förslagen på ämnen skickades in i ett formulär på projektets webbplats, en så kallad “PI/ECOTSS”.
En “PI/ECOTSS” är ett strukturerat sätt att formulera en klar och tydlig vetenskaplig frågeställning (4). ”PI/ECOTSS” är väletablerad inom forskningen och används ofta för att formulera frågeställningar när systematiska litteraturöversikter görs. Ett exempel på en PI/ECOTSS visas i figur 2. En “PI/ECOTSS” kan innehålla följande information om ämnet: befolkningsgrupp (population), intervention/exponering (intervention/exposure), jämförelser (comparators), utfall (outcome), uppföljning (timing), kontext (setting) och studiedesign (study design).
| Population (P) | Intervention or Exposure (I/E) | Comparators (C) | Outcomes
(O) |
Timing
(T) |
Setting
(S) |
Study design
(S) |
| Gravida kvinnor | Järnintag från kosten och järnstatus | Låga och höga intag
Låg och hög järnstatus
|
Utveckling av graviditets-diabetes | Månader eller år | Hög-inkomst-länder, nordisk kontext | Kohortstudier, interventions-studier, randomiserade studier och andra typer av studier |
Population befolkningsgrupp, intervention/exposure intervention/exponering, comparators jämförelser, outcome utfall, timing uppföljning, setting kontext, study design studiedesign
Figur 2. Exempel på en PI/ECOTSS som är ett strukturerat sätt att formulera vetenskapliga frågeställningar.
Totalt kom från den allmänna utlysningen 45 nomineringar som innehöll förslag på fler än 200 samband att undersöka. För att identifiera ytterligare potentiella ämnen för systematiska litteraturöversikter gjorde arbetsgruppen en genomgång av publicerade översiktsartiklar, som täckte de 51 näringsämnen och livsmedelsgrupper som är relevanta för NNR. Även denna genomgång resulterade i “PI/ECOTSS”.
För att undvika duplicering av redan publicerade systematiska litteraturöversikter identifierades 80 kvalificerade systematiska litteraturöversikter av arbetsgruppen. Av alla PI/ECOTSS som identifierats och som inte redan undersökts i en publicerad kvalificerad systematisk litteraturöversikt valdes 52 ut som relevanta. Därefter rankades ämnena som hög (n=21), medel (n=9) eller låg (n=22). De ämnen som rankats högt prioriterades i Delfi-processen i tre steg. I korthet innebär Delfi-processen att ämnena rankades av alla i arbetsgruppen, med en gemensam diskussion om resultatet efter varje omgång av individuell rankning. De fem första ämnena som valts ut för systematiska litteraturöversikter finns beskrivna i tabell 1. Ämnena för resterande fem systematiska litteraturöversikter inom projektet, kommer att väljas ut och presenteras på projektets webbplats framöver.
Tabell 1. De fem första systematiska litteraturöversikterna som ska genomföras i NNR-projektet.
| Näringsämne/
livsmedelsgrupp
Åldersgrupp |
Exponering | Utfall |
| Protein
Små barn från 6 månader |
Totalt intag av protein: Lågt och högt intag
Mängd protein från olika källor |
Antropometri till exempel längd och vikt |
| Baljväxter
Vuxna och äldre |
Olika typer av baljväxter
Lågt eller högt intag Dos-respons-samband |
Hjärt-kärlsjukdom och diabetes typ 2. Riskmarkörer för hjärt-kärlsjukdom och diabetes, insulinresistens och insulinkänslighet |
| Protein
Vuxna |
Jämföra intag av protein från animalier mot proteiner från växtriket | Hjärt-kärlsjukdom och diabetes typ 2. Riskmarkörer för hjärt-kärlsjukdom och diabetes, insulinresistens och insulinkänslighet |
| Vitamin B12
De mest känsliga grupperna: barn, gravida, ammande, äldre, veganer |
Olika exponeringsnivåer från supplement och intag via maten | Vitamin B12-status |
| Fett och fettsyror
Medelålders vuxna och äldre (från 50 år) |
Olika typer av fettsyror och fettyper (ej totalt fett) | Kognitiva utfall, som Alzheimers sjukdom och demens |
Följande typer av studier kommer att användas: randomiserade studier, interventionsstudier och prospektiva kohortstudier.
Ett kapitel uppdateras som en kartläggande litteraturöversikt, men tar in underlag från de nya systematiska litteraturöversikterna från NNR SR-centret, andra kvalificerade systematiska litteraturöversikter och övriga relevanta studier. Kapitel som fanns med i NNR 2012 utgör en utgångspunkt. Men i NNR2022 ingår som tidigare nämnts många fler kapitel, till exempel om livsmedelsgrupper.
Integrering av miljömässig hållbarhet i de livsmedelsbaserade råden
Det Nordiska ministerrådet har som mål att Norden ska vara världens mest hållbara och integrerade region år 2030. Därför kommer det också vara större fokus på hållbarhet i NNR2022. Ett av delmålen för projektet är att ta fram en plattform för hur miljömässig hållbarhet ska integreras i livsmedelsbaserade råd.
Detta arbete är komplext och därför har projektet tagit hjälp av Chatham House i London, ett oberoende institut som arbetar med olika typer av policyfrågor. Chatham House kommer att stödja skrivandet av de två bakgrundsartiklarna och en artikel som beskriver själva integrationen av miljömässig hållbarhet i NNR. I skrivargruppen kommer det finnas representanter från arbetsgruppen och experter från de nordiska och baltiska länderna.
Författarna uppger inga jävsförhållanden.
Tidigare publiceringar om NNR2022 på Nutritionsfakta:
Nordiska näringsrekommendationer 2022 – nu är de första artiklarna om metodiken publicerade
Hållbarhet ställer nya krav på näringsrekommendationer
Klart med de första systematiska litteraturöversikterna för NNR2022
Referenser
1. Christensen JJ, Arnesen EK, Andersen R, Eneroth H, Erkkola M, Høyer A, Lemming EW, Meltzer HM, Halldórsson ÞI, Þórsdóttir I, Schwab U, Trolle E, Blomhoff R. The Nordic Nutrition Recommendations 2022 – principles and methodologies. Food Nutr Res. 2020 Jun 18;64. doi: 10.29219/fnr.v64.4402. PMID: 32612489; PMCID: PMC7307430.
2. Arnesen EK, Christensen JJ, Andersen R, Eneroth H, Erkkola M, Høyer A, Lemming EW, Meltzer HM, Halldórsson ÞI, Þórsdóttir I, Schwab U, Trolle E, Blomhoff R. The Nordic Nutrition Recommendations 2022 – handbook for qualified systematic reviews. Food Nutr Res. 2020 Jun 18;64. doi: 10.29219/fnr.v64.4404. PMID: 32612492; PMCID: PMC7307435.
3. Arnesen EK, Christensen JJ, Andersen R, Eneroth H, Erkkola M, Høyer A, Lemming EW, Meltzer HM, Halldórsson ÞI, Þórsdóttir I, Schwab U, Trolle E, Blomhoff R. The Nordic Nutrition Recommendations 2022 – structure and rationale of qualified systematic reviews. Food Nutr Res. 2020 Jun 18;64. doi: 10.29219/fnr.v64.4403. PMID: 32612488; PMCID: PMC7307429.
4. Thabane L, Thomas T, Ye C, Paul J. Posing the research question: not so simple. Can J Anaesth. 2009 Jan;56(1):71-9. doi: 10.1007/s12630-008-9007-4. Epub 2008 Dec 24. PMID: 19247780.
Biomarkörer för att mäta matvanor
Notis
Webbinarium 26-27 april 2021
Årligen anordnar Nätverket Epidemiologi Och Nutrition (NEON) nationella möten inom olika områden relaterade till forskning inom mat och hälsa. Temat för årets möte var biomarkörer och rubriken på mötet var ”Dietary biomarkers for measuring food habits – possibilities and challenges”. I år arrangerades mötet som ett webbinarium av NEON, Kungliga Vetenskapsakademiens (KVA) Nationalkommitté för Nutrition och Livsmedelsvetenskap och EpiHealth. Inspelningen av webbinariet finns tillgänglig via NEON:s och KVA:s webbplatser.
Nyckelhålet blir ännu grönare
Nyckelhålet – Livsmedelsverkets märkning för nyttigare mat – har funnits i över 30 år och utvecklas hela tiden. Märkningen ställer krav på mer fullkorn och fibrer, mindre socker och salt och nyttigare fett. Den första mars trädde nya kriterier för märkningen i kraft, som innebär att fler växtbaserade rätter kan märkas och att det blir enklare att märka nyttiga färdigrätter.
>> text: Veronica Öhrvik, AgrDr, Avdelningen för hållbara matvanor, Livsmedelsverket, Uppsala
Nyckelhålets kriterier baseras på de nordiska näringsrekommendationerna, NNR, (1) och revideras regelbundet för att följa med i förändringar i matvanor, näringsrekommendationer och kostråd.
Första mars i år trädde den tionde versionen av Nyckelhålsföreskrifterna i kraft (2). De två huvudsakliga syftena med den nya versionen var att göra det enklare att Nyckelhålsmärka färdigrätter genom förenklade, men inte mindre strikta kriterier – och att göra det enklare att äta grönt, i enlighet med NNR och Livsmedelsverkets kostråd.
Färre men lika strikta
Tidigare krävdes att sammanlagt 11 villkor på produkt- och näringsämnesnivå skulle uppfyllas för att färdigrätter skulle kunna märkas. Företagen uppgav också att ju mer sammansatta produkterna är, desto svårare är det att märka dem med Nyckelhålet (3). Konsumenterna anser att det är svårast att hitta just färdigrätter och vegetariska produkter med Nyckelhålet (4), eftersom utbudet är litet. 2019 var det bara några enstaka procent av färdigrätterna som var Nyckelhålsmärkta (5).
Samtidigt ökar efterfrågan på färdigrätter. Syftet med revideringen av kriterierna för färdigrätter var därför att ta bort de villkor som gjorde reglerna för komplexa, och som var mindre relevanta för den hälsosamma helheten: mer fullkorn och grönt, mindre salt och socker och nyttigare fett.
De krav som har strukits är:
- Kravet om energiinnehåll per portion, vilket också gör att nu kan även flerportionsförpackningar märkas.
- Kravet om maxhalt av salt per portion – men krav på salt per 100 gram finns kvar.
- Kravet på andel av energiinnehållet som kommer från fett – ändrat till en maxgräns i gram för att göra det enklare att förstå.
I de reviderade kriterierna för Nyckelhålsmärkningen har det förtydligats att mindre mängder mjöl, till exempel för redning, inte behöver vara fullkornsmjöl. Dessutom gäller det endast för panerade produkter att tillagningsanvisningen inte får innebära att fett tillförs. Förhoppningen är att förändringarna ska leda till fler Nyckelhålsmärkta färdigrätter på marknaden.
Lättare att äta grönt
Ett studentarbete från SLU 2019 (6) visade att Nyckelhålet behöver utvecklas för att göra det enklare att följa kostrådet att äta grönare. Förslagen har lett till en rad konkreta förändringar i den nya versionen:
- Fullkorn kan nu delvis eller helt ersättas av baljväxter, grönsaker eller rotfrukter i spannmålsbaserade produkter.
- Kött kan delvis ersättas av fullkorn, baljväxter, grönsaker eller rotfrukter i köttprodukter.
- Växtbaserade produkter breddas genom att ändra kravet på socker till tillsatt socker för att göra det möjligt att rotfruktsbiffar och liknande produkter som naturligt innehåller lite mer socker kan märkas med Nyckelhålet.
- Växtbaserade produkter breddas också genom att kravet på max 33 procent mättat fett ändras till en maxgräns i gram istället. Många av produkterna i kategorin har en mycket låg fetthalt vilket tidigare gjorde att ett innehåll på mindre än ett halvt gram mättat fett per 100 gram kunde innebära att produkten inte kunde märkas.
- En ny kategori ”skivade vegetabiliska pålägg” har införts. Kategorin har högre salthalt än övriga vegetabiliska produkter. Det tog emot för oss i den nordiska gruppen att ändra till en högre salthalt eftersom det med dagens matvanor inte räcker att alltid välja Nyckelhålsmärkt för att komma ner i populationsmålet på 6 gram salt per dag och person (7). Men vi bedömde att det annars var orealistiskt att företagen skulle märka några produkter inom denna kategori. Det är fortfarande ett striktare kriterium än för salt i skinka och i princip samma nivå som för ost.
Vegetariska produkter är ett segment som växer mycket snabbt och därför såg vi ett stort behov av att uppdatera kriterierna för produktgruppen. Samtidigt som ändringarna förhoppningsvis underlättar märkning med Nyckelhålet, ställs nu också högre krav på ingredienserna i de vegetariska produkterna. Minst 50 procent ska bestå av fullkornsspannmål, grönsaker, baljväxter, rotfrukter eller icke-animaliskt protein. Förut låg gränsen på att 60 procent av råvarorna skulle vara vegetabiliska, men då kunde till exempel produkter huvudsakligen framställda på vanligt mjöl märkas.
Välkänt och välanvänt
Nyckelhålet är en av de mat-märkningar som konsumenter känner till allra bäst. Mer än 95 procent av alla konsumenter i Sverige har hört talas om Nyckelhålet – och det gäller oavsett kön, utbildningsnivå, inkomst och bostadsort. Åtta av tio av dem som känner till Nyckelhålet förknippar märkningen med hälsosam mat och mer än fem av tio uppger att de använder Nyckelhålet för att välja hälsosamt (4).
Även företagen uppger att de använder Nyckelhålet. Enligt ett mastersarbete vid SLU använder nästan nio av tio av de större producenterna Nyckelhålet på sina produkter och mer än hälften uppger att de för viss del av sitt sortiment använder Nyckelhålet som riktmärke vid produktutveckling (8).
Nyckelhålet används även praktiskt inom vården. Enligt en undersökning från 2017 hade tre av fyra dietister och mer än hälften av läkarna och sjuksköterskorna använt Nyckelhålet i sitt arbete under det senaste året (9). Nyckelhålet har även visat sig vara ett uppskattat verktyg för föräldrar till överviktiga barn (10).
Nyckelhålet används även inom preventivt arbete. Ett exempel är de satsningar Angereds Närsjukhus gör för jämlik hälsa. De anordnar bland annat butiksvandringar där deltagarna får tips och information om hälsosamma val i matbutiken. Deltagarna får bland annat reda på vad Nyckelhålsmärkning innebär och vid dessa vandringar är Nyckelhålet ”jätteuppskattat” (11). Ett annat exempel är den bok som BVC delar ut till landets 5-åringar för att uppmuntra till läsglädje och kunskap om hur kroppen fungerar (12). Barnen uppmuntras där bland annat att leka Nyckelhåls-detektiver.
Men det finns såklart en hel del som kan förbättras. Till exempel vet bara 3 av 10 konsumenter att Nyckelhålet innebär mindre salt (4). Att titta efter Nyckelhålet är ett av de enklaste sätten att minska sitt saltintag – vilket mer än hälften av befolkningen uppger att de åtminstone försöker då och då (13). Vet man inte att Nyckelhålet står för mindre salt kommer man inte heller använda märkningen för att välja produkter med mindre salt.
Nyckelhålet anses inte heller vara särskilt modernt – främst i de äldsta åldersgrupperna (4). Det har också bekräftats i en enkät till sjuksköterskor, där de som ger råd om Nyckelhålet framför allt verkar vara sjuksköterskor mellan 21 och 30 år. De övriga uppgav att de ”Saknar tillräcklig kunskap om kostrådet”, ”Anser att det ligger utanför mitt ansvarsområde” och ”Anser kostrådet omodernt” (14).
Livsmedelsverket skulle behöva arbeta mer för att öka både kunskap och förståelse för Nyckelhålet, för att nå ut med budskapet att det inte behöver vara så svårt som det kan kännas att förbättra sina matvanor. Det går att äta hälsosammare utan att ställa om hela livet. Det är just det som Livsmedelsverket vill lyfta fram genom sitt nya sätt att kommunicera om Nyckelhålet – Det handlar inte om att byta liv.
Första märkningen i sitt slag
Idag finns det många märkningar globalt för hälsosamma val av livsmedel och EU-kommissionen ska 2022 ge förslag på harmoniserad märkning i EU.
När Nyckelhålet lanserades av Livsmedelsverket 1989 var det unikt och 2009 började Nyckelhålet även användas i Norge och Danmark och 2013 på Island. Sedan dess är Nyckelhålet ett nordiskt samarbete, både för regelverket och kommunikationen kring märkningen.
Syftet med Nyckelhålet är att underlätta för konsumenter att göra hälsosamma val. Nyckelhålet visar på de bästa alternativen, med de nordiska näringsrekommendationerna som utgångspunkt, i varje produktgrupp som omfattas av Nyckelhålet. Nyckelhålet står för mindre socker och salt, mer fullkorn, fibrer, grönsaker, baljväxter, rotfrukter och nyttigare fett.
Nyckelhålet är också ett sätt att uppmuntra branschen att utveckla hälsosammare alternativ. Det är frivilligt och avgiftsfritt att använda Nyckelhålet, men de företag som gör det måste följa reglerna och märkningen omfattas av offentlig kontroll. Legalt räknas Nyckelhålet som ett näringspåstående.
Författaren uppger inga jävsförhållanden.
Referenser
1. Nordic Council of Ministers. Nordic Nutrition Recommendations 2012. Integrating nutrition and physical activity. Köpenhamn. Danmark.
2. Livsmedelsverkets föreskrifter om användning av symbolen Nyckelhålet; LIVSFS 2005:9.
3. Nyckelhålets påverkan på produktutvecklingen under 25 år. Ipsos. 2015. Stockholm.
4. Öhrvik V. 2021. L 2021 nr 06: Vad tycker konsumenterna om Nyckelhålet. Livsmedelsverkets rapportserie. Uppsala.
5. 2020. Slutrapport: Regeringsuppdrag Nyckelhålet 2017–2019. Livsmedelsverkets regeringsuppdrag. Uppsala.
6. Ramberg E. En utredning av Nyckelhålet med fokus på miljömässig hållbarhet – Ger kriterierna vägledning för Livsmedelsverkets kostråd “ät grönare”? Kandidatarbete 2019. SLU, Uppsala.
7. Åhlin J. Nutritional benefits achieved when exchanging certain food products with those labeled with the Keyhole symbol. Masterarbete 2015. Stockholms universitet, Stockholm.
8. Andersson C. The Nordic Keyhole – quantitative analysis of its use in product reformulation and development. Masterarbete 2021. SLU, Uppsala.
9. Orbe J & Theroell C. En kvantitativ undersökning om förtroendet för Livsmedelsverket bland kostarbetare 2017. SIFO (1537248).
10. Ek A, et al. Responding positively to “children who like to eat”: Parents’ experiences of skills-based treatment for childhood obesity. Appetite 2020; 145: 104488.
11. Muntligt Maria Magnusson, Angereds Närsjukhus
12. Sundström J, et al. Saga-sagor Fiffiga kroppen och finurliga knoppen. 2019. Bonnier Carlsen Bokförlag. Stockholm.
13. 2021. Konsumenternas kunskap om och attityd till salt. Opublicerad data.
14. Lindqvist S, et al. Kostråd från sjuksköterska till patient: En kvantitativ studie om sjuksköterskors kännedom om och förmedling av Livsmedelsverkets kostråd till patienter. Kandidatarbete 2018. Uppsala universitet.
Glöd i stället för tomtebloss – psykologiprofessor Magnus Lindwall om motivation och hälsa
Intervju
Vad motiverar oss till att äta mer hälsosamt, träna eller minska i vikt? Cecilia Nälsén har intervjuat Magnus Lindwall, professor i psykologi med inriktning hälsopsykologi som forskar om hållbar motivation. Han berättar om hur var och en oss skapar motivationen för sig själv, hur den kan få oss att leva hälsosamt och må bättre – utan att ge upp.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
Motivation kan beskrivas som drivkrafter som ligger bakom vårt beteende och vår ansträngning, och även riktningen och intensiteten på ansträngningen.
– Ofta pratar man allmänt om motivation till vardags och fokuserar på kvantitet, hur motiverad du är. Forskningen går djupare och handlar om typen av motivation, kvaliteten, det som håller över tid, säger Magnus Lindwall.
Forskningen utgår främst från den så kallade självbestämmandeteorin (self-determination theory). En stor del av forskningen om motivation baseras på denna idag 50-åriga teori, som kan liknas vid en flygbild av terrängen. Grunden i självbestämmandeteorin är vad som skapar hållbar motivation och hur den påverkas av vår miljö och omgivning.
– En styrka i teorin är att den baseras på breda principer och innefattar många delar som man sedan skräddarsyr efter olika frågeställningar. Självbestämmandeteorin har lett till utvecklingen av verktyg för att skapa hållbar motivation, berättar Magnus Lindwall.
Centrala begrepp inom teorin är självbestämmande och kontrollerande motivation. Magnus Lindwall understryker att det är den självbestämmande motivationen man vill nå för att skapa en hållbar motivation som gör att vi fungerar och mår bättre.
– Typen av motivation, kvaliteten, är viktig och avgör om motivationen blir hållbar över tid. Livet är som ett Vasalopp, och vi behöver en hållbar drivkraft för att glöda och orka hålla i beteendet, och inte en tillfällig gnista, betonar Magnus Lindwall.
Forskningen visar att sannolikheten ökar att vi når en självbestämmande motivation om vi känner oss tillfredsställda med tre psykologiska behov: kompetens, autonomi och tillhörighet.
Om vi känner att vi lyckas med något leder det till att vi känner kompetens – och fortsätter därmed. Med autonomi menas valfrihet och frivillighet i ett beteende, till exempel att du själv väljer vilken mat du lagar. Känner du tillhörighet eller social samhörighet med andra, att du delar samma åsikter med andra vad du ska äta och inte äta, är det större sannolikhet att en självbestämmande och hållbar drivkraft skapas. Man kan likna det vid att du sitter i förarsätet i bilen och styr, och inte i baksätet.
– Om du däremot känner att du inte lyckas och att beteendet är påtvingat då ökar sannolikheten att du inte fortsätter. I förlängningen fungerar och mår du sämre. Drivkraften finns i alla men genom att skapa en miljö där du uppfyllt de tre psykologiska behoven kan hållbar motivation byggas, säger Magnus Lindwall.
Den kontrollerande typen av motivation kan vara en belöning eller att undvika ”straff” eller dåligt samvete, till exempel utföra något för att undvika att få skäll, alltså något påtvingat. Kontrollerande motivation kan också vara att du själv fungerar som kontrollant – att du äter nyttigt för att inte få dåligt samvete. Kontrollerande motivation kan fungera som kortsiktig motivation men är inte hållbar på längre sikt enligt Magnus Lindwall.
Hans forskning är baserad på självbestämmandeteorin, och främst om fysisk aktivitet och träning. Personer som känner kompetens, autonomi och tillhörighet kopplad till sin träning har större sannolikhet till självbestämmande motivation.
– Det leder till att träningen blir hållbar och att personerna fortsätter vara fysiskt aktiva och inte slutar träna. Centralt i min forskning har varit att studera hur denna hållbara drivkraft skapas.
Det finns än så länge lite forskning om motivation och matvanor eller viktminskning, men det skulle kunna vara liknande principer som för motivation och fysisk aktivitet och andra hälsobeteenden, anser Magnus Lindwall.
– Du kan känna dig kompetent genom att lyckas laga hälsosammare mat. När förändringen inte är påtvingad och när du känner stöd från dina närmaste eller social tillhörighet till en grupp, då kan det leda till en förändring som håller i sig över tid.
Är det skillnad i teorin bakom att komma i gång med ett positivt hälsobeteende och att upprätthålla det?
– Det kan vara bra att komma i gång med en ny vana i små steg så att du känner dig kompetent – att du lyckas komma i gång. Starten kan vara kontrollerande motivation i form av råd från läkare att äta mer hälsosamt. Om motivationen sedan ska bli hållbar bör du snabbt känna valfrihet och att den övergår i självbestämmande motivation. Det är ingen nackdel för motivationen om den nya vanan är belönande i sig, konstaterar Magnus Lindwall.
Hållbar motivation kommer vid två typer av motivation, inre och yttre motivation. Inre motivation kan till exempel vara att ett beteende i sig är belönande, till exempel att äta något som är nyttigt och gott. Inre motivation bidrar till känslan av meningsfullhet och är en kraftfull typ av motivation.
Yttre motivation handlar om att du accepterat argumenten bakom, till exempel att du tränar regelbundet för att må bra.
– Ett viktigt begrepp inom den självbestämmande teorin är internalisering. Internalisering är att du tar in värdet från yttre källor och gör om dem till dina egna och på så sätt leder det till en självägande och hållbar motivation.
Skiljer sig motivationen mellan kvinnor, män, ungdomar och barn?
– Principerna gäller generellt för alla, men kan innebära olika saker för olika grupper. Man behöver förstå andras perspektiv och innebörden av att känna sig kompetent. Vad som är utvecklande kan skilja sig mycket beroende på till exempel ålder.
Dina bästa tips för att skapa hållbar motivation?
– Försök att hitta tillfällen då de tre psykologiska behoven möts. Vill du motivera andra behöver du inventera hur drivkrafterna ser ut i gruppen för att skapa en miljö där dessa tre behov nås. Det finns också verktyg som kombinerar delar från den självbestämmande teorin med till exempel motiverande samtal.
Hur kan jag under pandemin motivera mig till att träna och äta hälsosamt?
– Sätt målet lågt. Ha inte för höga ambitioner och ta små steg i början. Nöj dig med en promenad och inte en lång joggingtur, och ändra inte hela kosten på en gång utan börja till exempel med att äta mer grönsaker, tipsar Magnus Lindwall.
– Gläd dig över små vinster. Om målet är satt för högt är risken större att du känner att du misslyckas och sannolikheten att du lägger av ökar. Vi behöver glöda under lång tid för att motivationen ska bli hållbar och inte explodera som ett tomtebloss.
Lästips: Motivationsrevolutionen: från temporär tändning till livslång låga av Magnus Lindwall och Olof Röhlander, Bokförlaget Forum, 2020.
Samband behöver inte betyda orsak
Notis
Lästips om tolkning av vetenskapliga studier: Artikeln ”Samband” behöver inte betyda ”orsak” från tidningen Vetenskap & Praxis som ges ut av Statens beredning för medicinsk och social utvärdering, SBU.
Osäker på hur koststudier ska tolkas och värderas? Livsmedelsverkets rapport ger vägledning
Interventionsstudier. Randomiserade kontrollerade studier.
Observationsstudier. Systematiska litteraturöversikter.
Det är bara några olika typer av forskningsstudier. En rapport från Livsmedelsverket reder ut begreppen och ger vägledning till hur resultaten ska tolkas och värderas inom nutrition.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
Nyheter och uttalanden om mat och hälsa väcker ofta intresse i media, men är många gånger svåra att värdera och bedöma. Vem är avsändare? Hur tillförlitliga är resultaten?
För att utforma rekommendationer och råd om näringsämnen och livsmedel som vilar på en vetenskaplig grund krävs en samlad bedömning av den vetenskapliga litteraturen. De nordiska näringsrekommendationerna, NNR, är grunden för Livsmedelsverkets arbete inom mat och hälsa. Även sammanställningar av den vetenskapliga litteraturen i form av rapporter från andra myndigheter och organisationer eller i form av översiktsartiklar är viktiga. Det kan till exempel vara sammanställningar från den Europeiska myndigheten för livsmedelssäkerhet (Efsa) och Världshälsoorganisationen (WHO).
Värdering och hantering är två separata delar
Livsmedelsverket arbetar med kostråd enligt en process som grundas på riskanalysens principer, ett vetenskapligt arbetssätt som används inom EU. Riskanalysen består av tre olika delar: riskvärdering, riskhantering och riskkommunikation. Detta innebär att man skiljer på värdering och hantering. Värderingen utgörs av det vetenskapliga underlaget, till exempel för NNR. Hanteringen utgörs här av kostråden, alltså åtgärder för att minska risker som identifierats. Andra hanteringar än kostråd förekommer också, som lagändringar eller berikning av livsmedel. När kostråd tas fram vägs även andra relevanta faktorer in, till exempel matkultur, miljöaspekter och livsmedelsutbud.
Olika typer av studier
I rapporten beskrivs olika typer av studier för att bedöma det vetenskapliga underlaget inom nutritionsområdet – och för- och nackdelar med dessa.
Interventionsstudier
Interventionsstudier innebär en jämförelse mellan minst två alternativ och oftast en randomisering, slumpmässig fördelning, av deltagarna till olika grupper. Interventionsgruppen utsätts för det som ska prövas, till exempel att de ska äta medelhavskost, medan kontrollgruppen lever som vanligt, eller följer en kost som är typisk för normalbefolkningen. Sedan jämförs förändringen mellan interventionsgrupp och kontrollgrupp för att ta reda på om interventionen haft någon effekt på ett bestämt hälsoutfall, till exempel typ 2-diabetes.
Interventionsstudier ger generellt ett högt bevisvärde vid utvärdering av studier, men eftersom metoden kan skilja mycket mellan olika interventionsstudier måste kvaliteten på varje enskild studie bedömas. Det finns problem med interventionsstudier där kostfaktorer undersöks, till exempel för att studier behöver pågå under lång tid för att visa om interventionen påverkar risken för att utveckla en sjukdom. Dessutom är det svårt att få deltagare att ändra sin kost under flera år. I denna typ av studier kan istället en indikator på sjukdom användas; exempelvis kan deltagarnas blodtryck mätas där högt blodtryck kan vara en indikator för ökad risk för hjärt- och kärlsjukdom.
Bland interventionsstudierna har randomiserade kontrollerade studier (RCT) högst bevisvärde eftersom de på ett kontrollerat sätt har fördelat så kallade störfaktorer (confounders), till exempel ålder, lika mellan undersökningsgrupperna. På så sätt minskar man risken för att andra faktorer än det man vill undersöka skiljer sig mellan grupperna. En RCT är utformad för att mäta direkta samband mellan det som studeras och en eller flera effekter.
I läkemedelsstudier är det ett krav att göra RCT, men RCT är mindre vanlig vid i studier med kostfaktorer. Olika näringsämnen och bioaktiva ämnen (till exempel antioxidanter och andra skyddande ämnen) i livsmedel och möjligen även ämnen som vi idag inte känner till, gör det svårt att undersöka mer komplicerade samband med RCT.
Observationsstudier
I observationsstudier följer forskarna studiedeltagarna utan att deltagarna ändrar något för att de ingår i studien. Till exempel kan matvanorna hos en del av befolkningen studeras för att se om det finns ett samband mellan vissa matvanor och en sjukdom. Det är viktigt att vara uppmärksam på att denna typ av studier inte visar orsak-verkansamband. Det går alltså inte att säga helt säkert veta vad sambandet står för. I Livsmedelsverkets rapport skriver författarna att observationsstudier generellt har ett lägre bevisvärde än interventionsstudier, men att varje studie måste bedömas enskilt.
Det finns olika typer av observationsstudier, till exempel kohortstudier, fall-kontrollstudier och tvärsnittsstudier. En kohort definieras som en grupp människor som har en eller flera gemensamma egenskaper och som följs under en viss tid, vanligtvis flera år. Ett slumpmässigt urval av en del av befolkningen bjuds in att delta, exempelvis alla i en viss ålder i en region. Kohorten kan ge svar på om det finns ett statistiskt samband mellan nutritionsfaktorn och hälsoutfallet, men inte om nutritionsfaktorn är orsaken till hälsoutfallet, till exempel typ 2-diabetes.
I en fall-kontrollstudie ingår individer som fått en viss sjukdom (fall) och som matchas med personer i en kontrollgrupp som liknar fallen med avseende på till exempel ålder och kön. På sätt kan fallens matvanor innan de blev sjuka jämföras med kontrollgruppens matvanor.
I en tvärsnittsstudie mäts faktorer vid en och samma tidpunkt hos deltagarna, till exempel kan matvanor och vikt mätas som sedan relateras till varandra. Tvärsnittsstudier kan användas för att få kunskap om matvanorna i befolkningen. Nackdelen med denna typ av studier är att de inte ger någon information om riktningen på sambandet, det vill säga vad som är orsak respektive verkan.
Kostmönster
Livsmedelsverket skriver i rapporten att ett generellt problem inom nutritionsepidemiologin, där samband mellan matvanor och sjukdomsrisk studeras, är att det är svårt att skilja effekten av ett näringsämne från ett annat eftersom de finns i samma livsmedel. Genom att studera ett så kallat kostmönster kan helheten av matvanorna undersökas. Det finns olika metoder att undersöka kostmönster. Forskare kan skapa ett index som ger poäng beroende på hur väl ett kostmönster följs, till exempel medelhavskosten. Kostmönster kan också vara datadrivna. Då används en statistisk metod för att få fram kombinationer av livsmedel som deltagarna i en matvaneundersökning ofta äter. Sedan studerar forskarna sambandet mellan olika kostmönster och ett visst hälsoutfall.
Resultat från flera enskilda studier vägs samman
I en litteraturöversikt (review) vägs flera studier med liknande frågeställning samman och en samlad bedömning kan göras. Det kan finnas olika felkällor i studierna som ingår, men om resultaten ändå pekar åt samma håll ger det tyngd åt litteraturöversiktens slutsats.
En litteraturöversikt kan vara systematisk eller icke-systematisk. Livsmedelsverket skriver i rapporten att grunden för en värdering av det samlade bevisvärdet för ett samband mellan mat och hälsa är en systematisk litteraturöversikt (systematic review). En systematisk litteraturöversikt behöver ha en väl avgränsad frågeställning, till exempel intag av baljväxter och hjärt-och kärlsjukdom, medan en så kallad scoping review, ger en övergripande beskrivning av ett område.
I en systematisk litteraturöversikt ingår flera huvudmoment, till exempel en tydlig frågeställning, att urvalskriterier såsom studietyp och studielängd ska definieras och att inklusions- och exklusionskriterier för studierna ska redovisas. I översikten ska alla studierna som uppfyller urvalskriterierna vara med. Även en tydligt beskriven litteratursökning som anger söktermer och databaser och en värdering av studiekvaliteten av de ingående studierna ska ingå.
Några myndigheter, organisationer och nätverk har publicerat verktyg för att göra systematiska översikter, förbättra kvaliteten på rapportering av systematiska litteraturöversikter och bedöma om en litteraturöversikt är systematisk eller inte. Statens beredning för medicinsk och social utvärdering (SBU) har publicerat en metodbok som är tänkt att användas som ett praktiskt stöd för dem som ska genomföra en utvärdering.
Systematiska litteraturöversikter och meta-analyser värderas högt
Resultat från systematiska litteraturöversikter värderas generellt högt, men den ger inte samma information som meta-analyser.
I en meta-analys ingår resultat från enskilda studier med en likartad frågeställning. Därefter görs nya statistiska analyser och på så sätt vägs resultaten samman från alla ingående studier. Studierna som ingår i meta-analysen väljs ut på liknande sätt som i en systematisk översikt. Resultatet från meta-analyser värderas generellt mycket högt, men är beroende av kvaliteten på de ingående studierna.
Studiekvalitet
Med studiekvalitet menas kvalitet på vetenskaplig metod och att resultat från de ingående studierna ger svar på aktuell frågeställning. Följande är exempel på faktorer som bör beaktas när studiekvaliteten på de ingående studierna värderas: studiedesign, studiepopulation, studielängd, studiestorlek, hur kostdata beskrivs och samlas in, bortfall och statistiska analyser.
Bedöming av helheten
I rapporten skriver Livsmedelsverket att det samlade vetenskapliga underlaget för ett specifikt samband mellan en kostfaktor och ett hälsoutfall behöver analyseras utifrån studiekvalitet, samstämmighet i resultaten, resultatens allmängiltighet för den aktuella målgruppen, storleken på hälsoeffekten, osäkerhet i dataunderlaget och även andra aspekter kan vara aktuella.
Därefter kan man värdera det samlade bevisvärdet för om ett orsak-verkansamband finns mellan en kostfaktor och ett hälsoutfall. Det finns dessutom olika system för att gradera och visa vilken styrka det samlade bevisvärdet har.
Författarna skriver i rapporten att traditionellt har bevisvärdet för ett samband rangordnats efter studietyp, där randomiserade kontrollerade studier har värderats ha högre bevisvärde än kohort- och fall-kontrollstudier. Men rangordningen påverkas mycket av studiekvaliteten och hur generaliserbara resultaten är för den aktuella populationen.
Läs mer i Livsmedelsverkets rapport: Så arbetar Livsmedelsverket med vetenskapliga underlag inom nutritionsområdet
Klart med de första systematiska litteraturöversikterna för NNR2022
Uppdateringen av de nordiska näringsrekommendationerna, NNR2022, omfattar en rad systematiska litteraturöversikter inom vissa områden. Nu är det första urvalet gjort.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
NNR2022-kommittén har beslutat om de fem första områdena för systematiska litteraturöversikter, som ska ge en samlad bedömning av de samband man vill studera:
- Intag av växtbaserat protein hos barn – och tillväxt hos barn
- Intag av baljväxter – och hjärt- och kärlsjukdom och typ 2-diabetes
- Intag av växtbaserat protein hos vuxna – och hjärt- och kärlsjukdom och typ 2-diabetes
- Vitamin B12 och vitamin B12-status i riskgrupper
- Fettkvalitet och mental hälsa
Ytterligare fem områden kommer presenteras senare under 2021. Hur processen ser ut för att ta fram de prioriterade områdena för de systematiska litteraturöversikterna kommer att publiceras i Food & Nutrition Research.
NNR2022-kommittén arrangerar ett andra webbinarium om mat och hållbarhet den 25 maj. En inspelning av webbinariet kommer att finnas tillgänglig på projektets webbplats. Se också webbplatsen för mer information om NNR2022. Där läggs också alla utlysningar ut.
Gluten, celiaki och typ 1-diabetes – finns det något samband?
Typ 1-diabetes och celiaki (glutenintolerans) är två kroniska sjukdomar där det egna immunförsvaret bryter ner kroppsegna organ. Bägge dessa autoimmuna sjukdomar är ärftliga och har gemensamma gener på kromosom 6. Högriskgener kopplade till typ 1-diabetes och celiaki finns i 40 procent av den svenska befolkningen. Trots det kommer majoriteten av dessa individer aldrig att utveckla någon av sjukdomarna.
Idag pågår flera studier i Sverige, där forskarna söker svar på vad som kan göras för att minska riskerna hos barn som har ärftliga anlag att bli sjuka. Forskning pågår för att ta reda på om det finns ett samband mellan gluten i kosten – och utvecklingen av celiaki och typ 1-diabetes. Det handlar bland annat om när barnen ska börja äta gluten och om probiotika kan ha en positiv effekt. Klart är att samspelet är komplext, och kompliceras dessutom bland annat av alla virusinfektioner som drabbar tarmen.
>> text: Carin Andrén Aronsson, PhD, dietist, Enhetschef, Enheten för Diabetes och Celiaki, Kliniska vetenskaper, Lunds universitet, Malmö
Både typ 1-diabetes och celiaki är autoimmuna sjukdomar där immunförsvaret bryter ned kroppsegna organ. Vid typ 1-diabetes blir de langerhanska cellöarna i bukspottkörteln inflammerade vilket leder till att betacellerna förstörs och all insulinbildning upphör. Vid celiaki blir slemhinnan i tunntarmen inflammerad och tarmluddet försvinner vilket innebär minskat näringsupptag. Bägge sjukdomar har gemensamma så kallade HLA-gener (human leukocyte antigen) som sitter på kromosom 6. HLA är en vävnadstyp som är kopplad till människans immunsystem.
För celiaki avstannar den autoimmuna processen när man plockar bort gluten ur kosten. Gluten är ett samlingsnamn för olika typer av proteiner som finns i vete, råg och korn.
För typ 1-diabetes är antigenet, alltså det främmande ämne som framkallar en reaktion hos kroppen, ännu inte känt. Det finns flera möjliga kandidater varav en är insulin och andra är GAD65, IA-2 och ZnT8. Så kallade autoantikroppar mot dessa visar att betaceller som producerar insulin håller på att förstöras. Se mer om autoantikroppar i faktarutan sist i artikeln.
Individer med typ 1-diabetes har också en ökad risk för celiaki, med 5 till 10 procent ökad risk jämfört med 1 till 3 procent i befolkningen i stort.
Genetik
Den genetiska kopplingen finns i den del av arvsmassan (DNA) som reglerar immunförsvaret. Det finns en gemensam typ av HLA-gen, DR4-DQ8 och DR3-DQ2, som leder till ökad risk för både typ 1-diabetes och celiaki. En variant av denna gen, medför en ökad risk för att utveckla typ 1-diabetes och forskare har också identifierat genvarianten som innebär den allra högsta risken att utveckla typ 1-diabetes. Individer som är bärare av en annan variant av denna HLA-gen, har en högre risk för att utveckla celiaki och ytterligare en variant innebär den högsta risken att utveckla celiaki. Se mer om HLA-gener och risk att utveckla typ-1 diabetes och celiaki i faktarutan sist i artikeln.
Den multinationella TEDDY-studien (The Environmental Determinants of Diabetes in the Young) är en kohortstudie som samlar in data från barn med genetisk risk för typ 1-diabetes och celiaki i fyra länder -Finland, Tyskland, Sverige och USA. Av den framgår att omkring 20 procent av barn med gener som innebär den högsta risken för celiaki får celiaki före 10 års ålder.
Högriskgener kopplade till typ 1-diabetes och celiaki finns i 40 procent av den svenska befolkningen. Men – en majoritet av dessa individer kommer aldrig att utveckla någon av sjukdomarna. En hypotes är att det finns gemensamma miljöfaktorer som triggar igång alternativt skyddar från de bägge sjukdomarna. Faktorer som diskuterats bland forskare är upprepade virusinfektioner, förändringar i tarmflorans sammansättning, probiotika, gluten i kosten och D-vitaminstatus (se figur). Ett flertal av dessa faktorer påverkar direkt eller indirekt tarmens genomsläpplighet eller immunsystemet.

Figur. Genetisk predisposition och olika miljöfaktorer kan fungera som triggers (igångsättare) och mediators (förmedlare, möjliggörare) men även ha en skyddande inverkan och därmed på olika sätt bidra till risken att utveckla typ-1 diabetes och celiaki. Samspelet är komplext och forskning om flera faktorer pågår.
Glutenkonsumtion under graviditet
Ett flertal studier, både på djur och människa, har undersökt om mammans glutenkonsumtion under graviditeten påverkar barnets risk att senare utveckla typ 1-diabetes eller celiaki. Djurstudierna är främst gjorda på möss, och har visat att förekomsten av typ 1-diabetes minskade hos djurens avkomma om honorna fick en glutenfri kost under graviditeten (1, 2). Resultaten förklarades med att förändringar i tarmfloran ledde till att tarmen och bukspottkörteln blev mindre känsliga för inflammationer.
Glutenintag under graviditet har undersökts i observationsstudier på människor, och gett motstridiga resultat. Nyligen presenterade en dansk forskargrupp ett samband med högt glutenintag under graviditeten och ökad risk för typ 1-diabetes hos barnen (3). Barn till mammor som hade rapporterat ett högt glutenintag under graviditet hade dubbelt så stor risk att utveckla typ 1-diabetes, jämfört med barn till mammor med lågt glutenintag. Ett flertal tidigare studier har däremot inte kunnat visa på något samband mellan mammans glutenintag och barnets risk för typ 1-diabetes (4-6). Det spekuleras att ett högt glutenintag kan spegla matvanor som även formar mammans och därmed även det nyfödda spädbarnets tarmflora.
Det är känt att näringsinnehåll och sammansättning i bröstmjölken påverkas av mammans kost. Men kan bröstmjölkens sammansättning påverka barnets risk att senare i livet utveckla celiaki? Det finns ett fåtal studier – med motstridiga resultat. Den första studien kom 2015 och visade att mammans konsumtion av livsmedel som innehöll gluten (hur ofta) inte var associerad med risk för celiaki hos barnet (7). Däremot publicerades nyligen en norsk studie som faktiskt såg ett samband mellan högt glutenintag hos mamman under graviditet och ökad risk för att senare utveckla celiaki hos barnet (8). Det som också är intressant med denna studie är att en låg glutenkonsumtion och ett högt fiberintag verkade skyddande för barnet. Mekanismen bakom detta samband skulle kunna vara att ett högt fiberintag medför att högre nivåer av så kallade kortkedjiga fettsyror bildas i tarmen. Dessa gynnar fördelaktiga bakteriestammar med anti-inflammatoriska funktioner i tarmen. Det är ett komplext samspel mellan kosten, immunförsvarets utveckling, tarmflora och tarmens genomsläpplighet, och alla kanske på sitt sätt påverkar utvecklingen av typ 1-diabetes och celiaki.
Glutenkonsumtion under småbarnsåren
Ett flertal studier har undersökt sambandet mellan glutenkonsumtion och risk för typ 1-diabetes och celiaki. I inledande studier var det främst tidpunkten för glutenintroduktion och risk för sjukdom som intresserade forskarna. Även om en amerikansk studie (9) fann en ökad risk för typ 1-diabetes med tidig glutenintroduktion, före 3 månaders ålder, hos barn med ärftlig risk, har senare studier inte kunnat visa på resultat i samma riktning (10). Sambandet mellan glutenintag och typ 1-diabetes kommer huvudsakligen från observationsstudier. Det saknas ännu evidensbaserade data med randomiserade kliniska studier.
Det samma gäller för celiaki, där det tidigt identifierades ett ”window of opportunity” med rekommendationer att gluten borde introduceras i barnets kost mellan 4 och 6 månaders ålder för att minska risken för celiaki. Senare studier har dock inte kunnat visa på en skyddande inverkan, varken i randomiserade kliniska studier eller observationsstudier. Numera anses varken tidpunkt för introduktion av gluten eller amning kunna påverka risken att utveckla celiaki eller typ 1-diabetes. Den europeiska organisationen The European Society for Paediatric Gastroenterology Hepatology and Nutrition (ESPGHAN) rekommenderar idag att gluten kan introduceras till barnets kost samtidigt med annan fast föda, men tidigast från 4 månaders ålder (11). I december 2020 uppdaterade Livsmedelsverket de nationella råden, och rekommenderar att gluteninnehållande spannmål (vete, råg och korn) kan ingå i kosten från det att barnet börjar smaka på mat och att senast vid 12 månaders ålder bör gluteninnehållande spannmål ingå i kosten.
Glutenkonsumtion och risk för autoimmuna sjukdomar
Under de senaste åren har det kommit studier där mängden gluten i småbarnskosten, och risk för de två autoimmuna sjukdomarna har undersökts. Tre studier har undersökt glutenmängd och risk för typ 1-diabetes (6, 12, 13). Två av studierna är baserade på barn med en genetisk ökad risk för typ 1-diabetes, medan en norsk studie är baserad på normalbefolkningen. Även här är resultaten motstridiga. Två studier fann ett samband mellan högt glutenintag och ökad risk för typ 1-diabetes, medan en amerikansk studie inte fann något samband.
Förklaringen till skillnader i resultat kan vara att olika metoder använts. Det handlar om olika sätt att registrera kostintag – frekvensformulär eller kostregistrering – och val av studiepopulation – allmän befolkning eller högriskpopulation. Dessutom skiljer sig definition av så kallad endpoint, antingen diabetesdiagnos eller närvaro av autoantikroppar associerade med att de insulinproducerande betacellerna förstörs. Studierna har också olika uppföljningstid.
Forskarna förklarar sambandet mellan gluten och risk för typ 1-diabetes med att glutenproteiner fungerar som ett antigen och triggar igång en sjukdomsprocess som direkt eller indirekt ändrar tarmfloran och/eller främjar inflammation och ökad genomsläpplighet i tarmen. Tarmfloran är viktig för kroppens funktion, men också för hur immunsystemet mognar och fungerar i framtiden.
Resultat från TEDDY-studien visade att tarmfloran hos de barn som inte utvecklade autoantikroppar relaterade till typ 1-diabetes, hade en större andel tarmbakterier kopplade till omsättning och bildning av kortkedjiga fettsyror (14). Dessa fettsyror är tarmslemhinnans främsta energikälla och anses generellt fördelaktiga för hälsan. Upprepade mag-tarmvirusinfektioner ökar genomsläppligheten i tarmen vilket innebär en större genomsläpplighet av glutenproteinet, vilket leder till en autoimmun reaktion. Detta är speciellt intressant för sambandet glutenmängd och celiaki. På senare tid har ett antal nya studier visat en ökad risk för celiaki med högt glutenintag under småbarnsåren.
Under 2019 publicerades tre studier om glutenintag hos småbarn och risk att senare utveckla celiaki (15-17). Gemensamt för alla studier var att de kunde fastställa ett samband mellan ett högt glutenintag och ökad risk för celiaki. Det kan tyckas glädjande att tre stora studier, varav en multinationell studie, visar på resultat i samma riktning. Men det är svårt att tyda vad som innebär ett högt glutenintag hos små barn. Skillnaden är vilken kostundersökningsmetod, frekvensformulär eller kostregistrering, som använts, att kosten har mätts vid olika åldrar, och att barns matvanor ser olika ut i olika länder. Det är också svårt att definiera ett skadligt intag baserat enbart på observationsstudier. Nästa steg är att genomföra randomiserade kliniska studier med frågeställningar som har möjlighet att räta ut de frågetecken som återstår. Det är också viktigt att komma ihåg att två av studierna är baserade på barn med ärftlig risk att utveckla celiaki. Det ifrågasätts därför om kostråd för spädbarn ska baseras på fynd från en specifik grupp av barn.
Gluten, tarmvirus och tarmfloran
Det är tydligt att det inte enbart krävs en genetisk predisposition och ett högt glutenintag för att celiaki ska utvecklas. I data från TEDDY-studien kunde man visa att upprepade enterovirusinfektioner (enterovirus orsakar främst förkylningar) mellan 1 och 2 års ålder var associerade med en ökad risk att utveckla celiakirelaterade autoantikroppar (förstadium till celiaki) (18). Denna risk förstärktes hos de barn som samtidigt rapporterat ett högt glutenintag.
Nu ska den mest omfattande studien i sitt slag genomföras. Det handlar om 20 000 avföringsprover från barn i TEDDY-studien som ska analyseras för att ta reda på förekomsten av virus. Även tarmflorans sammansättning av godartade och mindre godartade bakterier ska analyseras. Syftet är att identifiera ett eller flera virus som fungerar som den trigger som krävs för att utlösa en infektion, som i sin tur leder till utveckling av celiaki. Prover från barn som diagnostiserats med celiaki kommer att jämföras med friska kontroller. Proverna samlades in regelbundet från 4 månaders ålder för att ta reda på förekomst av arvsmassa från olika virus, och tarmflorans sammansättning. Information om glutenkonsumtion under motsvarande tidsperiod kommer sedan att inkluderas i de statistiska analyserna. Studien, som är finansierad av National Institutes of Health (NIH), kommer förhoppningsvis kunna svara på frågan om och hur virusinfektioner, kost och tarmflora är involverade och påverkar utvecklingen av celiaki hos genetiskt predisponerade barn.
Studier på gång
Inom Center för Autoimmunitet och Prevention (CAP) vid Institutionen för kliniska vetenskaper, Lunds universitet (Malmö) bedrivs just nu ett antal studier som undersöker sambandet mellan just glutenintag, celiaki och typ 1-diabetes. Baserat på kunskapen om att höga mängder gluten under småbarnsåren ökar risken för celiaki, startade 2019 en studie som heter PreCiSe (Prevention Celiaki i Skåne) med syfte att studera hur man kan förhindra att barn med hög ärftlig risk utvecklar celiaki. Nyfödda barn med en HLA-gen som innebär risk för att utveckla celiaki, fördelades slumpmässigt i tre grupper. För den första gruppen gällde glutenfri kost fram till 3 års ålder och därefter långsamt introducera gluten till kosten. I den andra fick barnen äta familjens vanliga kost men med ett dagligt intag av ett kosttillskott som består av två olika probiotikastammar. I den tredje gruppen fick barnen äta familjens vanliga kost, men med ett dagligt intag av ett placebotillskott.
Hypotesen är att undvika gluten under de första åren då barn utsätts för upprepade mag-tarmvirusinfektioner, vilket i sin tur ökar genomsläppligheten av gluten i tarmen, för att på så sätt kunna minska risken för risk-individer att senare drabbas av celiaki. Ett dagligt kosttillskott av probiotika skulle kunna vara ett annat sätt att minska genomsläppligheten i tarmen och reglera immunförsvaret och därmed minska risken för celiaki.
Ytterligare en studie som ligger i startgroparna är GRAIN-studien (Glutenreduktion till barn under 5 år och risk för celiaki). Barn med genetisk risk äter här en glutenreducerad kost upp till 5 års ålder och följs i ytterligare 5 år. I två tidigare studier har nivåer av glutenintag som ökar risken att utveckla celiaki hos barn med förhöjd ärftlig risk identifierats. Hypotesen är att ett begränsat glutenintag under småbarnsåren hos genetiskt predisponerade barn kan vara ett sätt att minska risken att utveckla celiaki-relaterade autoantikroppar och därmed även celiaki. Studiedeltagarna kommer även att screenas regelbundet för autoantikroppar associerade med typ 1-diabetes. Studien bör därför även kunna svara på om en glutenreducerad kost påverkar diabetesrelaterade autoantikroppar och i förlängningen typ 1-diabetes.
Samtidigt slutförs just nu TEFA-studien (TEDDY Family Prevention) med barn och vuxna som utvecklat minst två autoantikroppar mot betacellerna, men ännu inte fått symtom på diabetes. Syftet med studien är att ta reda på om en glutenfri kost, jämfört med en normalkost, bevarar betacellernas funktion. Deltagarna fördelas slumpvis till en grupp med en glutenfri kost, och till en grupp som äter som vanligt under 18 månader. Preliminära data förväntas inom det närmsta året.
Sammanfattning
Samspelet mellan gluten i kosten, immunsystemet, tarmfloran, och tarmens genomsläpplighet är komplext. Till det kan läggas upprepade virusinfektioner som drabbar tarmen. Alla dessa faktorer kan potentiellt påverka risken for att utveckla typ 1-diabetes och celiaki – eller båda. Alla pusselbitar är långt ifrån på plats, men forskningen nu har goda förutsättningar att lösa gåtan med varför barn med förhöjd ärftlig risk drabbas av dessa förödande och livslånga sjukdomar.
Inga jävsförhållanden.
Fakta om autoantikroppar
För typ 1-diabetes är antigenet, det främmande ämne som framkallar en reaktion hos kroppen, ännu inte känt. Kandidater är insulin, GAD65 (glutaminsyradekarboxylas), IA-2 (islet antigen 2) och ZnT8 ((zinktransportör 8).
Autoantikroppar mot dessa antigen är markörer för att de insulinproducerande betacellerna i bukspottskörteln håller på att förstöras.
Fakta om genetiken bakom typ 1-diabetes och celiaki
Den gemensamma typen av HLA-gen, DR4-DQ8 och DR3-DQ2, leder till ökad risk för både typ 1-diabetes och celiaki. Dessa HLA-typer är specifika delar av kromosom 6. HLA-molekylerna är immunsystemets viktigaste informationsmolekyler.
Individer med genvariationen, HLA DR4-DQ8, har en högre risk för att utveckla typ 1-diabetes, och HLA DR3-DQ2/DR4-DQ8 innebär den högsta risken för typ 1-diabetes.
Individer med genvariationen, HLA DR3-DQ2 har en högre risk för att utveckla celiaki, och HLA DR3-DQ2/DR3-DQ2 innebär den högsta risken att utveckla celiaki.
Omkring 95 procent av patienter med celiaki bär på DR3-DQ2, medan resten bär på DR4-DQ8.
Personer som inte har HLA-typerna DQ2 och DQ8 kan inte utveckla celiaki.
Referenser
1. Hansen CH, Krych L, Buschard K, et al. A maternal gluten-free diet reduces inflammation and diabetes incidence in the offspring of NOD mice. Diabetes. 2014;63(8):2821-2832.
2. Antvorskov JC, Josefsen K, Haupt-Jorgensen M, Fundova P, Funda DP, Buschard K. Gluten-Free Diet Only during Pregnancy Efficiently Prevents Diabetes in NOD Mouse Offspring. J Diabetes Res. 2016;2016:3047574.
3. Antvorskov JC, Halldorsson TI, Josefsen K, et al. Association between maternal gluten intake and type 1 diabetes in offspring: national prospective cohort study in Denmark. BMJ. 2018;362:k3547.
4. Lamb MM, Myers MA, Barriga K, Zimmet PZ, Rewers M, Norris JM. Maternal diet during pregnancy and islet autoimmunity in offspring. Pediatr Diabetes. 2008;9(2):135-141.
5. Virtanen SM, Uusitalo L, Kenward MG, et al. Maternal food consumption during pregnancy and risk of advanced beta-cell autoimmunity in the offspring. Pediatr Diabetes. 2011;12(2):95-99.
6. Lund-Blix NA, Tapia G, Mårild K, et al. Maternal and child gluten intake and association with type 1 diabetes: The Norwegian Mother and Child Cohort Study. PLoS medicine. 2020;17(3):e1003032.
7. Uusitalo U, Lee HS, Aronsson CA, et al. Gluten consumption during late pregnancy and risk of celiac disease in the offspring: the TEDDY birth cohort. The American journal of clinical nutrition. 2015;102(5):1216-1221.
8. Lund-Blix NA, Tapia G, Mårild K, et al. Maternal fibre and gluten intake during pregnancy and risk of childhood celiac disease: the MoBa study. Scientific Reports. 2020;10(1):16439.
9. Norris JM, Barriga K, Klingensmith G, et al. Timing of Initial Cereal Exposure in Infancy and Risk of Islet Autoimmunity. Jama. 2003;290(13):1713-1720.
10. Pieścik-Lech M, Chmielewska A, Shamir R, Szajewska H. Systematic Review: Early Infant Feeding and the Risk of Type 1 Diabetes. Journal of pediatric gastroenterology and nutrition. 2017;64(3):454-459.
11. Fewtrell M, Bronsky J, Campoy C, et al. Complementary Feeding: A Position Paper by the European Society for Paediatric Gastroenterology, Hepatology, and Nutrition (ESPGHAN) Committee on Nutrition. Journal of pediatric gastroenterology and nutrition. 2017;64(1):119-132.
12. Lund-Blix NA, Dong F, Marild K, et al. Gluten Intake and Risk of Islet Autoimmunity and Progression to Type 1 Diabetes in Children at Increased Risk of the Disease: The Diabetes Autoimmunity Study in the Young (DAISY). Diabetes care. 2019;42(5):789-796.
13. Hakola L, Miettinen ME, Syrjala E, et al. Association of Cereal, Gluten, and Dietary Fiber Intake With Islet Autoimmunity and Type 1 Diabetes. JAMA pediatrics. 2019.
14. Vatanen T, Franzosa EA, Schwager R, et al. The human gut microbiome in early-onset type 1 diabetes from the TEDDY study. Nature. 2018;562(7728):589-594.
15. Lund-Blix NA, Marild K, Tapia G, Norris JM, Stene LC, Stordal K. Gluten Intake in Early Childhood and Risk of Celiac Disease in Childhood: A Nationwide Cohort Study. Am J Gastroenterol. 2019;114(8):1299-1306.
16. Marild K, Dong F, Lund-Blix NA, et al. Gluten Intake and Risk of Celiac Disease: Long-Term Follow-up of an At-Risk Birth Cohort. Am J Gastroenterol. 2019;114(8):1307-1314.
17. Andren Aronsson C, Lee HS, Hard Af Segerstad EM, et al. Association of Gluten Intake During the First 5 Years of Life With Incidence of Celiac Disease Autoimmunity and Celiac Disease Among Children at Increased Risk. Jama. 2019;322(6):514-523.
18. Lindfors K, Lin J, Lee HS, et al. Metagenomics of the faecal virome indicate a cumulative effect of enterovirus and gluten amount on the risk of coeliac disease autoimmunity in genetically at risk children: the TEDDY study. Gut. 2019.
”Låt varje tugga räknas” – de nya amerikanska kostråden är nu klara
Uppdateringen av de amerikanska kostråden är klar och den nionde utgåvan av ”Dietary Guidelines for Americans, 2020-2025”, är publicerad. Råden fokuserar på kostmönster och riktar sig till hela den amerikanska befolkningen och omfattar för första gången alla åldrar. Det är inga stora förändringar i råden jämfört med den förra utgåvan.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
Den nya utgåvan har underrubriken ”Make Every Bite Count With the Dietary Guidelines” och är som tidigare vetenskapligt baserade råd om vad man ska äta och dricka för att tillgodose näringsbehovet, främja hälsan och minska risken för kroniska sjukdomar, som till exempel hjärt- och kärlsjukdomar, typ 2-diabetes och fetma.
Följande tre förändringar lyfts särskilt fram:
· Den nya utgåvan är inriktad på att hela den amerikanska befolkningen, oberoende av hälsostatus, kan uppnå fördelar med ett hälsosamt kostmönster.
· Fokus på kostmönster. Kostmönster är den sammanlagda effekten av intag av livsmedel och näringsämnen på hälsan.
· I denna utgåva finns råd till alla åldersgrupper, från spädbarn till äldre. I tidigare utgåvor har inte de yngsta ingått.
Kostråden i korthet:
1. Följ ett hälsosamt kostmönster genom hela livet. Det är aldrig för tidigt eller för sent att börja äta hälsosamt. Det gäller både ung och gammal.
2. Råden ger en ram som kan anpassas efter individens näringsbehov, kulturella traditioner och ekonomiska situation.
3. Ett hälsosamt kostmönster innehåller näringsrika livsmedel som ger vitaminer och mineraler och andra nyttiga ämnen, och har inget eller lite tillsatt socker, begränsat med mättat fett och salt, och inte för mycket energi.
Följande livsmedelsgrupper ingår i ett hälsosamt kostmönster: alla sorters grönsaker, frukt (gärna hela frukter), spannmålsprodukter (minst hälften fullkorn), mejeriprodukter, proteinrika livsmedel (till exempel magert kött, fisk- och skaldjur, bönor, nötter och sojaprodukter) och oljor.
4. Begränsa mat och drycker med ett högt innehåll av tillsatt socker, mättat fett och salt, och begränsa intaget av alkoholhaltiga drycker. Ett hälsosamt kostmönster har inte mycket utrymme för tillsatt socker, mättat fett, salt eller alkoholhaltiga drycker.
· Intaget av tillsatt socker bör vara mindre än 10 procent av det dagliga energiintaget. Barn under 2 år ska helt undvika mat och drycker med tillsatt socker.
· Intaget av mättat fett bör vara mindre än 10 procent av det dagliga energiintaget (från 2 års ålder).
· Intaget av natrium bör vara mindre än 2300 mg natrium per dag och ännu mindre för barn yngre än 14 år.
Många vetenskapliga artiklar har publicerats och sammanställts inom området sedan förra utgåvan och dessa har stärkt sambandet mellan mat och hälsa, men sammantaget innehåller ”Dietary Guidelines for Americans, 2020-2025” inga stora förändringar.
I den nya utgåvan påpekar man också att en stor del av befolkningen inte äter hälsosamt. Forskning visar att 75 procent av den amerikanska befolkningen har ett kostmönster med för lite grönsaker, frukt och mejeriprodukter. Långt över hälften, 63 procent, äter för mycket tillsatt socker och 77 procent för mycket mättat fett.
För att äta hälsosamt krävs det att 85 procent av den dagliga energin utgörs av näringsrika livsmedel som ger vitaminer och mineraler, och andra nyttiga ämnen enligt ”Dietary Guidelines for Americans”. Endast 15 procent av det dagliga energiintaget kan vara livsmedel som innehåller mycket mättat fett eller tillsatt socker. De nya kostråden noterar också att även om varje individ själv bestämmer vad och hur mycket hen vill äta, har myndigheter, hälso- och sjukvård, organisationer och företag en roll i att stödja individer och familjer i att säkerställa att alla människor har tillgång till hälsosam mat.
Se följande länkar till infografik och filmklipp om ”Dietary Guidelines for Americans, 2020-2025”. Se även American Society for Nutritions webinar series: Understanding and Using the New 2020 Dietary Guidelines for Americans.
Fakta om Dietary Guidelines for Americans, DGA
The Dietary Guidelines for Americans, uppdateras vart femte år sedan 1980 av US Department of Agriculture (USDA) och Health and Human Services (HHS).
”Dietary Guidelines for Americans, 2020-2025” bygger på 2015 års upplaga med revideringar som baseras på 2020 års vetenskapliga rapport från Dietary Guidelines Advisory Committee.
Så påverkar kostfibrer mage och tarmar hos äldre personer
När vi åldras förändras hela kroppen och problem med mage och tarmar är vanligt hos dem som bor på senior- och vårdboenden. Vår forskning visar också att magproblemen är omfattande även hos äldre personer som inte har någon kontakt med vården.
Resultat från våra studier har visat att kostfibrer kan stärka tarmbarriären. En studie visade att magproblem var kopplade till en mindre mängd kostfibrer i maten.
Nu krävs mer specialinriktad forskning för att ta reda på hur kostfibrer exakt påverkar tarmen och hur de kan användas för att minska åldersrelaterade magproblem. För trots det stora antalet äldre personer med magproblem finns idag lite forskning.
>> text: Ida Schoultz, docent i biomedicin, Institutionen för medicinska vetenskaper, Örebro universitet, Örebro.
Det här händer i magen när vi åldras
Mag- och tarmkanalens huvuduppgift är att spjälka maten, ta upp näringsämnen och förse kroppen med näring och vatten. Denna process är helt beroende av rörlighet i tarmen – och en god produktion av enzymer och bakterier i tarmfloran som kan bryta ned maten.
När vi åldras får flera organ i mag- och tarmkanalen en försämrad funktion (se figur 1).
Smaken förändras samtidigt som många äldre får svårare att tugga och blir torra i munnen (1). Förändringarna i munnen leder ofta till att äldre personer undviker viss sorts mat vilket kan resultera i ett minskat näringsintag, som i sin tur kan utvecklas till en försämrad nutritionsstatus (1).
Förändringar i kosten kan också påverka tarmflorans sammansättning och funktion. Det gäller särskilt kostfibrer som fungerar som näring för tarmfloran och de bakterier som producerar kortkedjiga fettsyror, som smörsyra. Smörsyra är en stor näringskälla för tjocktarmens celler och experimentella studier tyder på att de är viktiga för en god tarmfunktion.
I matstrupen och tjocktarmen förändras också rörligheten vilket leder till att det tar längre tid för maten att passera genom mag- och tarmkanalen (2). Studier visar att tiden som maten befinner sig i tarmen påverkar tarmflorans sammansättning och även dess aktivitet och funktion (3). Åldrandet är förknippat med förändringar i tarmfloran, men man har inte kunnat identifiera förändringar som sker generellt för alla äldre, utan enbart de individuella förändringarna. Även om man ofta ser en förändring i mångfalden av bakterier som har en dokumenterad hälsofrämjande effekt på individen.
Forskningen har hittills använt olika metoder vilket gör det svårt att hitta gemensamma nämnare för hur tarmfloran förändras med åldern (4). Även om åldrandeprocessen är förknippad med en förändrad tarmflora, är det viktigt att komma ihåg att bakterier lätt anpassar sig och kan anta nya funktioner. Därför blir det extra viktigt att framtida studier särskilt kartlägger hur funktionen och aktiviteten hos tarmfloran förändras med åldrandet.

Figur 1. Hur vi åldras påverkas av flera olika faktorer: arv, livsstil, boendesituation, sjukdomar och mediciner. Det innebär att åldrandet är mycket individuellt. Åldrandeprocessen är också förknippad med flera förändringar i kroppen som påverkar mag- och tarmkanalen.
Utsöndringen av enzymer som hjälper till att bryta ned maten är viktigt för matspjälkningen. Nedbrytningen regleras genom ett komplext samspel, där både hormoner och faktorer som påverkar nervsystemet ingår. Forskningen visar att äldre friska personer har en lägre nivå av enzymer som pepsin, lipas och amylas i magsäcken som alla är viktiga i matspjälkningsprocessen (5). Däremot har man inte kunnat identifiera en förändring i utsöndringen av gallsyror hos äldre, vilka också är betydelsefulla i matspjälkningsprocessen. Men området är fortfarande till vissa delar outforskat och alla åldersrelaterade förändringar som sker i mag- och tarmkanalen har ännu inte dokumenterats på detaljnivå.
Förutom att matspjälkningsprocessen ska fungera är det också viktigt med en välfungerande mag- och tarmbarriär som skyddar mot främmande ämnen i maten, till exempel oönskade bakterier och toxiner. Endast näringsämnen och vatten bör passera, medan främmande ämnen ska transporteras ut ur kroppen. Än så länge finns få studier om hur tarmens barriärfunktion förändras när vi åldras. De få studier som finns visar att tarmens barriärfunktion inte verkar försämras i och med att vi åldras (6, 7). Men det behövs mer forskning för att kunna kartlägga om tarmen blir känsligare mot olika faktorer som vi vet påverkar tarmens barriärfunktion.
Med stigande ålder ökar användning av mediciner, samtidigt som kosten förändras. Fler får också olika sjukdomar som diabetes och hjärt- och kärlsjukdomar. Alla dessa är faktorer som påverkar mag- och tarmbarriären. Men det krävs mer forskning om hur dessa interagerar med tarmen och om tarmen hos äldre personer är mer känslig.
Åldrandet är dessutom förknippat med en låggradig inflammation och förändringar i immunförsvaret. Hur detta påverkar mag- och tarmkanalens funktion är inte känt.
Själva åldrandeprocessen i sig påverkas också av flera faktorer: arvsanlag, livsstil (kost och rökning), mediciner och sjukdomar. Hur mag- och tarmkanalen påverkas av åldrandeprocessen är därför väldigt individuellt.
Fler äldre lider av magproblem
Idag vet vi att magproblem är vanligt förekommande på senior- och vårdboenden (8). I en av våra studier fann vi dessutom att magproblem är ett stort bekymmer bland äldre personer som ännu inte är i behov av vård (9). Så många som 65 procent av de 250 individerna över 65 år som deltog i vår studie, led av någon form av magproblem, från milda till svåra besvär. Dessutom upplevde ofta deltagarna fler än ett symptom från magen, som också många gånger var svåra att skilja från varandra.
Våra preliminära resultat visar också att magproblemen hos äldre individer är förknippade med ett minskat intag av fibrer och protein – och kopplade till en ökad nivå av ångest och depression. Vi började därför intressera oss för orsakerna bakom magproblemen och varför så många äldre personer upplever problem med magen.
Det komplexa mag- och tarmsystemet
Tarmen har en mycket komplex uppgift. Den ska fungera som en barriär och inte släppa in främmande ämnen som bakterier eller toxiska ämnen som vi får i oss via maten. Samtidigt ska den ta upp näring och förse kroppen med vatten (10). Vid svårare inflammatorisk tarmsjukdom, vet vi att tarmens barriärfunktion är förändrad och sjukdomen är förknippad med en ökad genomsläpplighet i tarmen (11). Det innebär att främmande ämnen som bakterier och toxiska ämnen, kan ta sig in i kroppen i högre utsträckning, vilket bidrar till inflammation i tarmen (10).
Om en förändrad barriärfunktion med ökad genomsläpplighet också är central hos äldre personer med magproblem öppnar det upp för nya möjligheter. Behandlingar skulle kunna stärka tarmen och därmed eventuellt dämpa de magproblem som äldre ofta drabbas av.
Vi kunde nyligen visa att tarmbarriären är förändrad hos äldre individer som lider av magproblem jämfört med en yngre kontrollgrupp (12). Med den så kallade Ussingkammartekniken (10) studerade vi en vävnadsbit från tarmen, stor som ett knappnålshuvud, och fann olika markörer på att tarmen påverkats (se figur 2).

Figur 2. Ussingkammartekniken är idag den mest avancerade metoden för att mäta tarmens barriärfunktion och dess genomsläpplighetsförmåga. Genom att montera en vävnadsbit, en tarmbiopsi, i Ussingkammaren kan man med olika markörer få en uppfattning om tarmen har förändrad genomsläpplighetsförmåga. Tekniken mäter också elektrofysiologiska parametrar som till exempel resistansen, det vill säga motståndet, i tarmen. En minskad resistans kan betyda att tarmbarriären är försämrad.
Så påverkar kostfibrer tarmens barriärfunktion
Ett av de fynd som vi fann särskilt intressant var kopplingen mellan minskat fiberintag och magproblem även hos äldre individer som bor i eget boende, och som ofta uppvisar mildare symptom från magen.
I en parallell studie kunde vi konstatera att friska äldre personer som är aktiva orienterare hade en högre andel av en bakterie kallad Faecalibacterium prausnitzii som är förknippad med en kost rik på kostfibrer (13). Detta är fibrer som inte bryts ned i mag- och tarmkanalen. De fungerar istället som näring till bakterier i tarmfloran som bidrar till att smörsyra bildas – en av de främsta näringskällorna för tjocktarmens celler. Vi ville därför gå vidare och studera om ett tillskott av kostfibrer skulle kunna stärka mag- och tarmbarriären hos äldre och göra den mer tålig mot till exempel mediciner. Vi ville också se om kostfibrerna kunde lindra de magproblem som vi sett att äldre ofta lider av.
Vi genomförde därför en klinisk studie där deltagarna, 65 år eller äldre, slumpmässigt delades in i tre grupper. Två grupper fick under sex veckor äta kostfiber från antingen vete eller havre. Den tredje gruppen fick äta en verkningslös substans, placebo. Vi undersökte framför allt om kosttillskott med kostfibrer skulle kunna stärka tarmens barriärfunktion och göra den mer motståndskraftig mot de negativa effekter som vi vet antiinflammatoriska ämnen har på tarmen och som leder till en ökad genomsläpplighet i tarmen.
Vår studie fann inte att tillskott av kostfibrer skulle kunna stärka tarmen mot dessa läkemedel (14). Inte heller kunde vi se att milda magproblem hos deltagarna minskade efter medverkan i studien. Detta trots att majoriteten av studiedeltagarna åt mindre fibrer innan studiestart än vad Livsmedelsverket idag rekommenderar.
I den här studien hade vi inte möjlighet att ingående studera tarmbarriären genom Ussingkammartekniken utan vi använde oss av ett sockertest. Denna metod har använts sedan de allra första studierna av tarmbarriären genomfördes och innebär att studiedeltagarna dricker en lösning bestående av olika sockerarter. Dessa sockerarter bryts inte ned i kroppen utan tas i stället upp i olika delar av tarmen, i tjocktarmen eller tunntarmen.
Genom att mäta nivåerna av sockerarterna i urinen kan vi få en översiktsbild av tarmens genomsläpplighet (10). Den kan tala om för oss var i tarmen det finns en förändrad barriärfunktion och om den påverkas av intag av kostfibrer. Metoden ger däremot inte några detaljerade kunskaper om de mekanismer som ligger bakom den förändrade barriärfunktionen, eller hur kostfibrer påverkar tarmen direkt. För att bättre förstå om kostfibrer har förmågan att dämpa åldersrelaterade magproblem behövs mer riktade studier på grupper av äldre som lider av mer specifika och likartade symptom. Detta eftersom äldre som grupp är mycket heterogen.
Kostfibrer kan påverka tarmen direkt
För att ytterligare förstå hur kostfibrer påverkar mag- och tarmbarriären gick vi vidare i våra studier. Vi använde oss återigen av Ussingkammartekniken för att studera de direkta effekterna av kostfibrer på tarmen och det tunna cellager, epitelet, som klär insidan av den.
En liten vävnadsbit från tjocktarmen hos äldre personer som led av förstoppning och/eller diarré, monterades i Ussingkammaren. I vår studie var vi intresserade av att förstå om, och i sådana fall hur, kostfibrerna påverkar epitelet i tarmen direkt. Men vi ville också ta reda på om kostfibrer skulle kunna stärka tarmen och göra den mer motståndskraftig mot substanser som vi vet ökar vid stress och ångest hos äldre.
Det handlar om ökade nivåer av så kallade kortikotropin-frisättande hormon, en substans som har visat sig bidra till en förändrad mag- och tarmbarriär och är förknippad med en ökad genomsläpplighet i tarmen. För att efterlikna det som händer i kroppen vid stress och ångest använde vi oss av en kemikalie som delvis ger samma effekter som kortikotropin-frisättande hormon. Kemikalien leder precis som kortikotropin-frisättande hormon till frisättning av mastcellernas granule.
Mastceller finns i bindväven och förekommer i stor mängd runt blodkärlen i tarmen. De är en typ av immuncell, granulocyt, som bär på ett granule. Granule är små korn fyllda med inflammatoriska substanser, till exempel histamin. När mastcellerna frisätts leder det till att blodkärlen vidgar sig och till en ökad genomsläpplighet i tarmen. I vår studie var vi intresserade av att se om ett tillägg av kostfibrer direkt till vävnadsbiten från tjocktarmen skulle kunna förhindra den ökade genomsläppligheten som normalt sker i samband med frisättning av mastcellernas granule.
I studien fann vi att tillägg av en typ av kostfiber, beta-glukan, utvunnen ur jästsvamp gjorde tarmen mer tålig och genomsläppligheten minskade jämfört med utan behandling av kostfibern (12). Detta visar att kostfibrer interagerar direkt med tarmepitelet och har förmågan att stärka tarmen i vissa situationer. Men för att kunna dra slutsatsen att kostfibrer kan hjälpa mot magproblem kopplade till psykisk stress som depression och ångest, krävs särskilt riktade studier där personer som upplever psykisk stress och magsymptom deltar.
Det intressanta är att vi nu vet att kostfibrer kan interagera direkt med tarmen och ge direkta effekter på tarmens barriärfunktion. Den främsta effekten av kostfibrer på tarmen är att förändra tarmflorans sammansättning. Den kunskapen innebär att framtida studier bör omfatta mer mekanistiska studier av mag- och tarmbarriären till exempel genom att studera vävnadsbitar för att förstå exakt hur kostfibrer påverkar tarmen och hur de kan användas för att eventuellt lindra åldersrelaterade magproblem.
Ida Schoultzs forskning kan följas i sociala medier via @magperspektiv.
Inga jävsförhållanden. Delar av forskningen finansierades av anslag från Bo Rydins stiftelse till Ida Schoultz.
Referenser
1. Morley JE. The aging gut: physiology. Clin Geriatr Med 2007;23(4):757-67.
2. Bai JPF., et al. Literature Review of Gastrointestinal Physiology in the Elderly, in Pediatric Patients, and in Patients with Gastrointestinal Diseases. J Pharm Sci 2016;105(2):476-83.
3. Tottey W., et al. Colonic Transit Time Is a Driven Force of the Gut Microbiota Composition and Metabolism: In Vitro Evidence. J Neurogastroenterol Motil 2017;23(1):124-34.
4. An R., et al. Age-dependent changes in GI physiology and microbiota: time to reconsider? Gut 2018;67(12):2213-22.
5. Rémond D., et al. Understanding the gastrointestinal tract of the elderly to develop dietary solutions that prevent malnutrition. Oncotarget 2015;6(16):13858-98.
6. Wilms E., et al. Intestinal barrier function is maintained with aging – a comprehensive study in healthy subjects and irritable bowel syndrome patients. Sci Rep 2020;10(1):475.
7. Valentini L., et al. Small intestinal permeability in older adults. Physiol Rep 2014;2(4):e00281.
8. Costilla VC., et al. Constipation in adults: diagnosis and management. Curr Treat Options Gastroenterol 2014;12(3):310-21.
9. Fart F., et al. Gut health, nutrient intake and well-being in community-dwelling older adults. Preprint. MedRxiv 2019:2019.12.16.19015008. Doi: 10.1101/2019.12.16.19015008.
10. Schoultz I., Keita ÅV. The Intestinal Barrier and Current Techniques for the Assessment of Gut Permeability. Cells 2020;9(8):1909.
11. Schoultz I., Keita ÅV. Cellular and Molecular Therapeutic Targets in Inflammatory Bowel Disease-Focusing on Intestinal Barrier Function. Cells 2019;8(2):193.
12. Ganda Mall JP., et al. Differential effects of dietary fibres on colonic barrier function in elderly individuals with gastrointestinal symptoms. Sci Rep 2018;8(1):13404.
13. Fart F., et al. Differences in Gut Microbiome Composition between Senior Orienteering Athletes and Community-Dwelling Older Adults. Nutrients 2020;12(9):2610.
14. Ganda Mall J-P., et al. Effects of Dietary Fibres on Acute Indomethacin-Induced Intestinal Hyperpermeability in the Elderly: A Randomised Placebo Controlled Parallel Clinical Trial. Nutrients 2020;12(7).
Hållbarhet ställer nya krav på näringsrekommendationer
Referat
Klimatpåverkan, biologisk mångfald, vatten- och markanvändning, transporter samt sociala och ekonomiska aspekter – det är några avgörande faktorer för ett hållbart matsystem. Arbetet med kommande upplaga av de nordiska näringsrekommendationerna, NNR2022, pågår och det finns en tydlig ambition att integrera hållbarhet i näringsrekommendationerna.
>>text: Kajsa Asp Jonson, leg dietist, journalist, nutritionsfakta.se
Som en start på arbetet med att integrera hållbarhet i NNR2022 arrangerades ett webbinarium den 24 september 2020. Rune Blomhoff som projektleder revideringen av NNR, var värd för seminariet som finns tillgängligt via hemsidan.
Per Fredrik Pharo leder arbetet med Norway’s International Climate and Forest Initiative och har ansvarat för en global rapport från Food and Land Use Coalition (FOLU). Han inledde med att ge en översiktsbild: Det globala matsystemet har utvecklats snabbt och orsakar 30 procent av klimatförändringarna. Konsekvenserna är omfattande, både för miljön och för människan. Det finns många utmaningar men utveckling, biologisk mångfald och matsäkerhet går enligt Per Fredrik Pharo att förena med hälsa och hållbarhet. Målet är att skydda miljön och reparera de skador som redan uppstått.
Andelen animaliskt protein – framför allt nötkött som produceras storskaligt i Sydamerika – behöver minska och ersättas med marina och växtbaserade proteinkällor. Uppmaningen från Per Fredrik Pharo är att beslutsfattare, producenter, jordbrukare och konsumenter behöver ta ett större ansvar för miljö och hälsa. Utveckling av lokal matproduktion ställer krav på infrastrukturen, både den som avser transport av till exempel skördar och varor, och den digitala infrastrukturen. Levnadsvillkor för kvinnor och flickor behöver prioriteras – i vissa områden är detta helt nödvändigt för ekonomisk och social utveckling avslutade Per Fredrik Pharo.
Sverige först ut
Anna-Karin Johansson, som arbetar med miljöfrågor och hållbarhet vid Livsmedelsverket i Uppsala, berättade om erfarenheter av att inkludera hållbarhetsaspekter i näringsrekommendationerna. Sverige var först och har kommit långt. Men matvanorna är en betydande källa till ohälsa och mer behöver göras för att bekämpa under- och felnäring och ta ansvar för konsumtion, klimat och biologisk mångfald. Även tillgången till vatten är ett sårbart område påpekade Anna-Karin Johansson.
Många av de globala hållbarhetsmålen innefattar mat och nutrition. Kostråden utgår ifrån sex av målen, till exempel minskad klimatpåverkan, varierat jordbrukslandskap och ökad biologisk mångfald på land och i sjöar och hav. Konsumtionsmönster och matproduktion behöver förändras för att nå generationsmålet, det vill säga riktningen för vad som måste göras för att på ett ansvarsfullt sätt kunna lämna över till nästa generation. Läs mer i Naturvårdsverkets Fördjupad utvärdering av miljömålen 2019.
Den vetenskapliga förankringen utgör grunden för näringsrekommendationer och kostråd. Samma höga evidenskrav behöver gälla hållbarhetsaspekterna och det är viktigt att inte generalisera, miljöpåverkan kan vara väldigt olika påpekade Anna-Karin Johansson. På global nivå har kött- och mjölkproduktion en kraftig negativ påverkan på biodiversitet medan betande djur i Sverige bidrar till mångfald av djur och växtlighet – och till öppna landskap. Även råden kring frukt och grönsaker behöver specificeras enligt Anna-Karin Johansson.
Konceptet ”Hitta ditt sätt” från Livsmedelsverket grundar sig i NNR2012 och har enkla huvudbudskap: Ät grönare, ät lagom, var aktiv. Råden har tagit hänsyn till matvanor, miljö, och risk- och nyttovärdering. Här finns också ett konsumentperspektiv.
Perspektiv från andra länder
Forskare från Nederländerna, Frankrike och Storbritannien gav utifrån sina erfarenheter ett europeiskt perspektiv.
Corné van Dooren, The Netherlands Nutrition Centre, berättade om Sustainable Nutrient Rich Foods-index (SNRF) som kombinerar näringstäthet och klimatpåverkan och som ligger till grund för rekommendationerna i Nederländerna.
Dessa riktlinjer och kostråd sammanfattas i ett översiktligt cirkeldiagram kallat Wheel of five. För att råden ska accepteras – och få betydelse för folkhälsan – behöver de innebära en så liten förändring som möjligt jämfört med befintliga matvanor. Mycket arbete pågår för att ta fram metoder som väger samman de olika målen för mat, näring, hälsa och miljö. Stort fokus läggs på tydlig kommunikation och enkla hållbara val i vardagen enligt Corné van Dooren.

Råden för hälsa och hållbarhet går oftast hand i hand. Fisk är ett undantag. Fisk rekommenderas enbart en gång per vecka eftersom två portioner fisk ger en betydligt större miljöpåverkan i förhållande till hälsofördelarna. I modellen täcks 85 procent av rekommenderat energiintag. Resterande 15 procent utelämnas för att göra modellen flexibel och öka följsamheten.
Nicole Darmon vid Institute for Agricultural Research i Montpellier, presenterade de franska kostråden som kombinerar hälsa, hållbarhet och matkultur. Målet är att i ett holistiskt perspektiv skydda ekosystemen. För att råden ska bli accepterade inkluderas även traditioner och kultur samt ekonomi – både ur konsumentens och producentens perspektiv.
Små förändringar i kostmönstret har visats ge god effekt. Det gör störst skillnad för miljö och klimat om man minskar konsumtionen av kött, fisk och ägg (dessa hade slagits samman i redovisningen). Att äta mindre kött är accepterat i befolkningen men kan kräva att man äter mer av mjölk och fisk för att nå önskvärda intag av näringsämnen. Mejeriprodukternas roll i matkulturen värderas högt noterade Nicole Darmon.
I samband med presentationen ställdes många frågor kring metodik, klassificering av livsmedelsgrupper och ekonomiska beräkningar.
Kerry Brown vid avdelningen för folkhälsa vid London School of Hygiene & Tropical Medicine, gav ett brittiskt och globalt perspektiv på beteendeförändringar och kostmönster.
De brittiska näringsrekommendationerna uppdateras kontinuerligt med fokus på hälsa medan hållbarhetsaspekter ofta beräknas i efterhand. Man strävar efter små förändringar och en förflyttning av konsumtionsmönstret, bland annat via nudging. Ett exempel är hur proteinkällor presenteras: Istället för att använda benämningen ”kött, fisk och ägg” ger ”bönor, ägg, fisk eller kött” ett mer önskat beteende och hållbara val.
Matsystemet är globalt och mycket komplext. Kerry Brown visade att även önskvärda beteendeförändringar, till exempel ett ökat grönsaksintag, ger avtryck i miljö och klimat. Att inte överkonsumera och inte slänga mat är okomplicerade men viktiga råd för hälsa och miljö. Biodiversitet är ett komplext men väldigt viktigt område konstaterade hon.
Matens ursprung har stor betydelse. Vegetariska råvaror som frukt, avokado och nötter kräver ofta mycket vatten, som ibland måste transporteras långt. Animalieproduktion kräver inte lika hög vattenanvändning. Om man prioriterar lokal odling, och produktionen flyttas längre norrut blir odlingsförhållandena sämre och kostnader för arbetskraft ökar. Det innebär högre kostnad för konsumenten, inte minst för grönsaker och frukt, vilket också kan påverka konsumtionen avslutade Kerry Brown.
Kommentarer från forskare och andra deltagare
Webbinariet avrundades med att forskare och andra intressenter gav sina synpunkter i korta presentationer. Här presenteras ett urval.
Ola Thomsson, SLU, underströk att hållbarhet är en bred och komplicerad fråga. Som exempel nämndes att det krävs mycket vatten för att odla mandlar och olivolja medan kokos- och kaffeodling minskar biodiversiteten. Man måste titta på hela produktionen när man pratar om planetära gränser. Livscykelanalyser tar till exempel inte hänsyn till de positiva aspekterna av betande djur.
Elinor Hallström, RISE, lyfte två perspektiv: risker och möjligheter med livscykelanalyser, samt berikning av livsmedel. När vi äter allt mer växtbaserat måste näringsinnehåll och biotillgänglighet säkerställas, till exempel genom att berika andra produkter med järn eller kalcium. Befintlig kunskap inom området är begränsad och forskning pågår.
Sirpa Sarlio, Social- och hälsovårdsministeriet i Finland, lyfte att det finns många olika metoder att utvärdera matens kvalitet samt påverkan på klimat och miljö. När hållbarhetsfrågan inkluderas i rekommendationerna måste samma vetenskapliga krav ställas som på matens påverkan på hälsan.
Merja Saarinen, Naturresursinstitutet i Finland, poängterade att råd som integrerar både nutrition och miljöaspekter är komplexa och kan vara svåra för konsumenten att tolka. Råden behöver ta hänsyn till näringsbehov i olika grupper, till exempel vad gäller kött.
Nina Edholm, Klimat- och miljödepartementet, Norge, vill se ett holistiskt perspektiv på miljöpåverkan och att arbetet med hälsa och miljö görs i samförstånd mellan till exempel livsmedelsindustrin och hälso- och sjukvården.
Bryndis Eva Birgisdottir, Food Science and Nutrition vid Islands universitet, betonade att människans och planetens hälsa hänger ihop. Hållbara matsystem och konsumentens strävan efter att äta hälsosamt är starka drivkrafter men förutsättningarna är ojämlika och olika faktorer påverkar vårt beteende. Även förpackningar är en viktig fråga.
Nordiska näringsrekommendationer 2022 – nu är de första artiklarna om metodiken publicerade
Uppdateringen av de nordiska näringsrekommendationerna, NNR, pågår och planen är att de ska publiceras 2022. Nyligen publicerades de tre första artiklarna om metodiken som NNR2022 baseras på.
>>text: Cecilia Nälsén, PhD Nutrition, nutritionsfakta.se
NNR utgör den vetenskapliga grunden för referensvärden för näringsämnen och kostråd i Norden och är baserad på en samlad bedömning av det vetenskapliga underlaget. NNR är ett nordiskt samarbete som startades 1980. NNR har uppdaterats regelbundet sedan dess och detta är den sjätte utgåvan.
I NNR2022 kommer alla kapitel från den förra utgåvan, NNR2012, att uppdateras. Nya kapitel kan komma till med särskild betydelse för folkhälsan i de nordiska länderna. I NNR2022 kommer det att finnas ett ökat fokus på kostmönster, hållbarhet och miljö samt övervikt och fetma.
Nyligen publicerades de tre första artiklarna om NNR2022 i Food & Nutrition Research som beskriver processen och metoderna för hur NNR ska uppdateras. Den första artikeln handlar om organisation, upplägg och metoder och den andra och tredje artikeln beskriver hur de systematiska litteraturöversikterna (systematiska reviews) ska utföras i NNR-arbetet. De systematiska litteraturöversikterna ger en samlad bedömning av den vetenskapliga litteraturen för det samband man vill studera, till exempel kostmönster och hälsa. I en systematisk litteraturöversikt redovisas tydligt hur sökningar och urval av studier har gjorts.
Länk till artiklarna: foodandnutritionresearch.net/index.php/fnr/index
Se också Helsedirektoratets webbplats med mer information om NNR2022 och där läggs också alla utlysningar ut: www.helsedirektoratet.no/english/nordic-nutrition-recommendations-2022
Norge leder arbetet med NNR2022 och de nordiska länderna har två representanter var i arbetsgruppen och en representant i styrgruppen. Många forskare och experter i Norden kommer att engageras för att uppdatera NNR.
Flera orsaker till att fetma är en riskfaktor vid covid-19
Covid-19 som orsakas av SARS-CoV-2 (Severe Acute Respiratory Syndrome-Coronavirus-2) har sedan hösten 2019 snabbt spridits till mer än 100 länder över hela världen. Symptomen varierar från att likna mild influensa till mycket allvarliga sjukdomstillstånd som kräver intensivvård med andningsstöd och hög risk för död, framför allt bland äldre. Men även vuxna i yngre åldrar har drabbats hårt. En av de definierade riskgrupperna är personer med svår fetma, med ett BMI över 40 kg/m2 (1).
>> text: Ingrid Larsson, näringsfysiolog, docent, universitetssjukhusöverdietist, Enheten för klinisk nutrition och Regionalt obesitascentrum, Sahlgrenska universitetssjukhuset, Göteborg.
En utmaning med att sammanfatta ett nytt område (våren 2020) som covid-19 är inte bristen på vetenskapliga artiklar, utan motsatsen – den stora mängden av publicerade vetenskapliga artiklar. När ett nytt område så snabbt blir påtagligt för många länder och dess invånare blir det också högintressant ur forskningssynpunkt. Det leder i sin tur till att ett mycket stort antal artiklar publiceras under kort tid. Artiklarna om covid-19 handlar om allt från beskrivningar av grupper av sjukhusvårdade patienter och så kallade viewpoints och correspondence till riktlinjer baserade på den information som finns tillgänglig.
Med tiden kommer det att visa sig att några av slutsatserna vilar på otillräckligt underlag, eller är felaktiga. Antalet tillbakadragna artiklar kommer att öka. Redan nu har en sådan artikel rönt stor uppmärksamhet: den publicerades i Lancet i maj 2020 och handlar om behandling med klorokin vid covid-19 (2). Den drogs tillbaka på grund av brister i data, resultat och slutsatser.
Det är inte konstigt att många vill bidra till att öka kunskapen om coronaviruset, då det är förhållandevis okänt i nuvarande form och som under kort tid har drabbat många. Observationer av vilka som blir sjuka, vilka sjukdomar de har sedan tidigare, symptom, hur sjuka människor blir och vilka som avlider ger oss information och underlag till hur vi kan gå vidare med behandling och rehabilitering av de svårast sjuka. Men det är också viktigt att förstå att forskare har haft kort tid på sig att samla in och analysera informationen. De vetenskapliga tidskrifterna har snabbehandlat artiklarna före publicering, vilket ökar risken för fel eller inkonsekventa resonemang. Trots dessa förbehåll är det viktigt att ta upp kopplingen mellan covid-19 och fetma.
Fetma och övervikt i den vuxna befolkningen
I gruppen 16 till 84 år har 16 procent av svenskarna ett BMI över 30 kg/m2 (Hälsa på lika villkor, Folkhälsomyndigheten). Lägger man till gruppen med övervikt blir andelen 51 procent. Längd och vikt är självrapporterade, vilket gör det troligt att den verkliga förekomsten av övervikt och fetma är högre.
Gruppen med BMI över 40 kg/m2, så kallad fetma grad 3 (3), har identifierats som en riskgrupp, och en stor andel av dem som behöver sjukvård på grund av covid-19 har fetma. Dessutom kan det finnas många människor med fetma som är oroliga för sin hälsa under covid-19-pandemin, och som undrar om man kan göra något ytterligare för sin hälsa för att minska riskerna att smittas av coronaviruset förutom de givna rekommendationerna om handhygien, social distansering och att hålla sig hemma vid sjukdom.
Pandemier i historien
När kunskapen är begränsad är det bra att ta utgångspunkt i vad man vet sedan tidigare. Historiskt sett har vi flera kända pandemier. Digerdöden (pesten eller stora döden), orsakad av bakterien Yersinia pestis, drabbade Europa på 1300-talet, 1700-talet och även under senare delen av 1800-talet. Spanska sjukan, orsakades av influensavirus av typ A, var en pandemi som drabbade världen 1918 till 1920 då mellan 20 och 50 miljoner människor dog (4). Trots att det saknas detaljerad information om historiska pandemier kan vi nog utgå ifrån att de drabbade snarare var undernärda än övernärda. Fetma var inte en försvårande omständighet vid dessa bakterie- och virusutbrott.
Nittio år efter spanska sjukan, kom H1N1-pandemin, svininfluensan 2008-2009, och personer med svår fetma drabbades särskilt hårt (5). Studier visade att även om man var vaccinerad hade personer med fetma större risk att smittas av influensa, jämfört med personer med normalvikt (6). Efter svininfluensapandemin listade amerikanska Centers for disease control and prevention (CDC) personer med BMI 40 kg/m2 eller högre som en riskgrupp vid influensa (7).
Tidigt under våren 2020 definierade Folkhälsomyndigheten och Socialstyrelsen personer med BMI 40 kg/m2 eller högre som en riskgrupp för covid-19. Under försommaren 2020 justerade CDC gränsvärdet för BMI som ökad risk vid covid-19 till att gälla BMI 30 kg/m2 eller högre (8). De svenska myndigheterna avvaktar en justering av gränsvärdet för BMI tills det finns mer kunskap.
Varför är fetma en riskfaktor vid covid-19?
Med det aktuella informationsunderlag som publicerats under våren 2020 om covid-19, samt det man vet från svininfluensapandemin 2008-2009, vill jag lyfta fram tre aspekter av fetma och covid-19: fetma och samsjuklighet, endokrina aspekter och mekanistiska aspekter.
Fetma och samsjuklighet
Det är väletablerad kunskap att sjukdomen fetma är relaterad till många olika sjukdomsdiagnoser. Dessa innefattar typ 2-diabetes, hjärt- och kärlsjukdom, sjukdomar som påverkar andningsorganen, till exempel sömnapné, cancersjukdomar, skelett- och ledsjukdomar, fertilitetssjukdomar och psykiatriska sjukdomar (9). Flera av sjukdomarna kan dessutom öka mottagligheten för infektioner.
Sammanställningar från sjukhus i olika länder visar att mellan drygt 10 och 46 procent av patienterna med covid-19 också har fetma (10-13). Denna grupp har också allvarligare symptom av covid-19 jämfört med patienter med lägre BMI och behöver till högre grad intensivvård (10-15). Beskrivningarna visar också att de som behöver intensivvård till stor del också har högt blodtryck och typ 2-diabetes (10-12) samt kronisk obstruktiv lungsjukdom (KOL), leversjukdom och cancersjukdom (10). En gemensam nämnare för flera av dessa sjukdomar är just fetma.
Endokrina aspekter
Fetma kännetecknas av en kronisk låggradig inflammation (16). Inflammationsmarkörer som exempelvis cytokiner och interleukiner produceras i fettvävnaden. Ju större mängd fettvävnad, det vill säga ju högre vikt man har, desto högre koncentrationer av inflammationsmarkörer har en person (16, 17). Den kroniska låggradiga inflammationen påverkar immunsystemet negativt och skulle kunna leda till att personer med svår fetma har en sänkt motståndskraft mot coronaviruset (17). Om man dessutom har fetmarelaterad samsjuklighet skulle motståndskraften kunna sänkas ytterligare, vilket skulle kunna förklara varför exempelvis typ 2-diabetes, högt blodtryck och cancer är överrepresenterade bland de kritiskt sjuka.
Forskningen visar på en annan möjlig förklaring till varför personer med fetma är särskilt sårbara: att coronaviruset (SARS-CoV-2) tar sig in i cellerna via de så kallade ACE-2-receptorerna (angiotensin-konvertasenzym-2). ACE-2 ingår i RAAS (renin-angiotensin-aldosteronsystement) som bland annat håller blodtrycket i balans och skyddar mot inflammation (18-20).
Eftersom RAAS är nära relaterat till fetma och är ett dynamiskt system är forskarnas tes att coronaviruset genom att ”kidnappa” ACE-2-receptorer rubbar balansen i RAAS och därmed bidrar till ett svårare sjukdomsförlopp med hyperinflammation och andningssvikt (20, 21). Det är dock idag inte klarlagt vilken roll ACE-2 spelar vid covid-19 (22).
Mellan 20 och 50 procent av personer som drabbats av covid-19 har typ 2-diabetes (23). I en studie på möss fann man att kroniskt högt blodsocker ledde till försvagning av ACE-2-receptorer som skulle kunna ha en direkt effekt på beta-celler i bukspottskörteln som påverkar insulinproduktionen (24). När man gav mössen insulin normaliserades blodsockernivåerna och koncentrationen av ACE-2 i serum. Enligt författarna indikerar resultaten att insulin bidrar till normalisering av aktiviteten i RAAS (24). Det återstår att undersöka om detta även gäller människor, men skulle i så fall kunna förklara varför typ 2-diabetes leder till ett svårare sjukdomsförlopp i covid-19. Det är väl visat i tidigare studier att personer med typ 2-diabetes också ofta har fetma, högt blodtryck och därmed ökad risk för hjärt-kärlsjukdom.
Mekanistiska aspekter
Personer med fetma, särskilt de med ett BMI från 35 kg/m2 och över, har ofta svåra mekaniska problem med andningen och dessutom relaterade sjukdomar såsom sömnapnésyndrom. Till fetmarelaterade andningsstörningar hör obstruktiv sömnapné (obstructive sleep apnoea, OSA) som också ökar med stigande ålder (25). Förekomsten av fetma är hög i äldre åldersgrupper.
Baserat på Folkhälsomyndighetens data från 2018 i ”Hälsa på lika villkor” är förekomsten med fetma, över 30 kg/m2 i BMI, 18 procent bland personer 65-84 år. Lägger man till övervikt blir andelen 61 procent. Obstruktiv sömnapné förekommer som andningsstörningar under sömn hos mellan 30 och 80 procent av de äldre (26). I en äldre åldersgrupp, 65-90 år, hade 7,9 procent av männen och 4,9 procent av kvinnorna allvarlig obstruktiv sömnapné, definierat som mer än 30 andningsuppehåll per timme (27). Tidigare hjärtinfarkt, kärlkramp, stroke och astma var högre bland dem med obstruktiv sömnapné, oberoende av kön (27).
När coronaviruset angriper andningsorganen får den drabbade personen svårt att andas och syremättnaden i blodet sjunker. Om man redan har begränsad andningskapacitet på grund av fetma, eftersom fettdepåerna minskar utrymmet för lungorna att arbeta, blir det än svårare med andningen när lungorna angrips av coronaviruset. Detta skulle kunna vara en av förklaringarna till varför man ser en stor andel med svår fetma som behöver intensivvård med andningsstöd.
Sammantaget finns det flera delar som pekar mot varför personer med svår fetma utgör en riskgrupp vid covid-19: hög förekomst av relaterade sjukdomar som i sig ökar sårbarheten vid en infektion, den låggradiga inflammationen som kommer av att inflammationsmarkörer produceras i fettvävnaden och att personer med fetma har svårare att andas och syresätta blodet genom att fettvävnaden ger mindre utrymme för lungorna att arbeta på ett optimalt sätt.
Nutritionella aspekter vid återhämtning och rehabilitering efter covid-19
Oberoende om man har fetma eller inte före insjuknandet minskar vikten dramatiskt under lång tid av intensivvård (28). Patienterna i respirator får energi och näring genom sond. Ofta är detta inte tillräckligt för att fylla det ökade behovet av energi på grund av den svåra sjukdomen. Det är också svårt att beräkna energibehovet för en person med en svår sjukdom och som är orörlig under många veckor. Dessutom måste vården prioritera att behandla de akuta faserna av sjukdomen.
Svårigheterna kvarstår under rehabiliteringen (28). Sängläge under flera veckor leder till att en stor andel av viktförlusten är fettfri massa, det vill säga muskelmassa. Viktminskningen och förlusten av muskelmassa leder till många problem under rehabiliteringsperioden – som förväntas bli mycket lång för många. Vid svår fetma är de nutritionella problemen lika stora som vid normalvikt (28).
Det finns risk att personer med fetma som minskar i vikt under behandling av covid-19 kan utveckla så kallad sarkopen fetma. Sarkopeni innebär en liten andel muskelmassa i förhållande till fettmassan. Detta tillstånd påverkar nutritionsstatus hos personen och i studier på äldre med sarkopeni visar också att aptiten hos de äldre minskar. Svårigheter att äta på grund av eventuella skador efter intubering leder till ytterligare nutritionella utmaningar.
Vid rehabilitering av patienter med covid-19 är det alltså flera aspekter man behöver ta i beaktande, inte minst förlusten av muskelmassa som påverkar nutritionsstatus generellt och även aptiten (28). Mat, energi och näring kommer sannolikt att vara en mycket central del under rehabiliteringen av covid-19.
Fetma vid social isolering
En av de bärande rekommendationerna till befolkningen för att minska spridningen av coronaviruset är att minska sociala kontakter och hålla sig hemma så mycket som det går. En del kan fortsätta att arbeta tack vare tekniska lösningar, medan andra har blivit permitterade från sitt arbete på grund av den ekonomiska situationen. Andra är arbetssökande före pandemiutbrottet och påverkas ytterligare av isoleringen.
När strukturerna i vardagen, arbete, skola eller sysselsättning försvinner och isoleringen ökar, och detta kombineras med ökad oro för att bli smittad av covid-19, försöker människor hantera situationen. För de som har fetma och försöker hantera sin oro med hjälp av mat finns en risk att vikten ökar ytterligare.
Vid isolering eller vid karantän finns en rad rekommendationer för god nutrition (29) och som också gynnar en begränsad viktökning vid fetma:
• att försöka hålla regelbunden måltidsordning
• att äta varierat med stor andel grönsaker och frukt
• att begränsa intaget av energität mat såsom snabbmat, sötsaker och snacks
• att använda vatten och andra energifria drycker som törstsläckare
• att dagligen utöva fysisk aktivitet antingen i form av program hemma eller promenader
Pandemin som motivation för livsstilsförändring?
Kan en pandemi motivera till livsstilsförändring mot lägre vikt bland personer som lever med fetma? Det vet vi inte, men studier visar att en majoritet av personer som lever med fetma rapporterar att de ständigt försöker minska eller kontrollera sin vikt (30), så tanken är inte orimlig.
Vi vill alla ha en god hälsa och vara friska. När nu svår fetma identifierades som risk vid covid-19 tidigare i år, är det inte konstigt om många börjar fundera över vad man kan göra för att minska risken att bli drabbad av coronaviruset. Oavsett vilken anledning man har för att göra en livsstilsförändring för lägre vikt vid fetma, är det gynnsamt för hälsan. En del önskar stöd i förändringsarbetet och därför det är viktigt att hälso- och sjukvården erbjuder kunskapsbaserade behandlingsprogram.
Om man på egen hand vill påbörja förändringsarbetet kan man ta utgångspunkt i det amerikanska registret The National Weight Control Registry (NWCR) som systematiskt samlat kunskap om vad personer gjort som minskat mycket i vikt och kunnat hålla vikten (31) och gjort det under mer än 10 års tid (32). NWCR har kommit fram till sju framgångsfaktorer för lägre vikt under lång tid (31).
Framgångsfaktorer för bestående viktminskning enligt NWCR
|
Framgångsfaktor |
Praktiskt råd – kommentar |
|
Minska energiintaget |
Ta inte om av maten, väg maten enligt ett kostråd. |
|
Ät mindre fett och sött |
Ät mycket mindre av energität mat och dryck mellan måltider, såsom godis, choklad, bakverk, glass, snacks och sockersötade drycker. |
|
Planera för att äta måltider regelbundet under dagen |
Tre till fyra huvudmåltider som fördelas regelbundet som exempelvis frukost, lunch, middag och kvällsmål. Undvik småätande mellan måltiderna. Frukt som mellanmål rekommenderas. |
|
Ät frukost varje dag |
Den som äter frukost har lättare att äta lagom mycket under resten av dagen, och inte minst förhindra stora måltider kvällstid. |
|
Regelbunden vägning |
Upprätta en vägningsrutin, dagligen eller några gånger per vecka. Det blir då lättare att fånga upp och justera mindre viktökningar. |
|
Skriva matdagbok |
Med matdagbok (en app, skrivbok eller liknande) håller man koll på måltidsmönster och vad man äter. Det är lättare att förändra något man är medveten om. Det finns appar som kan beräkna kalorier, för dem som önskar. |
|
Vara fysisk aktiv minst en timme per dag |
Med hög energiomsättning och muskelarbete blir det lättare att behålla en lägre vikt och svårare att öka i vikt. |
Ett sätt att komma igång är att välja ut tre till fem av ovanstående punkter och testa dessa. De som fungerar i vardagen behåller man. Det viktigaste för viktminskning är att energiintaget är lägre än energiförbrukningen och att man kan upprätthålla denna obalans över tid. Den som använder covid-19-pandemin som ett incitament till en levnadsvaneförändring för en lägre vikt kan utnyttja pandemin på ett konstruktivt sätt – för att generellt minska risken för fetmarelaterad sjukdom.
Referenser
1. Ryan DH, Ravussin E, Heymsfield S. COVID 19 and the Patient with Obesity – The Editors Speak Out. Obesity (Silver Spring). 2020;28(5):847.
2. Mehra MR, Ruschitzka F, Patel AN. Retraction-Hydroxychloroquine or chloroquine with or without a macrolide for treatment of COVID-19: a multinational registry analysis. Lancet. 2020;395(10240):1820.
3. WHO. Obesity: preventing and managing the global epidemic. Report of a WHO consultation. World Health Organ Tech Rep Ser. 2000;894:i-xii, 1-253.
4. Kolata G. Berättelsen om den stora influensa-epidemin 1918 och jakten på det virus som orsakade den. Stockholm: Bokförlaget Prisma; 2000. 313 p.
5. Louie JK, Acosta M, Winter K, Jean C, Gavali S, Schechter R, et al. Factors associated with death or hospitalization due to pandemic 2009 influenza A(H1N1) infection in California. Jama. 2009;302(17):1896-902.
6. Neidich SD, Green WD, Rebeles J, Karlsson EA, Schultz-Cherry S, Noah TL, et al. Increased risk of influenza among vaccinated adults who are obese. Int J Obes (Lond). 2017;41(9):1324-30.
7. CDC. People at high risk for flu complications 2018 [Available from: https://www.cdc.gov/flu/highrisk/index.htm].
8. CDC. Coronavirus Disease 2019 (Covid-19). People with certain medical conditions. [Available from: https://www.cdc.gov/coronavirus/2019-ncov/need-extra-precautions/people-with-medical-conditions.html].
9. Jastreboff AM, Kotz CM, Kahan S, Kelly AS, Heymsfield SB. Obesity as a Disease: The Obesity Society 2018 Position Statement. Obesity (Silver Spring). 2019;27(1):7-9.
10. Cai Q, Chen F, Wang T, Luo F, Liu X, Wu Q, et al. Obesity and COVID-19 Severity in a Designated Hospital in Shenzhen, China. Diabetes Care. 2020.
11. Cummings MJ, Baldwin MR, Abrams D, Jacobson SD, Meyer BJ, Balough EM, et al. Epidemiology, clinical course, and outcomes of critically ill adults with COVID-19 in New York City: a prospective cohort study. Lancet. 2020;395(10239):1763-70.
12. Richardson S, Hirsch JS, Narasimhan M, Crawford JM, McGinn T, Davidson KW, et al. Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area. Jama. 2020.
13. Caussy C, Pattou F, Wallet F, Simon C, Chalopin S, Telliam C, et al. Prevalence of obesity among adult inpatients with COVID-19 in France. Lancet Diabetes Endocrinol. 2020.
14. Caussy C, Wallet F, Laville M, Disse E. Obesity is Associated with Severe Forms of COVID-19. Obesity (Silver Spring). 2020.
15. Gao F, Zheng KI, Wang XB, Sun QF, Pan KH, Wang TY, et al. Obesity Is a Risk Factor for Greater COVID-19 Severity. Diabetes Care. 2020.
16. Hotamisligil GS. Inflammation and metabolic disorders. Nature. 2006;444(7121):860-7.
17. Chiappetta S, Sharma AM, Bottino V, Stier C. COVID-19 and the role of chronic inflammation in patients with obesity. Int J Obes (Lond). 2020.
18. Alifano M, Alifano P, Forgez P, Iannelli A. Renin-angiotensin system at the heart of COVID-19 pandemic. Biochimie. 2020;174:30-3.
19. Iannelli A, Favre G, Frey S, Esnault V, Gugenheim J, Bouam S, et al. Obesity and COVID-19: ACE 2, the Missing Tile. Obes Surg. 2020.
20. Lundström A, Sandén P. ACE-2 och coronavirus – en fråga om balans och dynamik? Läkartidningen. 2020;117(17-18):F383.
21. Hoffmann M, Kleine-Weber H, Schroeder S, Kruger N, Herrler T, Erichsen S, et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell. 2020;181(2):271-80 e8.
22. Dalan R, Bornstein SR, El-Armouche A, Rodionov RN, Markov A, Wielockx B, et al. The ACE-2 in COVID-19: Foe or Friend? Horm Metab Res. 2020;52(5):257-63.
23. Bornstein SR, Rubino F, Khunti K, Mingrone G, Hopkins D, Birkenfeld AL, et al. Practical recommendations for the management of diabetes in patients with COVID-19. Lancet Diabetes Endocrinol. 2020;8(6):546-50.
24. Roca-Ho H, Riera M, Palau V, Pascual J, Soler MJ. Characterization of ACE and ACE2 Expression within Different Organs of the NOD Mouse. Int J Mol Sci. 2017;18(3).
25. Sforza E, Hupin D, Pichot V, Barthelemy JC, Roche F. A 7-year follow-up study of obstructive sleep apnoea in healthy elderly: The PROOF cohort study. Respirology. 2017;22(5):1007-14.
26. Young T, Peppard PE, Gottlieb DJ. Epidemiology of obstructive sleep apnea: a population health perspective. Am J Respir Crit Care Med. 2002;165(9):1217-39.
27. Donovan LM, Kapur VK. Prevalence and Characteristics of Central Compared to Obstructive Sleep Apnea: Analyses from the Sleep Heart Health Study Cohort. Sleep. 2016;39(7):1353-9.
28. Brugliera L, Spina A, Castellazzi P, Cimino P, Arcuri P, Negro A, et al. Nutritional management of COVID-19 patients in a rehabilitation unit. Eur J Clin Nutr. 2020;74(6):860-3.
29. Muscogiuri G, Barrea L, Savastano S, Colao A. Nutritional recommendations for Covid-19 quarantine. Eur J Clin Nutr. 2020;74(6):850-1.
30. Zenténius E, Andersson-Assarsson JC, Carlsson LMS, Svensson P-A, Larsson I. Self-reported weight loss methods and weight change: 10-years analysis in the Swedish Obese Subjects Study control group. Obesity, accepted for publication. 2018.
31. Wing RR, Hill JO. Successful weight loss maintenance. Annu Rev Nutr. 2001;21:323-41.
32. Thomas JG, Bond DS, Phelan S, Hill JO, Wing RR. Weight-loss maintenance for 10 years in the National Weight Control Registry. Am J Prev Med. 2014;46(1):17-23.
Rätt beredning och processning av växtbaserade livsmedel minskar risk för brist på järn och zink
Mindre protein från kött och mer från växtriket. Denna kost anses vara en väg att minska utsläppen av växthusgaser från den globala livsmedelsproduktionen, främst via storskalig djurhållning. En kost med mindre kött och mer växtbaserade livsmedel och fisk kopplas också till minskad risk för övervikt och sjukdomar. Samtidigt ökar denna kost risken för brist på många för människan livsviktiga mineraler, som järn och zink. Men det finns en lösning. Avgörande är beredning och processning av växtbaserade livsmedel, som spannmål och baljväxter, skriver Ann-Sofie Sandberg, professor i livsmedelskunskap vid Chalmers Tekniska Högskola.
>> text: Ann-Sofie Sandberg, professor, Livsmedelsvetenskap, Chalmers Tekniska Högskola, Göteborg.
Proteinskiftet
I EAT Lancet-rapporten som publicerades 2019 och fick stort genomslag beskrivs en riktning man enligt författarna behöver gå för att uppnå ett globalt hållbart och hälsosamt livsmedelssystem (1). Livsmedelssektorn står för mer än 25 procent av utsläppen av växthusgaser i världen och storskalig djurhållning utgör den största källan. Att minska intaget av rött kött anges som den viktigaste åtgärden för att minska utsläppen av växthusgaser och man föreslår i rapporten en övergång från animaliskt till växtbaserat protein. Denna förändring benämns ”proteinskiftet”. För nordiska förhållanden kan även miljömässigt hållbara fiskråvaror utgöra ett komplement till växtbaserat protein (2).
Hälsoeffekter av ett proteinskifte
Ett flertal studier visar på att en vegetarisk, vegansk eller så kallad pescetarisk kost (vegetarisk med tillägg av fisk och skaldjur) innebär minskad risk för övervikt och för flera av våra vanligaste folksjukdomar såsom typ 2-diabetes och hjärt-kärlsjukdom. Ett kostmönster med växtbaserade livsmedel rikt på fullkorn, baljväxter, frukt och grönt samt enkel- och fleromättade fetter, liksom fisk och skaldjur är således förknippat med minskad risk för sjukdom och lägre dödlighet, särskilt om fisk ingår (3). Men man måste vara medveten om att mat som är klimatsmart inte nödvändigtvis är bra för hälsan – och att hälsosam mat inte alltid är bra för miljön.
Om man utesluter kött och fisk ur kosten finns en risk för brist på flera mikronäringsämnen såsom vitamin D, B12, jod, järn och zink. Saknas fisk och skaldjur i kosten får man inte i sig fiskfettsyrorna, de långkedjiga omega 3-fettsyrorna EPA och DHA, som bland annat skyddar mot hjärt-kärlsjukdom (4). Växtbaserade livsmedel innehåller inte vitamin D, B12, jod och fiskfettsyror. Järn och zink i dessa livsmedel är bundna till organiska föreningar, som fytinsyra och tanniner, och är därför svåra att ta upp i tarmen.
Enligt SIFO:s klimatbarometer 2019 säger 40 procent av svenska befolkningen att de minskat sin köttkonsumtion för att begränsa klimatpåverkan, och trenden bekräftas av Jordbruksverkets statistik. Att äta vegetarisk kost eller vegankost har särskilt attraherat unga kvinnor, som samtidigt utgör en riskgrupp för järnbrist och zinkbrist. Betydelsen för andra mineraler såsom kalcium och magnesium är mer oklart, därför ligger fokus i denna artikel på järn och zink.
Järn och zink
Järn och zink är livsnödvändiga mineraler för människan. Järn behövs för att transportera syret i blodet och i muskler. Zink ingår i många av våra enzymsystem och är bland annat viktigt för immunsystemets funktion. Man räknar med att en man som väger 75 kg behöver ta upp 1 mg järn om dagen. En kvinna i barnafödande ålder behöver mer (1,5 mg/dag) beroende på menstruationen (5). För barn och tonåringar som växer och gravida kvinnor ökar järnbehovet. Även zinkbehovet är större för dessa grupper (6).
Järn förekommer i två former i vår mat: hemjärn och icke-hemjärn. Hemjärn finns enbart i animaliskt protein, alltså i kött och fisk, som dessutom innehåller icke-hemjärn. I växtbaserade livsmedel finns enbart icke-hemjärn. Hemjärn och icke-hemjärn tas upp via två olika vägar i tarmen. När det gäller hemjärn tas hela molekylen upp i tarmcellen. För icke-hemjärn är det bara de fria järnjonerna som tas upp, vilket gör att absorptionen kan påverkas av andra faktorer i kosten.
Biotillgängligheten, det vill säga den andel av järnet som tas upp och kan utnyttjas av kroppen, är för hemjärn cirka 25 procent och för icke-hemjärn 5 procent. Kött och fisk innehåller dessutom protein som stimulerar kroppens upptag av icke-hemjärn.
Kött och fisk stimulerar järnupptaget
Det är alltså två faktorer i kött och fisk som är gynnsamt för järnupptaget, både innehållet av hemjärn och protein som stimulerar upptaget av icke-hemjärn. I en måltid med kött och fisk är biotillgängligheten för järn ungefär 15 procent, medan en vegetarisk måltid ligger på 4-7 procent. beroende på innehållet av stimulerande eller hämmande faktorer (5, 7).
Viktiga zinkkällor i kosten är kött, mejeriprodukter och fisk. För kvinnor som åt vegetarisk kost kunde man i en kontrollerad studie visa att absorptionen av zink bara var 2/3 jämfört med en blandad kost (6). Den som äter vegetariskt behöver alltså ett 50 procent högre zinkintag för att uppnå samma absorberad mängd zink som den som äter blandad kost.
I växtbaserade livsmedel finns flera föreningar som hämmar upptaget av icke-hemjärn. Den viktigaste är fytinsyra som bildar olösliga föreningar eller aggregat med järn och zink i tarmen vilket hindrar att mineralerna tas upp. Fytinsyra som främst finns i fullkorn, kli, baljväxter, frön och nötter är den mest betydande hämmande faktorn (8). Vissa järnbindande polyfenoler, såsom tanniner och sojaprotein, är också potenta hämmare. Tanniner finns bland annat i svart sorghum, svart te och i bönor (9).
Å andra sidan är de viktigaste stimulerande faktorerna för upptaget av icke-hemjärn animaliskt protein, och askorbinsyra som framför allt finns i frukt, bär och grönsaker. Även för zink utgör fytinsyra den viktigaste hämmande faktorn medan animaliskt protein stimulerar absorptionen.
Kalcium är den enda komponent i maten som kan hämma upptaget av hemjärn och icke-hemjärn (10).
Vegetarianer riskerar brist på järn och zink
Kvinnor i barnafödande åldrar samt barn och tonåringar har stort järnbehov och ökad risk för järnbrist. Järnbrist förekommer hos ungefär var fjärde kvinna i fertil ålder i Sverige, men är långt vanligare och mer allvarlig i låginkomstländer. Enligt Riksmaten ungdom från 2016-2017 har var tredje flicka i årskurs 8 och årskurs 2 i gymnasiet järnbrist (11). Enligt Världshälsoorganisationen (WHO) lider 2 miljarder människor, främst kvinnor och barn, av järnbrist (12).
Den milda formen av järnbrist ger trötthet, försämrad kognitiv funktion och prestation. Svårare järnbrist, som framför allt förekommer i låginkomstländer, ökar risken för att gravida kvinnor föder för tidigt, ökad dödlighet och sjuklighet för mamma och barn, försämrat immunförsvar och försämrad utveckling av hjärnans funktion hos barn.
Liknande tillstånd kan uppstå vid zinkbrist. Den kan också leda till tillväxthämning och störd utveckling hos barn. För vuxna kan bristen medföra försämrad sårläkning och försämrad aptit. Förekomsten av zinkbrist i låginkomstländer anses ligga på samma nivå som järnbrist, men i Sverige har risken för zinkbrist ansetts låg. Detta kan komma att förändras i och med övergång till mer växtbaserad kost.
I kontrollerade studier är det visat att vegetarianer har mindre lager av järn i kroppen (6). Utvärdering av vegetarisk kost avseende zink har varit svårare att genomföra då det inte finns bra metoder för att mäta mild zinkbrist, men även för zink tycks nivåerna i blodet sjunka vid vegetarisk kost (6, 13). Dock har inga funktionella störningar uppmätts i höginkomstländer.
Livsmedelsberedning och processer kan förbättra upptaget av järn och zink från växtbaserad mat
Den goda nyheten är att järn- och zinkupptaget från spannmål och baljväxter kan förbättras genom beredning och process. Eftersom fullkorn och vissa typer av baljväxter har ett högt innehåll av järn och zink skulle de kunna utgöra en god källa för dessa mineraler – om fytinsyra och tanniner togs bort. I växten finns ofta naturligt förekommande enzymer som kan bryta ner fytinsyran och även tanninerna om förhållandena är de rätta, som surhetsgrad, temperatur och tid. Man kan också använda mikroorganismer, mjölksyrabakterier och svampar, som producerar dessa enzymer (14).
När det gäller järnupptaget måste fytinsyran brytas ner nästan fullständigt för att järnabsorptionen ska förbättras, medan zinkupptaget förbättras redan vid 80 procents nedbrytning. Traditionell behandling av livsmedel har ofta fungerat så, till exempel surdegsjäsning av bröd, hydrotermisk behandling, mältning och fermentering. Hydrotermisk behandling är en fukt-och värmebehandling av sädeskornet som används vid framställning av skrädmjöl. Vid mältning fuktas hela sädeskornet till groning vilket framför allt används i framställning av öl, men också för att göra mältat mjöl.
Genom nästan fullständig nedbrytning av fytinsyra kan järnupptaget bli nästan lika bra från växtbaserade livsmedel som från kött. Detta har visats i kontrollerade studier på människa (15, 16). Vid fermentering, till exempel mjölksyrajäsning, kan man välja mikroorganismer som bryter ner de hämmande faktorerna. Men det gäller att ha de rätta förhållandena under beredning och process för att nå syftet med ökad biotillgänglighet (17)! Val av sorter av spannmål och baljväxter är också viktigt, inte bara på grund av skillnader i mineralinnehåll, utan också på stora skillnader i innehåll av hämmande faktorer, som fytinsyra och polyfenoler, och enzymaktivitet (fytas, polyfenoloxidas).
Fler näringsrika produkter behövs
Idag finns ett flertal växtbaserade produkter på marknaden, varav många är baserade på sojaprotein. Flera av dem har ett högt innehåll av mättat fett (palmolja) och salt, och en del har låg biotillgänglighet av mineraler. Livsmedelsprocessens effekt på näringsvärdet kan vara både positivt och negativt och är därför viktigt att dokumentera. Det är en utmaning för livsmedelsindustrin att ta fram växtbaserade produkter med hög biotillgänglighet av järn och zink så att ett proteinskifte inte leder till försämrad järn- och zinkstatus, särskilt hos unga kvinnor.
Referenser
1. Willet W et al. Food in the Anthropocene: the EAT Lancet Commission on healthy diets from sustainable food systems. The Lancet 2019;393:447.
2. Bryngelsson S och Jonsson K. Mat, hälsa och hållbarhet-EAT-Lancet i nordiskt perspektiv. Nutritionsfakta 11 febr, 2020.
3. Mozaffarian D. Dietary and Policy Priorities for Cardiovascular Disease, Diabetes and Obesity. Circulation 2016;133:187.
4. Craig W. Health effects of vegan diets. Am J Clin Nutr 2008;89(suppl):1627S.
5. Moretti D. Plant-Based Diets and Iron Status. In Vegetarian and Plant-Based Diets in Health and Disease Prevention, Chapt 39, 2017, Elsevier Inc p 715.
6. Hunt J. Bioavailability of iron, zinc and other trace minerals from vegetarian diets. Am J Clin Nutr 2003;78 (suppl):633S.
7. Larsson I & Hulthén L. Nutritionella och vetenskapliga reflektioner på EAT-Lancet rapporten. Dietistaktuellt Nr2, mars 2019, s 42.
8. Sandberg A-S & Scheers N. Phytic acid: properties, uses and determination. In The Encyclopedia of Food and Health, 2016, vol 4, p 365, Eds. Caballero B, Finglas P & Toldra F. Oxford:Academic Press.
9. Petry N et al. Polyphenols and Phytic Acid Contribute to the Low Iron Bioavailability from Common Beans in Young Women. J Nutr 2010;140:1977.
10. Lönnerdal, B. Calcium and Iron Absorption–Mechanisms and Public Health Relevance. Int J Vitam Nutr Research 2010;80:293.
11. Riksmaten ungdom 2016-2017. Så äter ungdomar i Sverige. Del.2. Näringsintag och näringsstatus bland ungdomar i åk 5, åk 8 och åk 2 på gymnasiet. Livsmedelsverkets rapportserie nr 23, 2018. Livsmedelsverket, 2018.
12. Stoltzfus, R. J. Iron Deficiency: Global Prevalence and Consequences. Food and Nutrition Bulletin 2003;24:S99.
13. Foster M & Samman S. Vegetarian Diets Across the Lifecycle: Impact on Zinc Intake and Status. In Advances in Food and Nutrition Research, 2015, Vol 74, Chapt 3. p 93.
14. Sandberg, A-S. Bioavailability of minerals in legumes Brit J Nutr 2002;88,Suppl 3:S281.
15. Brune et al. Human iron absorption from bread: inhibiting effects of cereal fiber, phytate and inositol with different number of phosphate groups. J Nutr 1992;122:442.
16. Hurrell RF. Influence of Vegetable Protein Sources on Trace Element and Mineral Bioavailability. J Nutr 2003;133:2973S.
17. Fredlund K et al. Hydrothermal treatment and malting of barley improved zinc absorption in humans. Eur J Clin Nutr 2003;57:1507.
Prenumerera på vårt nyhetsbrev
Senaste inläggen
- Ätbeteenden och psykologiska faktorer – påverkan på viktminskning vid behandling av svår obesitas
- Hälsosam nordisk kost och kost rik på fleromättat fett med mindre kolhydrater – effekter på leverfett vid typ 2-diabetes och prediabetes
- Tarmfloran genom livet – hur kost, miljö och åldrande formar tarmens mikrobiota
- Varma julhälsningar från oss på Nutritionsfakta
- Begränsat med fiber är relaterat till åderförfettningsplack i hjärtats kranskärl